Cyberaanvallen op ziekenhuizen kunnen verwoestende gevolgen hebben, vooral voor afdelingen radiologie en radiotherapie die in het bijzonder afhankelijk zijn van technologie om te kunnen functioneren. Een voorbeeld hiervan is de landelijke cyberaanval op de Ierse volksgezondheidsdiensten in mei 2021, waarbij geplande radiotherapiebehandelingen voor sommige kankerpatiënten tot 12 dagen werden onderbroken.
Na dit incident hebben medisch fysici van Universitair Ziekenhuis Galway en Nationale universiteit van Ierland, Galway begon een interne tool te ontwikkelen om herziene behandelplannen voor radiotherapie op te stellen na onderbrekingen. De tool – genaamd EQD2VH – berekent behandelcompensatieplannen en maakt visuele vergelijking mogelijk van alle planopties, evenals individuele analyse van elke structuur in het plan van een patiënt. De onderzoekers beschrijven de nieuwe softwaretool in de Tijdschrift voor Toegepaste Klinische Medische Fysica.
Radiotherapie wordt meestal gedurende meerdere weken toegediend in een reeks kleine stralingsdoses (conventioneel 2 Gy) die fracties worden genoemd. Ongeplande hiaten in de behandeling - of het nu gaat om cyberaanvallen, machinestoringen of ziekte van de patiënt - kunnen aanzienlijke tegenslagen veroorzaken. Tijdens dergelijke hiaten herbevolken kankercellen zich snel in tumorweefsel, wat resulteert in een verlaging van de radiobiologische dosis tot het planningsdoelvolume (PTV).

Om dit probleem aan te pakken, EQD2VH gebruikt dosis-volumehistogram (DVH)-informatie die is geëxtraheerd uit oorspronkelijke patiëntenplannen om berekeningen van de behandelingsafstand uit te voeren. Hoofdauteur Katie O'Shea, van de National University of Ireland Galway, en collega's leggen uit dat de software de fysieke dosis in elke dosisbak (het dosisbereik tussen gegevenspunten in een DVH) omzet in de biologisch effectieve dosis (BED). Dit verklaart zowel de herbevolkingseffecten in de PTV als de effecten van subletale schade aan niet-gerepareerd normaal weefsel in risicoorganen (OAR's).
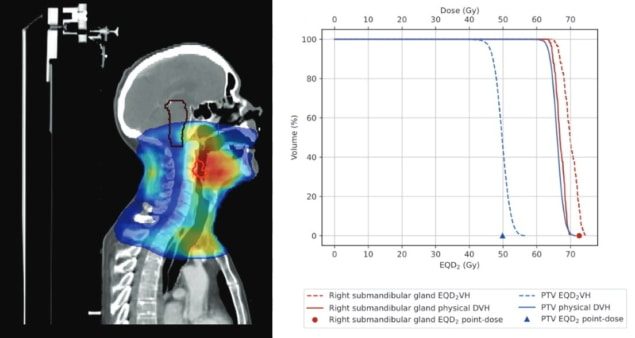
Na het wijzigen van de BED-conversie om rekening te houden met dosisvariaties in elke structuur, met behulp van een methode met variabele dosis, zet het hulpmiddel het BED voor elke structuur om in de equivalente dosis in fracties van 2 Gy (EQD2). Dit normaliseert elke behandeling naar conventionele fractionering en maakt het mogelijk om plannen met verschillende fractioneringsschema's bij elkaar op te tellen. De resulterende EQD2 -gebaseerde DVH biedt een 2D-weergave van de impact van compensatiestrategieën voor behandelingskloven op zowel PTV- als OAR-dosisverdelingen, in vergelijking met het voorgeschreven behandelplan.
EQD evalueren2VH als een hulpmiddel voor klinische besluitvorming, selecteerden de onderzoekers vijf patiënten met hoge prioriteit met snelgroeiende tumoren bij wie de behandelingskloven niet langer mogen zijn dan twee dagen. Dit omvatte vier patiënten met hoofd-halskanker die intensiteit-gemoduleerde radiotherapie ondergingen en één longkankerpatiënt die 3D-conforme radiotherapie onderging, met een behandelingspauze van 12 of 13 dagen. Deze cases stelden het team in staat om het gebruik van EQD . te evalueren2VH voor patiënten met zowel conventionele (2 Gy) als niet-conventionele (2.2 Gy) fractionering en verschillende behandelingsintervallen (van negen tot 46 dagen in hun therapie).
De herziene behandelplannen voor elke patiënt waren gebaseerd op hun oorspronkelijke plannen, waarbij ofwel de dosis per fractie of het aantal fracties werd gewijzigd. O'Shea legt uit dat het herziene plan en schema van elke patiënt een combinatie van tweemaal daagse fractionering, weekendbehandelingen en verhoogde dosis tot het doelvolume gebruikte om de effecten van celrepopulatie te verminderen.
De plannen beperkten de behandeling tot zes fracties per week en sloten tweemaal daagse fractionering op opeenvolgende dagen uit. Als de voorgeschreven behandeling niet binnen het vereiste tijdsbestek kon worden afgerond, onderzochten de onderzoekers plannen met behulp van hypofractionering (toediening van verhoogde dosis per fractie). Ze waren in staat om verschillende herziene plannen visueel en kwantitatief te vergelijken met het oorspronkelijke plan van de patiënt om te bepalen welke de beste dosis aan de PTV zou leveren met de minste dosis aan OAR's.
De onderzoekers merken op dat de 2D-weergave van elke individuele structuur in EQD2VH biedt een meer diepgaande analyse dan de door het Royal College of Radiologists (RCR) aanbevolen 1D-puntdosisberekeningsmethode die momenteel wordt gebruikt om hiaten in de radiotherapie te beheren. Een 1D-weergave van de dosisverdeling binnen een volume houdt geen rekening met OAR's die doorgaans een niet-uniforme dosisverdeling hebben en zou de OAR-dosis kunnen overschatten. Bovendien is de EQD2De VH-tool kan plannen maken voor elke behandelingskloof, terwijl de RCR-richtlijnen gebaseerd zijn op een standaardkloof van vier tot vijf dagen.
Bijkomende voordelen van de nieuwe tool zijn onder meer de mogelijkheid om elke OAR in het plan van de patiënt te volgen om verdere dosisverhogingen die meer acute toxiciteiten zouden kunnen veroorzaken, tot een minimum te beperken. Gebruikers kunnen ook de impact van verschillende behandelingspauzes op de behandeling van een patiënt berekenen. Deze mogelijkheid kan helpen bepalen of een patiënt naar een andere kliniek moet worden overgebracht als de onderbreking in de geplande kliniek te lang is of dat de patiënt veilig kan wachten tot de behandeling wordt hervat.

Hoe heeft COVID-19 de verstrekking van bestralingstherapie beïnvloed?
EQD2VH kan ook verantwoordelijk zijn voor veranderingen in de totale behandeltijd en subletale schade in normaal weefsel, wat een commercieel systeem mogelijk niet kan doen. Het belangrijkste is dat de tool niet verbonden hoeft te zijn met het ziekenhuisnetwerk om te kunnen functioneren - hij kan zelfs worden gebruikt als de servers van een ziekenhuis nog steeds verlamd zijn door een cyberaanval.
“We evalueren nog steeds EQD2VH als hulpmiddel bij het nemen van beslissingen”, zegt hoofdonderzoeker Margaret Moore van het University Hospital Galway. “Het maakt deel uit van een huidig project waarin patiënten worden beoordeeld die meerdere herbehandelingen ondergaan voor palliatieve regimes waarbij de dosis-per-fractie niet-standaard is en waarbij er een keuze kan zijn uit fractioneringsschema's om te overwegen. Omrekenen van behandeldosis van een aantal behandelingen met verschillende fractioneringen naar EQD2 maakt het mogelijk om de radiobiologische dosis gericht op weefsels en OAR's te accumuleren voor een algemeen dosisoverzicht, wat kan helpen bij de besluitvorming voor de keuze van verdere behandeling."