HONG KONG, 17 februari 2022 – (ACN Newswire) – SinoMab BioScience Limited ("SinoMab" of het "Bedrijf", samen met zijn dochterondernemingen, de "Groep", aandelencode: 3681.HK), een in Hong Kong gevestigd biofarmaceutisch bedrijf dat zich toelegt op onderzoek, ontwikkeling, productie en commercialisering van therapieën voor de behandeling van immunologische ziekten, is verheugd aan te kondigen dat, op 11 februari 2022 (EST lokale tijd), een Investigational New Drug-toepassing ("IND"), voor de First-in-Class (FIC) astmatherapeutisch product SM17 (gehumaniseerd anti-IL17RB monoklonaal antilichaam voor injectie) is ingediend en geaccepteerd door de Amerikaanse Food and Drug Administration ("FDA"). Het bedrijf is van plan om de First-In-Human-studie in de VS in het eerste kwartaal van 2022 te starten, zodra de IND is goedgekeurd door de FDA.
 |
SM17 is 's werelds eerste monoklonale antilichamen gericht op IL17BR, mede ontwikkeld door SinoMab en LifeArc (een liefdadigheidsinstelling voor medisch onderzoek gevestigd in het Verenigd Koninkrijk). SM17 heeft een breed scala aan indicaties, waaronder indicaties met grote marktvolumes zoals astma en ziekten met hoge sterftecijfers zoals idiopathische longfibrose. In vergelijking met andere producten op de markt geniet SM17 differentiatievoordelen. Met de preklinische gegevens en het unieke werkingsmechanisme van SM17 is het bedrijf van mening dat SM17 mogelijk een breder en gunstiger effect heeft op de behandeling van astma dan andere goedgekeurde biologische geneesmiddelen.
Op de wereldmarkt neemt het aantal astmapatiënten geleidelijk toe en zal naar verwachting 247.5 miljoen bedragen in 2023 en verder toenemen tot 267.7 miljoen in 2030. Het aantal astmapatiënten in de VRC neemt sneller toe dan het wereldwijde aantal en zal naar verwachting 25.6 miljoen bedragen in 2023 en verder toenemen tot 27.8 miljoen in 2030. In termen van marktomvang zal de wereldwijde astmamarkt naar verwachting 25.1 miljard dollar bereiken in 2023 en 34.6 miljard dollar in 2030. De astmamarkt in de Verwacht wordt dat de VRC tegen 36.4 2023 miljard RMB zal bereiken en tegen 65.0 2030 miljard RMB. Wat de behandelingsopties betreft, is de traditionele astmabehandeling gebaseerd op inhalatiecorticosteroïden, maar ze zijn vatbaar voor ernstige bijwerkingen, vooral bij adolescenten. Geneesmiddelresistentie kan zich ook ontwikkelen als het gedurende lange tijd wordt gebruikt. De introductie van SM17 zal naar verwachting een betere behandelingsoptie bieden in termen van de balans tussen werkzaamheid en veiligheid.
Dr. Shui On LEUNG, voorzitter, uitvoerend directeur en Chief Executive Officer van SinoMab zei dat: "na de aanvaarding van de IND-aanvraag voor SN1011 voor de behandeling van multiple sclerose door de NMPA, de aanvaarding van de SM17 IND-aanvraag door de FDA volledig toont de efficiënte uitvoering van het nieuwe R&D-programma voor geneesmiddelen van het bedrijf aan. Er is nog steeds een onvervulde medische behoefte aan aanvullende effectieve therapieën, met name voor patiënten die niet reageren op de huidige behandelingen. We hebben daarom vertrouwen in de enorme vooruitzichten van de klinische ontwikkeling van SM17. Onze kern producten, waaronder SM03, SN1011 en SM17, boeken soepel vooruitgang op het gebied van klinische R&D, waardoor het bedrijf gestaag op weg is naar commercialisering. In de toekomst zullen we de implementatie van onze projecten versnellen om patiënten voordelen te bieden en waarde te creëren voor aandeelhouders door middel van innovatie."
Over SM17
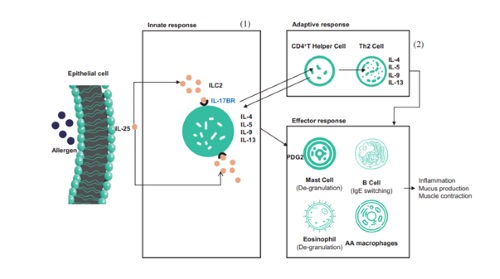
Van SM17 is bekend dat het 's werelds eerste gehumaniseerde IgG4-k monoklonale antilichaam is voor de ontwikkeling van nieuwe geneesmiddelen, dat zich richt op IL-17RB. En IL-17RB is een type I enkelvoudig transmembraan glycoproteïne dat behoort tot de IL-17-receptorfamilie. De binding van SM17 aan IL-17RB zou Th2-immuunreacties kunnen onderdrukken die worden geïnduceerd door een categorie cytokinen genaamd "alarmine", waarvan is aangetoond dat het betrokken is bij de pathogenese van allergische aandoeningen en virale reacties van de luchtwegen. Een alternatieve benadering die zich richt op stroomopwaartse mediatoren van de Th2-inflammatoire cascade, zoals "alarmins", zal naar verwachting een breder effect hebben op luchtwegontsteking en een effectievere astmacontrole bieden dan momenteel beschikbare therapieën, en producten met een vergelijkbaar werkingsmechanisme als SM17 zijn goedgekeurd door de FDA.
Over SinoMab BioScience Limited
SinoMab BioScience Limited (voorraadcode: 3681.HK) houdt zich bezig met onderzoek, ontwikkeling, productie en commercialisering van therapieën voor de behandeling van immunologische ziekten. Het vlaggenschipproduct van het bedrijf SM03 is een potentiële wereldwijde first-in-target mAb tegen CD22 voor de behandeling van reumatoïde artritis (RA) en bevindt zich momenteel in een klinische fase III-studie voor reumatoïde artritis in China, die is erkend als een van de significante speciale projecten voor de ontwikkeling van significante nieuwe geneesmiddelen van de twaalfde vijfjarenplanperiode en de dertiende vijfjarenplanperiode. Daarnaast beschikt de Vennootschap over andere potentiële first-in-target en first-in-class kandidaat-geneesmiddelen, waarvan sommige zich al in het klinische stadium bevinden, met indicaties voor reumatoïde artritis (RA), systemische lupus erythematosus (SLE), pemphigus vulgaris (PV), non-Hodgkin-lymfoom (NHL), astma en andere ziekten met grote onvervulde klinische behoeften.
Copyright 2022 ACN Newswire. Alle rechten voorbehouden. www.acnnewswire.comSinoMab BioScience Limited ("SinoMab" of het "Bedrijf", samen met zijn dochterondernemingen, de "Groep", aandelencode: 3681.HK), een in Hong Kong gevestigd biofarmaceutisch bedrijf dat zich toelegt op onderzoek, ontwikkeling, productie en commercialisering van therapieën voor de behandeling van immunologische ziekten
- 11
- 2022
- 7
- versnellen
- ACN Nieuwslijn
- Actie
- Extra
- voordelen
- Alles
- al
- aankondigen
- Aanvraag
- nadering
- Beschikbaar
- gelooft
- betekent
- Miljard
- voorzitter
- Goede doel
- chef
- chief executive officer
- China
- code
- commercialisering
- afstand
- zeker
- onder controle te houden
- auteursrecht
- kon
- Actueel
- gegevens
- toegewijd aan
- ontwikkelen
- Ontwikkeling
- Director
- Ziekte
- ziekten
- aandrijving
- drug
- Drugs
- effect
- effectief
- enorm
- vooral
- uitvoerend
- Leidinggevend directeur
- verwacht
- familie
- FDA
- Voornaam*
- volgend
- eten
- toekomst
- Globaal
- Hoge
- HTTPS
- Inclusief
- Laat uw omzet
- Innovatie
- bekend
- Groot
- Beperkt
- lokaal
- lang
- groot
- maken
- productie
- Markt
- medisch
- miljoen
- Officier
- Keuze
- Opties
- Overige
- fase
- Product
- Producten
- Programma
- projecten
- zorgen voor
- Quarter
- R & D
- reeks
- Tarieven
- onderzoek
- Veiligheid
- Zei
- aanzienlijke
- gelijk
- Maat
- Stadium
- voorraad
- Studie
- ingediend
- Door
- niet de tijd of
- samen
- traditioneel
- behandeling
- proces
- ons
- unieke
- United
- United Kingdom
- waarde
- WIE