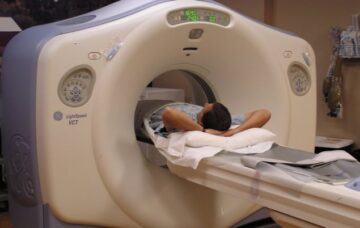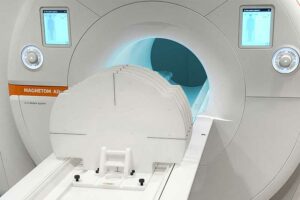
Stereotactische lichaamsstralingstherapie (SBRT) is een precisiebehandeling van kanker die minder stralingsfracties met een hogere dosis oplevert dan traditionele radiotherapie. SBRT kan uitstekende lokale tumorcontrole bieden, maar voor sommige tumorlocaties bestaat het risico dat nabijgelegen risicoorganen (OAR's) worden blootgesteld aan onaanvaardbare bestralingsniveaus. Op protonen gebaseerde SBRT biedt een betere OAR-besparing, maar vereist nog steeds enige behandelingsmarges die de klinische toepasbaarheid ervan kunnen beperken.
FLASH-radiotherapie, waarbij straling wordt toegediend met ultrahoge dosissnelheden, zou het verder sparen van OAR's mogelijk kunnen maken. Om het potentieel ervan te onderzoeken, heeft een onderzoeksteam leiding gegeven aan Emory University ontwikkelt een raamwerk voor het optimaliseren van de levering van protontherapie om te voldoen aan de eisen van FLASH-radiotherapie.
De meeste moderne protontherapiesystemen kunnen FLASH-dosissnelheden bereiken met behulp van een hoogenergetische transmissiebundel die door de patiënt gaat en de dosis gedurende zijn hele traject afgeeft. Deze aanpak elimineert echter het grote voordeel van protonentherapie: het vermogen ervan om doses af te geven in een gespreide Bragg-piek. Om de conformiteit bij FLASH-dosissnelheden te verbeteren, Ruirui Liu en collega's stellen voor dat patiëntspecifieke randfilters een dosisverdeling kunnen bieden die vergelijkbaar is met die van conventionele intensiteitsgemoduleerde protontherapie (IMPT).
Voor FLASH-behandelingen zijn de dosis, het dosisgemiddelde dosistempo (DADR) en de dosisgemiddelde lineaire energieoverdracht (LETd) beïnvloeden allemaal de biologische respons. Daarom ontwikkelden de onderzoekers een geïntegreerd raamwerk voor fysieke optimalisatie (IPO) dat tegelijkertijd deze drie parameters optimaliseert om de OAR-besparing in het behandelplan van een patiënt te maximaliseren. Het raamwerk, beschreven in de International Journal of Radiation Oncology, Biologie, Natuurkunde, maakt gebruik van de IPO-IMPT-objectieffunctie om meerdere oplossingen te bieden voor het ontwerp van patiëntspecifieke randfilters en protonspotkaarten.
De randfilters, die worden gebruikt in combinatie met een bereikcompensator, bestaan uit een reeks zigguratvormige pinnen die de Bragg-piek van een straal van 250 MeV verspreiden om een straalspecifiek planningsdoelvolume te bestrijken. Het team ontwikkelde software voor inverse planning om de pinlocaties voor een patiëntspecifiek filter te definiëren, en gebruikte op Geant4 gebaseerde Monte Carlo-simulaties om dosis- en LET-invloedmatrices te verkrijgen.

Patiëntenplannen
Om het IPO-IMPT-raamwerk te demonstreren, ontwikkelden de onderzoekers behandelplannen voor drie patiënten met longkanker. Ze schreven een dosis van 50 Gy (vijf fracties van 10 Gy) voor op het klinische doelvolume, met een maximale hotspotdosis van 62.5 Gy. Afhankelijk van welke parameter prioriteit krijgt, zijn de plannen erop gericht de FLASH-dekking te vergroten en/of de LET te verminderend, met behoud van de doeldosis.
Voor patiënt 1, die een centrale longtumor dichtbij het hart had, waren de OAR's het hart en de long. Voor dit geval hebben de onderzoekers een IPO-IMPT-plan met één bundel gegenereerd met als doel de LET te verminderend naar het hart terwijl de doeldekking behouden blijft. Het IPO-IMPT-plan voldeed aan dit doel en vertoonde een vergelijkbare doelstellingsdekking als een conventioneel IMPT-plan, maar verminderde de LET aanzienlijkd naar het hart.
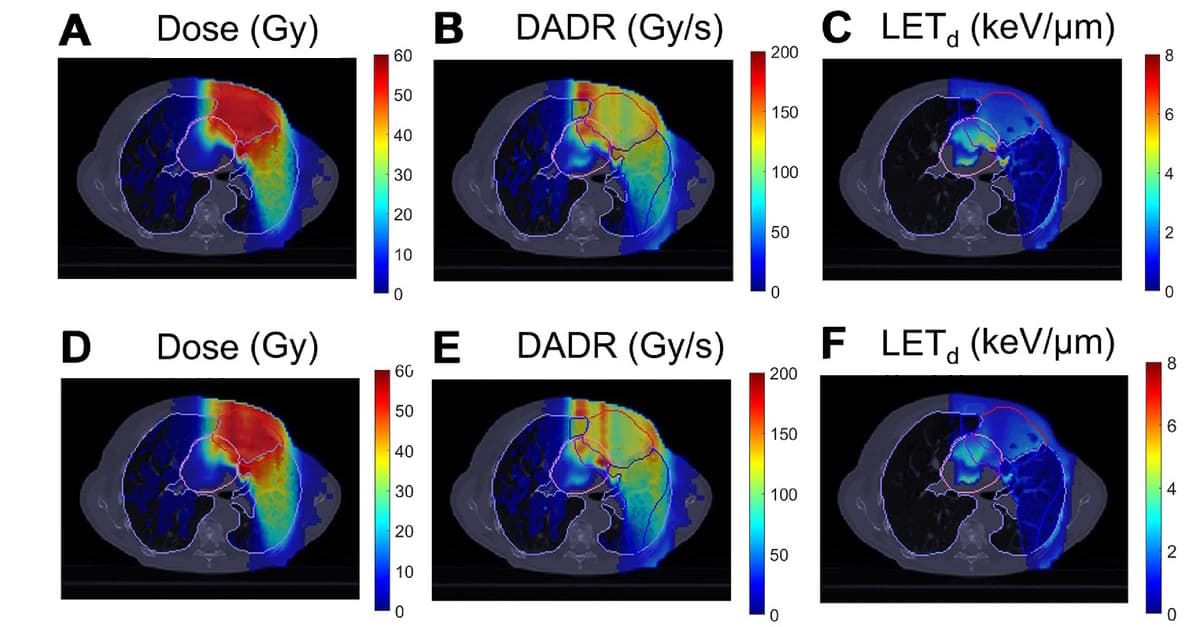
Patiënt 2 had een metastatische tumor in de rechter onderkwab en patiënt 3 had een tumor in de subcarinale lymfeklier. In deze gevallen was de slokdarm ook een OAR en was het belangrijkste doel het sparen van de slokdarm. Voor zowel IPO-IMPT als IMPT voldeed bijna 100% van het slokdarmevaluatievolume aan de FLASH-drempel van 40 Gy/s. Bij patiënt 2 verlaagde IPO-IMPT de LET lichtjesd voor het hart en de slokdarm en verhoogde FLASH-dekking voor het hart.
Spaar pin-ontwerp
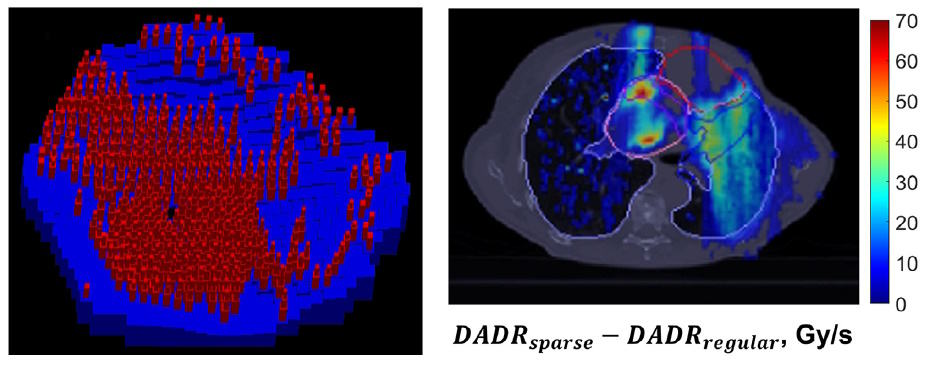
Reguliere randfilters, ontworpen met behulp van het IPO-IMPT-framework, spaarden selectief OAR's door de LET te verminderen en de FLASH-dekking te vergroten. Schaarse nokfilters, waarvan sommige pinnen zijn weggelaten, bieden echter mogelijkheden om de OAR-besparing verder te vergroten. Het verwijderen van filterpinnen op specifieke locaties levert een hogere protonenflux op, terwijl de resterende pinnen nog steeds voldoende doeldekking bieden.
Voor patiënt 1 genereerden de onderzoekers een IPO-IMPT-plan met dunne randfilters en meerdere bundels. Vergelijking met een IMPT-plan met reguliere nokfilters toonde aan dat voor beide de tumordekking behouden bleef en de hotspots goed onder controle waren. De schaarse randfilters verhoogden echter het OAR-volume dat een FLASH-dosis ontving met respectievelijk 31% en 50%, voor respectievelijk hart- en longevaluatievolumes.
De spaarse randfilters bieden flexibiliteit om het volledige potentieel van het IPO-IMPT-framework te realiseren. De pinverwijderingsniveaus kunnen bijvoorbeeld worden afgestemd op individuele patiëntcasussen. Een drempelwaarde voor het verwijderen van pinnetjes van 50% leverde redelijke resultaten op voor de grote tumor van patiënt 1, terwijl een drempelwaarde van 30% een goed uitgangspunt was voor de kleinere doelwitten van patiënten 2 en 3, bij wie de op spaarzame randfilters gebaseerde plannen de DADR in de slokdarm verhoogden terwijl de tumor behouden bleef. Dekking.
Om te verifiëren dat een nokfiltersamenstel (filterpennen en een compensator) de voorspelde dosis zou kunnen leveren, hebben de onderzoekers ten slotte een patiëntspecifiek nokfilter in 3D geprint. Ze leverden een behandelplan op dat was ontworpen om een uniforme doeldosis te bieden en voerden dosismetingen uit met een ionisatiekamerarray. Het totale gamma-goedkeuringspercentage bedroeg 92.9% voor absolute doses, wat hoger is dan de standaard patiëntencriteria van 90%, wat aantoont dat de assemblage een klinisch aanvaardbare dosisverdeling kan opleveren.

NPL introduceert absolute dosimetrie voor FLASH-protonenbundels
“Deze proof-of-concept studie toont de haalbaarheid aan van het gebruik van een IPO-IMPT-framework om FLASH stereotactische lichaamsprotonentherapie te verwezenlijken, rekening houdend met dosis, DADR en LETd tegelijkertijd”, concluderen de onderzoekers. “Deze nieuwe methode zal de levering van conforme protonvelden met FLASH-snelheden voor preklinische en klinische onderzoeken vergemakkelijken.”
Senior auteur Liyong Lin vertelt Natuurkunde wereld dat het team hoopt zijn software voor dergelijke toepassingen verder te ontwikkelen. “Emory's Office of Technology Transfer moedigde ons aan om een startend bedrijf op te richten, Radiotherapy Biological Optimization (RBO) Solutions”, legt Lin uit. “RBO is door het Applicant Assistance Program van de National Institutes of Health geaccepteerd om vóór 41 april een R5-subsidie voor technologieoverdracht voor kleine bedrijven in te dienen bij het National Cancer Institute. IBA, de grootste leverancier van deeltjestherapie, en de dosimetrieafdeling van IBA zullen het RBO-subsidievoorstel voor R41 onderschrijven. ”
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- Platoblockchain. Web3 Metaverse Intelligentie. Kennis versterkt. Toegang hier.
- Bron: https://physicsworld.com/a/patient-specific-ridge-filters-enable-conformal-flash-proton-therapy/
- :is
- $UP
- 1
- 10
- 2023
- 3d
- a
- vermogen
- absoluut
- aanvaardbaar
- bereiken
- Accounting
- Bereiken
- Voordeel
- Alles
- en
- toepassingen
- nadering
- April
- ZIJN
- reeks
- bijeenkomst
- Hulp
- At
- auteur
- BE
- Balk
- Betere
- tussen
- Grootste
- biologie
- lichaam
- bedrijfsdeskundigen
- by
- CAN
- Kanker
- Kanker
- geval
- gevallen
- centraal
- Klimaatkamers
- Charles
- Kinderen
- Klik
- Klinisch
- Sluiten
- collega's
- combinatie van
- afstand
- vergelijking
- concludeert
- onder controle te houden
- gecontroleerd
- conventioneel
- kon
- deksel
- dekking
- criteria
- leveren
- geleverd
- levert
- levering
- eisen
- tonen
- demonstreert
- Afhankelijk
- beschreven
- Design
- ontworpen
- ontwikkelen
- ontwikkelde
- het ontwikkelen van
- verschil
- distributie
- Uitkeringen
- Divisie
- elimineert
- in staat stellen
- aangemoedigd
- onderschreven
- energie-niveau
- evaluatie
- voorbeeld
- overschrijdt
- uitstekend
- exposeren
- Verklaart
- vergemakkelijken
- Velden
- filter
- filters
- flash
- Flexibiliteit
- FLUX
- Voor
- formulier
- Achtergrond
- oppompen van
- vol
- functie
- verder
- gegenereerde
- doel
- goed
- toe te kennen
- opschrift
- Hart
- hoger
- bezit
- hoopt
- hotspot
- Echter
- HTML
- HTTPS
- beeld
- verbeteren
- BELASTING
- in
- Laat uw omzet
- meer
- meer
- individueel
- beïnvloeden
- informatie
- Instituut
- geïntegreerde
- Introduceert
- onderzoeken
- IPO
- kwestie
- IT
- HAAR
- tijdschrift
- jpg
- sleutel
- Groot
- niveaus
- LIMIT
- lokaal
- locaties
- Het handhaven
- groot
- Maps
- marges
- max-width
- Maximaliseren
- maximaal
- maten
- Maak kennis met
- methode
- Modern
- meervoudig
- nationaal
- knooppunt
- roman
- doel van de persoon
- of
- bieden
- Kantoor
- on
- open
- optimalisatie
- Optimaliseert
- optimaliseren
- parameter
- parameters
- deeltjes therapie
- passes
- Voorbijgaand
- pad
- patiënt
- patiënten
- Hoogtepunt
- Fysiek
- pijnboom
- plan
- planning
- plannen
- Plato
- Plato gegevensintelligentie
- PlatoData
- punt
- potentieel
- precisie
- voorspeld
- geprioriteerd
- Programma
- voorstel
- voorstellen
- protonen
- zorgen voor
- mits
- biedt
- radiotherapie
- reeks
- tarief
- Tarieven
- realiseren
- redelijk
- ontvangende
- verminderen
- vermindering
- regelmatig
- resterende
- verwijdering
- het verwijderen van
- vereist
- onderzoek
- onderzoekers
- antwoord
- Resultaten
- risico's
- s
- gelijk
- gelijktijdig
- Klein
- kleine bedrijven
- kleinere
- Software
- Oplossingen
- sommige
- specifiek
- Spot
- verspreiden
- standaard
- Start
- startup
- Still
- studies
- Studie
- voorleggen
- dergelijk
- Systems
- op maat gemaakt
- doelwit
- doelen
- team
- Technologie
- vertelt
- dat
- De
- Deze
- drie
- drempel
- Door
- overal
- thumbnail
- naar
- Totaal
- traditioneel
- overdracht
- behandeling
- waar
- us
- verkoper
- controleren
- volume
- volumes
- GOED
- welke
- en
- WIE
- wil
- Met
- zephyrnet