Myelin er et beskyttende lag som dannes rundt nerver for å isolere dem og øke hastigheten på overføring av elektriske impulser. Demyelinisering, tap av dette isolerende laget, bidrar til mange nevrologiske sykdommer, inkludert multippel sklerose, Alzheimers sykdom, hjerneslag og demens. En effektiv teknikk for å oppdage denne potensielt reversible tilstanden kan forbedre diagnoser av hjernesykdommer og muliggjøre overvåking av mulige behandlinger. For øyeblikket kan imidlertid ingen avbildningstester nøyaktig identifisere demyelinisering.
For å løse denne mangelen har forskere fra Gordon senter for medisinsk bildebehandling ved Massachusetts General Hospital og Harvard Medical School undersøker bruken av en ny PET-radiotracer – 18F-3-fluor-4-aminopyridin (18F-3F4AP) – for å avbilde demyeliniserte lesjoner i hjernen. De har nå testet sporstoffet på mennesker for første gang, og rapporterte funnene deres i European Journal of Nuclear Medicine and Molecular Imaging.
"Å ha et bildeverktøy som er spesifikt for demyelinisering, kan bidra til bedre å forstå bidraget av demyelinisering til forskjellige sykdommer og bedre overvåke en sykdom eller responsen på terapi - for eksempel en remyeliniserende terapi," sier førsteforfatter Pedro Brugarolas i en pressemelding.
18F-3F4AP er en radiofluorert versjon av multippel sklerosemedisinen 4-aminopyridin. Sporstoffet, som kommer inn i hjernen via passiv diffusjon, binder seg til demyeliniserte aksoner på lignende måte som selve stoffet. Tidligere studier har vist at PET med 18F-3F4AP kan oppdage lesjoner i en rottemodell for demyelinisering, og at sporstoffet har egnede egenskaper for å avbilde hjernen til rhesus-makaker, noe som får teamet til å undersøke bruken hos mennesker.
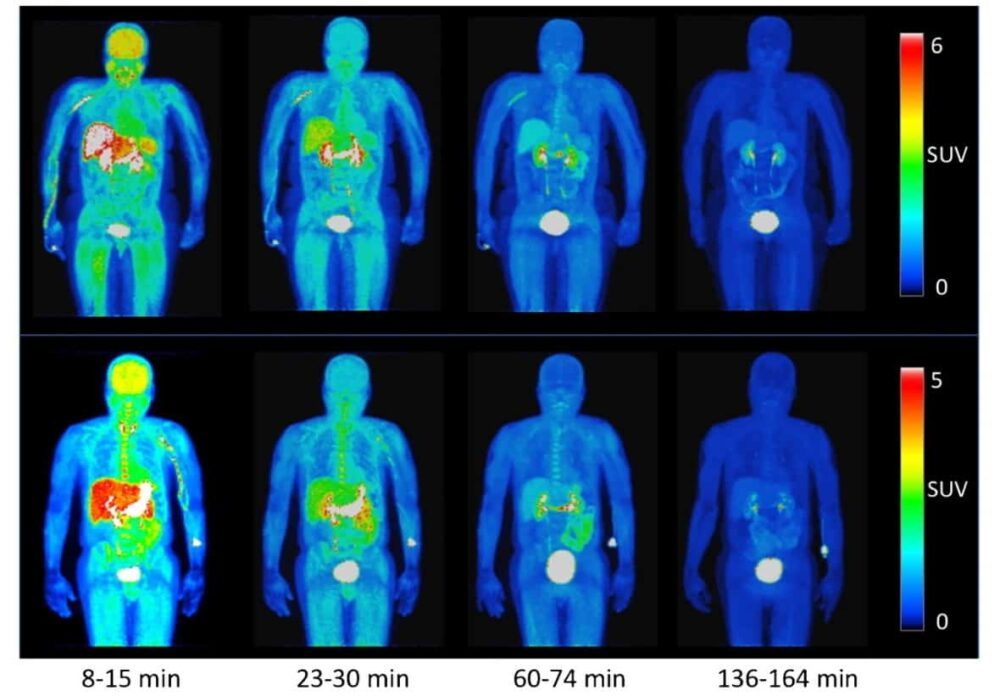
Brugarolas og kolleger utførte PET-skanninger på fire friske frivillige etter å ha administrert 368±17.9 MBq av 18F-3F4AP. Etter en lavdose CT-skanning startet de PET umiddelbart etter sporstoffinjeksjon, og tok opp en serie bilder i syv skannersengeposisjoner for å dekke hele kroppen. For å fange sporingskinetikken og maksimere bildekvaliteten, var den første skannetiden per posisjon 1 min, og økte til 2, 4 og 8 minutter per posisjon. Hele PET-anskaffelsen tok 4 timer.
De resulterende PET-bildene og tidsaktivitetskurvene (TACs) avslørte at sporstoffet distribuerte seg raskt gjennom hele kroppen, inkludert hjernen, og raskt fjernet via nyreutskillelse. 8–14 minutter etter injeksjon ble det sett maksimal aktivitet i lever, nyrer, urinblære, milt, mage og hjerne. Ved 22–28 min var den høyeste aktiviteten i nyrene, galleveiene og urinblæren. Etter 60 minutter var det meste av aktiviteten fjernet fra organene og samlet seg i urinblæren.
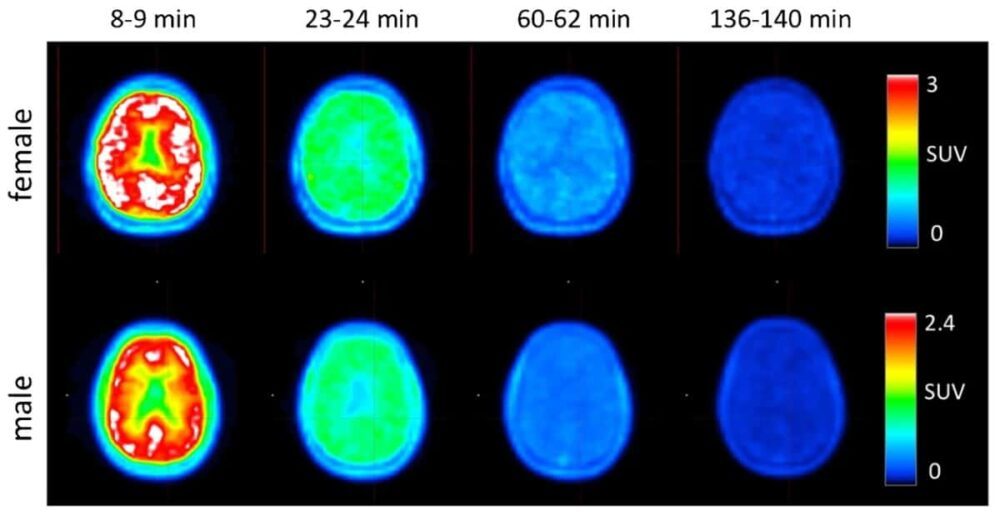
Teamet brukte også de integrerte TAC-ene til å utføre dosimetri. Den gjennomsnittlige effektive dosen var 12.2 ± 2.2 µSv/MBq for de fire deltakerne, uten forskjeller sett mellom mannlige og kvinnelige frivillige. Forskerne bemerker at denne effektive dosen er betydelig lavere enn den estimerte fra ikke-menneskelige primatstudier (21.6 ± 0.6 µSv/MBq), sannsynligvis på grunn av den raskere clearance sett hos mennesker enn i rhesus-makaker. Denne dosen var også lavere enn for andre PET-sporstoffer, som f.eks 18F-FDG.
Det er viktig at sporings- og bildebehandlingsprosedyren ble godt tolerert av alle deltakerne, uten at det oppsto uønskede hendelser under skanningen. Det var ingen signifikante forskjeller i frivilliges vitale tegn (temperatur, blodtrykk og oksygenmetning) før og etter skanningen, og ingen signifikante endringer i blodmetabolitt- og elektrokardiogramresultater oppnådd innen 30 dager før og etter skanningen.

PET-sporstoff måler demyelinisering hos mus
Det konkluderer forskerne med 18F-3F4AP kommer lett inn i hjernen og er trygg for bruk hos mennesker, med et akseptabelt nivå av stråledose. De foreslår at funnene deres åpner døren for videre studier som undersøker sporstoffets evne til å oppdage demyeliniserte lesjoner i forskjellige pasientpopulasjoner.
Brugarolas forteller Fysikkens verden at teamet for tiden forfølger to små kliniske studier som bruker det nye sporstoffet: for å undersøke verdien for avbildning av multippel sklerose; og å vurdere bruken hos pasienter med traumatisk hjerneskade, mild kognitiv svikt og Alzheimers sykdom.