Positron emisjonstomografi (PET) er en medisinsk bildeteknologi som er mye brukt for både kliniske og prekliniske applikasjoner. Innen kreftomsorgen, radiotraceren 18F-FDG (fluor-18-fluordeoksyglukose) brukes i PET/CT-skanninger for å identifisere økt glukoseinntak, et kjennetegn på kreftceller. Og forskere har utviklet en rekke ekstra radiosporere for å målrette andre sykdomsspesifikke markører.
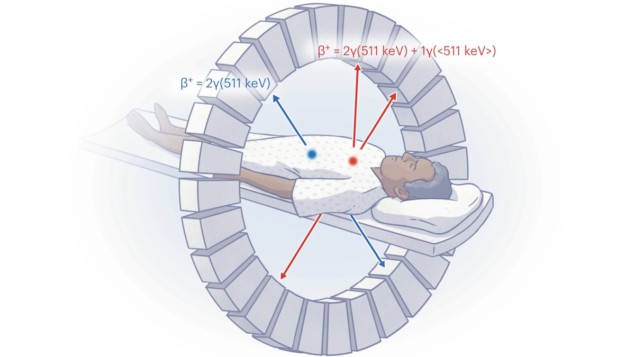
PET fungerer ved å detektere to 511 keV annihileringsfotoner som dannes når et positron som sendes ut av radiotraceren tilintetgjør med et elektron i kroppen. Men fordi alle PET-isotoper produserer de samme to 511 keV-fotonene, er det bare mulig å avbilde én radiosporing om gangen. Å oppdage signaturer fra mer enn ett sporstoff krever sekvensiell PET-skanning, men dette er kostbart, avhenger av at ett sporstoff forfaller tilstrekkelig over tid og øker pasientens strålingseksponering fra de medfølgende CT-skanningene.
Et forskningsteam ledet av denne begrensningen Jan Grimm at Memorial Sloan Kettering Cancer Center og Joaquin Herraiz at Complutense universitet i Madrid har utviklet en ny bilderekonstruksjonsmetode som muliggjør in vivo avbildning av to forskjellige PET-sporstoffer samtidig. Forskerne beskriver teknikken deres, kalt multiplexed PET (mPET), i Naturbiomedisinsk ingeniørfag.
"Dette fremskrittet kan bidra til å øke dybden av molekylær informasjon som er oppnåelig under en enkelt skanning, og gi både forskere og radiologer mer tidsriktig informasjon for en diagnose og iscenesettelse som ikke kunne gjøres med en biopsi," forklarer med-seniorforfatter Grimm i en pressemelding .
Utnytter prompt-gammaene
PET-bilder lages ved å bruke responslinjer (LOR) mellom detektorpar som oppdager to utslettelsesfotoner («doble» hendelser) innenfor et tilfeldighetstidsvindu på omtrent 3.5 ns. Noen positron-emitterende isotoper sender også ut et ekstra prompt gamma-foton. Hvis dette oppdages innenfor tilfeldighetsvinduet, gir det opphav til en "trippel" hendelse, som vanligvis anses som falsk og ikke rekonstruert. Ofte unngås slike isotoper i medisinske skanninger.
Men førsteforfatter Edwin Pratt og kolleger har vist hvordan man bruker denne umiddelbare gamma-utslippet til å skille mellom to radiosporere i en PET-skanning. Ved å øke tilfeldighetsenergivinduet til å inkludere den umiddelbare gamma-utslippet, og utvikle en metode for å skille og rekonstruere doble tilfeldigheter fra trippelsammentreff, kan de generere to separate datasett for hver PET-skanning.
Disse datasettene kan brukes til å produsere kvantitative bilder av to PET-radiosporere administrert samtidig, med lignende ytelse som to separate anskaffelser. "Ved å bruke et passende radiosporing-par (det ene inneholder en standard positron-emitterende isotop og det andre en isotop som også sender ut en prompt gamma), og en riktig bilderekonstruksjonsmetode (mPET), kan ekte simultan PET-bilde med to isotoper oppnås i de fleste nåværende PET-skannere, uten modifikasjoner eller behov for energidiskriminering, sier co-seniorforfatter Herraiz.
Forskerne testet først gjennomførbarheten av mPET-metoden deres på en preklinisk og en klinisk PET-skanner. De avbildet fantomer som inneholder den dobbeltemitterende isotopen zirkonium-89 (89Zr) og det trippel-emitterende jod-124 (124JEG). De fant at begge systemene kunne skaffe data egnet for mPET-separasjon, og at mPET-rekonstruksjonsmetoden kunne lage to samtidige isotopbilder. De flyttet deretter til in vivo prekliniske eksperimenter.
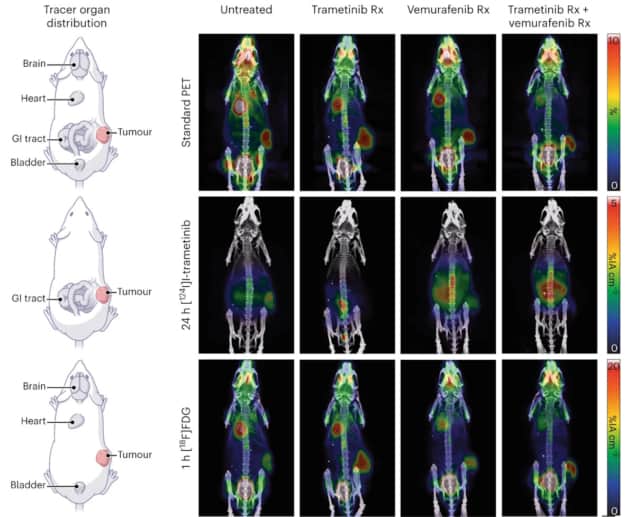
Hos mus med melanomsvulster brukte forskerne mPET for å spore biodistribusjonene til to injiserte radiosporere: 124I-trametinib, som retter seg mot prolifererende vev; og 18F-FDG, som retter seg mot glukoseaktivitet. Ved å separere de doble og tredoble hendelsene, observerte de to forskjellige biodistribusjoner fra de to sporstoffene. De avbildet også mus som mottok forskjellige medikamentelle behandlinger, og observerte at dobbel avbildning med mPET kunne brukes til å spore medisinenes effekter på svulsten samtidig som de opprettholder et standard FDG-PET-bilde.
Spore medikamentlevering
Nanopartikler er mye brukt som medikamentbærere og som midler for å endre biodistribusjon av legemidler, og reduserer ideelt sett levering utenfor målet. Ofte vurderes slik medikamentlevering ved å spore den radiomerkede nanopartikkelen og anta at medikamentfordelingen er den samme. Men dette er kanskje ikke alltid tilfelle. For å undersøke dette videre, brukte Pratt og kollegaer mPET for ikke-invasivt å overvåke og kvantifisere et radiomerket medikament og nanopartikkel separat.
Teamet administrerte 89Zr-ferumoxytol nanopartikler lastet med kreftmedisinen 124I-trametinib til en melanombærende mus. Bruk av mPET for å skille signaler fra stoffet og nanopartikkelen avslørte at kort tid etter injeksjon, samsvarte ikke medikamentfordelingen med bærenanopartiklen. Dette funnet tyder på at det meste av stoffet uventet hadde dissosiert raskt in vivo, og demonstrerer en verdifull anvendelse for denne nye teknikken.
Forskerne brukte også mPET for å spore CAR T-celler brukt i immunterapi for å målrette prostataspesifikke membranantigen (PSMA)-positive svulster. Hos mus med en PSMA-positiv svulst brukte de 124I å visualisere fordelingen av CAR T-celler og gallium-68 (68Ga)-PSMA-11 for samtidig å måle PSMA-positiv tumorplassering og uttrykk.
Evnen til mPET til å skille de to radiosporerne viste at det var distinkte fordelinger av 68Ga-PSMA-11 i svulsten, nyrene og blæren, mens 124Jeg ble funnet i svulsten, skjoldbruskkjertelen, nyrene, magen og blæren. Aksiale skiver gjennom svulsten avslørte forskjellige intratumorale fordelinger av de to sporstoffene. mPET-rekonstruksjonen ga en måte å spore målrettingen av CAR T-celler mens den bekreftet PSMA-uttrykk under samme PET-skanning.

Kompakt strålingsdetektor kan fremskynde bruken av dynamisk PET
Forskerne konkluderer med at mPET gir tilleggsinformasjon ved å legge til et ekstra sporstoff, og utnytter mange isotoper som tidligere ble sett på som problematiske på grunn av deres ekstra gamma-utslipp. De understreker at mPET kan implementeres på både prekliniske og kliniske PET/CT-systemer uten noen modifikasjoner av maskinvare eller programvare for bildeopptak. "Det fine er at mPET umiddelbart kan oversettes klinisk," sier Pratt. "Tilnærmingen kan gjøres på de fleste eksisterende maskiner, med minimale modifikasjoner."
Neste steg blir å bruke mPET på ulike studier, forteller forskerne Fysikkens verden. Dette inkluderer bruk av mPET for å identifisere kreftresistens mot terapi, evaluere den med andre positron-gamma-emittere, utvide dens evner til å avbilde mer enn to isotoper samtidig, og teste den i klinikken med pasienter i riktig setting.
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk deg selv. Tilgang her.
- PlatoAiStream. Web3 Intelligence. Kunnskap forsterket. Tilgang her.
- PlatoESG. Bil / elbiler, Karbon, CleanTech, Energi, Miljø, Solenergi, Avfallshåndtering. Tilgang her.
- BlockOffsets. Modernisering av eierskap for miljøkompensasjon. Tilgang her.
- kilde: https://physicsworld.com/a/multiplexed-pet-can-image-two-radiotracers-in-a-single-scan/
- : har
- :er
- :ikke
- $OPP
- 10
- a
- evne
- Om oss
- oppnådd
- erverve
- oppkjøp
- oppkjøp
- aktivitet
- tillegg
- Ytterligere
- Tilleggsinformasjon
- administrert
- avansere
- Etter
- agenter
- AL
- alike
- Alle
- også
- alltid
- an
- og
- noen
- Søknad
- søknader
- Påfør
- tilnærming
- ER
- AS
- vurderes
- At
- oppnåelig
- forfatter
- unngås
- BE
- Beauty
- fordi
- mellom
- biomedisinsk
- kroppen
- både
- men
- by
- som heter
- CAN
- Kreft
- Kreftceller
- evner
- bil
- hvilken
- bærere
- saken
- Celler
- klart
- klikk
- klinikk
- Klinisk
- tilfeldighet
- kollegaer
- konkluderer
- ansett
- kostbar
- kunne
- skape
- opprettet
- Gjeldende
- dato
- datasett
- levering
- demonstrere
- avhenger
- dybde
- beskrive
- oppdage
- oppdaget
- utviklet
- utvikle
- gJORDE
- forskjellig
- distinkt
- skille
- distribusjon
- Distribusjoner
- gjort
- dobbelt
- medikament
- to
- under
- dynamisk
- e
- hver enkelt
- effekter
- utslipp
- Utslipp
- understreke
- ansatt
- muliggjør
- energi
- evaluere
- Event
- hendelser
- eksisterende
- fremskynde
- eksperimenter
- forklarer
- utnytte
- Eksponering
- uttrykk
- strekker
- finne
- Først
- Til
- funnet
- fra
- videre
- generere
- gir
- Giving
- HAD
- maskinvare
- Ha
- ledet
- hjelpe
- Hvordan
- Hvordan
- Men
- HTTPS
- ideelt sett
- identifisere
- if
- bilde
- bilder
- Imaging
- umiddelbart
- immunterapi
- implementert
- in
- inkludere
- inkluderer
- Øke
- økt
- øker
- økende
- informasjon
- undersøke
- utstedelse
- IT
- DET ER
- jpg
- begrensning
- linjer
- plassering
- senking
- maskiner
- Vedlike
- mange
- Match
- max bredde
- Kan..
- måle
- medisinsk
- metode
- minimal
- modifikasjoner
- molekyl~~POS=TRUNC
- Overvåke
- mer
- mest
- flyttet
- Natur
- Trenger
- Ny
- neste
- mange
- of
- ofte
- on
- ONE
- bare
- åpen
- or
- Annen
- enn
- oversikt
- par
- par
- pasienter
- ytelse
- Fotoner
- Fysikk
- Fysikkens verden
- plato
- Platon Data Intelligence
- PlatonData
- mulig
- trykk
- tidligere
- produsere
- ordentlig
- forutsatt
- gir
- kvantitativ
- raskt
- mottak
- Krever
- forskning
- forskere
- Motstand
- svar
- Avslørt
- ikke sant
- Rise
- samme
- sier
- skanne
- skanning
- forskere
- Sekund
- sett
- separat
- separering
- innstilling
- Vis
- viste
- vist
- signaler
- signaturer
- lignende
- samtidig
- enkelt
- Sloan
- Software
- noen
- snart
- iscenesettelse
- Standard
- Uttalelse
- Trinn
- studier
- slik
- foreslår
- egnet
- Systemer
- Target
- rettet mot
- mål
- lag
- Teknologi
- fortelle
- testet
- Testing
- enn
- Det
- De
- deres
- deretter
- Der.
- de
- denne
- Gjennom
- thumbnail
- tid
- til
- trekke
- spor
- Sporing
- Triple
- sant
- to
- gjennomgår
- universitet
- upon
- bruke
- brukt
- ved hjelp av
- vanligvis
- Verdifull
- ulike
- av
- var
- Vei..
- var
- når
- hvilken
- mens
- allment
- vil
- vindu
- med
- innenfor
- uten
- virker
- verden
- zephyrnet