Protonterapi kan levere svært konforme dosefordelinger til et tumormål samtidig som dosen til vev utenfor målvolumet minimeres. Å lage behandlingsplaner som realiserer denne styrken er en toppprioritet for dosimetrister og medisinske fysikere.
Protoner avsetter dose på en fundamentalt annen måte enn røntgenstråler, en annen type ekstern strålebehandling. Når et proton når slutten av sin bane, øker hastigheten som energien overføres til vev – dens lineære energioverføring (LET), uttrykt i keV/µm.
Den relative biologiske effektiviteten (RBE) fanger opp de biologiske implikasjonene av å øke LET, og en fast RBE-verdi på 1.1 brukes ofte for kliniske protonbehandlinger. Men proton RBE er avhengig av mange andre faktorer, inkludert kliniske endepunkter, vevstype, fraksjoneringsskjema, pasientspesifikk radiosensitivitet, fysisk dose og usikkerheter i eksperimentelle målinger. Som et resultat vil bruk av en fast RBE-verdi i protonterapi sannsynligvis undervurdere RBE på steder med høyt LET-nivå, noe som kan resultere i økt risiko for strålingsindusert toksisitet.
Likevel er LET sterkt korrelert med RBE og er en nøkkelfaktor for å bestemme variabel RBE i protonterapi. Som sådan undersøker forskere tilnærminger for å beregne og evaluere LET under behandlingsplanlegging. Disse biologiske behandlingsplanleggingsverktøyene er imidlertid begrenset, og inntil de er utviklet og studert videre, må klinikker identifisere sine egne behandlingsplanleggingspraksis for å minimere LET utenfor målvolumene, sier Austin Faught, en medisinsk fysiker ved St Jude Children's Research Hospital i Tennessee.
"Hvordan påvirke [LET-distribusjonen] er et aktivt forskningsområde, og det er noen flotte metoder under utvikling," forklarer Faught. "Problemet vi står overfor er at de ikke er lett tilgjengelige uten tilpasset programvare utviklet internt eller gjennom spesielle forskningsversjoner av leverandørleverte applikasjoner ... [og det er] få studier som gir kvantitativ veiledning om hva vi bør sikte mot."
Behandlingsplanleggingsstrategier
I et skritt mot LET-basert planevaluering og optimalisering for fotonterapi, utførte Faught og teamet hans en undersøkelse av planleggingsstrategier som er kommersielt tilgjengelige for kliniske team for intensitetsmodulert protonterapi (IMPT). Studien deres, rapportert i Journal of Applied Clinical Medical Physics, introduserer noen veiledning for planleggere av protonterapibehandling. "Vi ønsket å se på noen lett tilgjengelige behandlingsplanleggingsteknikker og hvordan de kan påvirke LET," forklarer Faught.
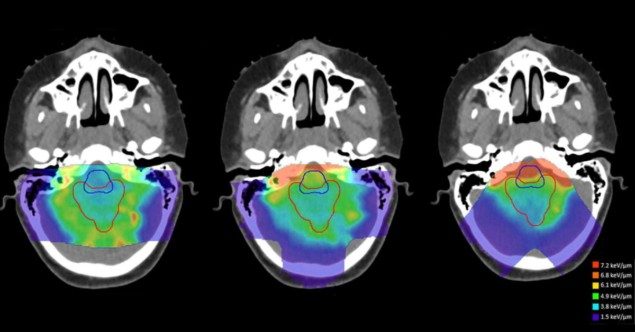
Forskerne evaluerte forskjellene i dosevektet LET (LETd) mellom åtte fremtidsbaserte behandlingsplanleggingstilnærminger brukt på et sylindrisk vannfantom og fire pediatriske hjernesvulsttilfeller (Faught bemerker at strålingsindusert toksisitet er et fokusområde for teamet). De sammenlignet disse planleggingsstrategiene med en plan som bruker motsatte sidestråler (for fantomet) eller med den opprinnelige kliniske planen (for pasienter), ved å bruke Monte Carlo sekundære beregninger for å evaluere både dosen og LETd.
Forskerne fant at behandlingsfeltgeometri var den største bidragsyteren til plasseringen av områder med høy LET. For å dempe den potensielle effekten av biologiske usikkerheter forbundet med høy LETd, foreslår de at behandlingsplanleggere bruker store skjæringsvinkler mellom behandlingsbjelker og unngår bjelker som stopper umiddelbart proksimalt til kritiske strukturer.
"Dette er gode nyheter siden det betyr at nøye utvalg av antall behandlingsfelt og deres orientering med hensyn til nærliggende helsevev kan være effektive," sier Faught. "Med noen bevisste tanker på forhånd, er det noe alle behandlingsplanleggere kan ta i betraktning under planleggingsprosessen."
Forskerne fant også at bruk av en rekkeviddeskifter reduserte gjennomsnittlig LET betydeligd i det kliniske målvolumet. Som et resultat anbefaler de å bruke avstandsskiftere og alternative strategier for punktplasseringsrestriksjoner sparsomt, og bare når klinikker kan beregne den resulterende LETd å evaluere mot alternative planleggingsstrategier.
På grunn av studiens lille utvalgsstørrelse, kunne forskerne ikke etablere en klar trend i LETd variasjoner i de kliniske tilfellene. De evaluerte ikke sammenhengen mellom endringer i LET og en endring i sannsynligheten for tumorkontroll eller normale vevskomplikasjoner.
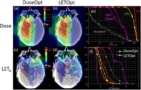
LET-baserte planer optimerer protonterapi
Mens effekten av hver planleggingstilnærming på høy-LET-regioner var beskjedne, sier Faught at det er viktig å erkjenne at teamets behandlingsplanleggingsstrategier og anbefalinger er evidensbasert og lett kan omsettes til klinisk praksis.
«Jeg håper at en av fordelene er at vi som felt vil ha nytte av kommersielle verktøy som gjør det mulig å beregne LET i behandlingsplanleggingssystemet. Enda bedre, vi vil gjerne ha måter å optimalisere med LET i tankene. Denne studien var en god bro inntil disse verktøyene er mer tilgjengelig, sier Faught.