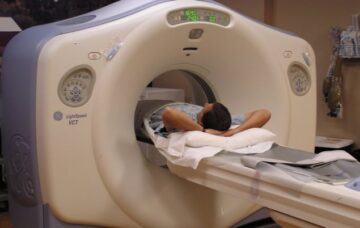
Stereotaktyczna radioterapia ciała (SBRT) to precyzyjna terapia przeciwnowotworowa, która dostarcza mniej frakcji promieniowania o wyższych dawkach niż tradycyjna radioterapia. SBRT może zapewnić doskonałą lokalną kontrolę guza, ale w przypadku niektórych lokalizacji guza grozi narażeniem pobliskich zagrożonych narządów (OAR) na niedopuszczalne poziomy napromieniowania. SBRT oparty na protonach zapewnia lepszą oszczędność OAR, ale nadal wymaga pewnych marginesów leczenia, które mogą ograniczać jego zastosowanie kliniczne.
Radioterapia FLASH, w której promieniowanie jest dostarczane z ultrawysokimi dawkami, może umożliwić dalsze oszczędzanie OAR. Aby zbadać jego potencjał, zespół badawczy skierował się do Emory University opracowuje ramy optymalizacji dostarczania terapii protonowej, aby sprostać wymaganiom radioterapii FLASH.
Większość nowoczesnych systemów terapii protonowej może osiągnąć moc dawki FLASH przy użyciu wysokoenergetycznej wiązki transmisyjnej, która przechodzi przez pacjenta, osadzając dawkę na całej swojej drodze. Takie podejście eliminuje jednak główną zaletę terapii protonowej: jej zdolność do dostarczania dawki w rozłożonym piku Bragga. Aby poprawić zgodność przy dawkach FLASH, Ruirui Liu i współpracownicy proponują, że specyficzne dla pacjenta filtry grzbietowe mogą zapewnić podobny rozkład dawki jak w przypadku konwencjonalnej terapii protonowej o modulowanej intensywności (IMPT).
W przypadku terapii FLASH dawka, uśredniona moc dawki (DADR) i liniowy transfer energii uśredniony w dawce (LETd) wszystkie wpływają na odpowiedź biologiczną. Dlatego naukowcy opracowali zintegrowane ramy optymalizacji fizycznej (IPO), które jednocześnie optymalizują te trzy parametry, aby zmaksymalizować oszczędzanie OAR w planie leczenia pacjenta. Ramy, opisane w International Journal of Radiation Oncology, Biology, Physics, wykorzystuje funkcję celu IPO-IMPT, aby zapewnić wiele rozwiązań do projektowania filtrów grzbietowych specyficznych dla pacjenta i map plamek protonowych.
Filtry grzbietowe, które są używane w połączeniu z kompensatorem zasięgu, składają się z szeregu szpilek w kształcie zigguratu, które rozkładają pik Bragga z wiązki 250 MeV, aby pokryć docelową objętość planowania specyficzną dla wiązki. Zespół opracował oprogramowanie do planowania odwrotnego w celu zdefiniowania lokalizacji pinów dla filtra specyficznego dla pacjenta i wykorzystał symulacje Monte Carlo oparte na Geant4, aby uzyskać macierze wpływu dawki i LET.

Plany pacjenta
Aby zademonstrować ramy IPO-IMPT, naukowcy opracowali plany leczenia trzech pacjentów z rakiem płuc. Zalecili dawkę 50 Gy (pięć frakcji po 10 Gy) do docelowej objętości klinicznej, z maksymalną dawką hotspot 62.5 Gy. W zależności od tego, który parametr jest traktowany priorytetowo, plany mają na celu zwiększenie zasięgu FLASH i/lub zmniejszenie LETd, przy zachowaniu dawki docelowej.
Dla pacjenta 1, który miał centralny guz płuc blisko serca, OAR były sercem i płucami. W tym przypadku naukowcy stworzyli jednowiązkowy plan IPO-IMPT w celu zmniejszenia LETd do serca przy zachowaniu zasięgu docelowego. Plan IPO-IMPT spełnił ten cel, wykazując podobne pokrycie docelowe jak konwencjonalny plan IMPT, ale znacznie zmniejszając LETd do serca.
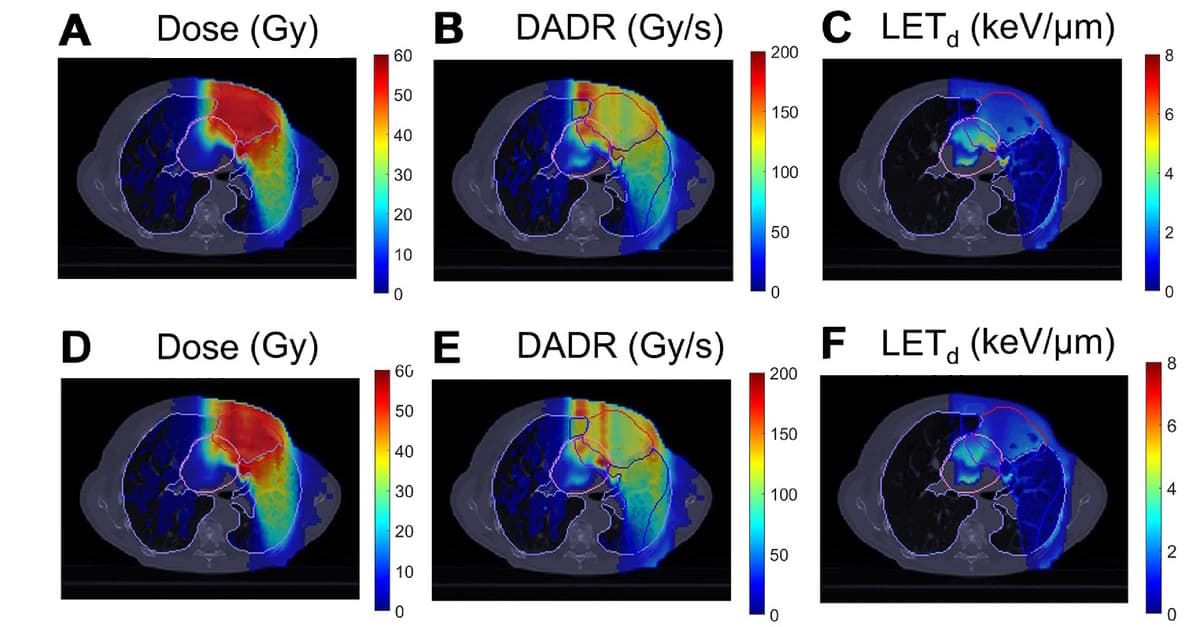
Pacjent 2 miał guza z przerzutami w prawym dolnym płacie, a pacjent 3 miał guz w podkarinalnym węźle chłonnym. W tych przypadkach przełyk był również wiosłem, a kluczowym celem było oszczędzanie przełyku. Zarówno dla IPO-IMPT, jak i IMPT, prawie 100% ocenianej objętości przełyku osiągnęło próg FLASH 40 Gy/s. Dla pacjenta 2, IPO-IMPT nieznacznie zmniejszył LETd dla serca i przełyku oraz zwiększone pokrycie FLASH dla serca.
Rzadka konstrukcja pinów
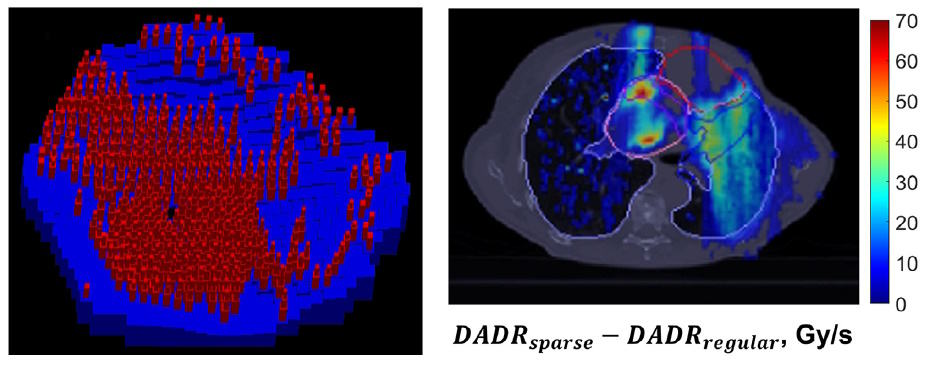
Zwykłe filtry grzbietowe zaprojektowane przy użyciu struktury IPO-IMPT selektywnie oszczędzały OAR, zmniejszając LET i zwiększając zasięg FLASH. Jednak rzadkie filtry grzbietowe, w których pominięto niektóre szpilki, oferują potencjał do dalszego zwiększenia oszczędności OAR. Usunięcie szpilek filtra w określonych miejscach zapewnia wyższy strumień protonów, podczas gdy pozostałe szpilki nadal zapewniają odpowiednie pokrycie celu.
W przypadku pacjenta 1 naukowcy wygenerowali plan IPO-IMPT z rzadkimi filtrami grzbietowymi i wieloma wiązkami. Porównanie z planem IMPT przy użyciu zwykłych filtrów grzbietowych wykazało, że w obu przypadkach zachowano pokrycie guza, a punkty zapalne były dobrze kontrolowane. Rzadkie filtry grzbietowe zwiększyły jednak objętość OAR otrzymując moc dawki FLASH o 31% i 50%, odpowiednio dla objętości oceny serca i płuc.
Rzadkie filtry grzbietowe zapewniają elastyczność umożliwiającą wykorzystanie pełnego potencjału struktury IPO-IMPT. Na przykład poziomy usuwania szpilek można dostosować do indywidualnych przypadków pacjentów. Próg usuwania 50% szpilek zapewnił rozsądne wyniki w przypadku dużego guza pacjenta 1, podczas gdy próg 30% był dobrym punktem wyjścia dla mniejszych celów pacjentów 2 i 3, u których plany oparte na rzadkich filtrach grzbietowych zwiększyły DADR w przełyku przy jednoczesnym utrzymaniu guza zasięg.
Wreszcie, aby sprawdzić, czy zespół filtra grzbietowego (szpilki filtra i kompensator) może dostarczyć przewidywaną dawkę, naukowcy wydrukowali w 3D filtr grzbietowy dostosowany do pacjenta. Dostarczyli plan leczenia mający na celu zapewnienie jednolitej dawki docelowej i wykonali pomiary dawki za pomocą zestawu komór jonizacyjnych. Całkowity współczynnik przenikania promieni gamma wyniósł 92.9% dla dawek bezwzględnych, co przekracza standardowe kryteria przepuszczania przez pacjenta wynoszące 90% i pokazuje, że zestaw może zapewnić klinicznie akceptowalny rozkład dawki.

NPL wprowadza dozymetrię bezwzględną dla wiązek protonów FLASH
„To badanie potwierdzające słuszność koncepcji pokazuje wykonalność zastosowania struktury IPO-IMPT do realizacji stereotaktycznej terapii protonowej ciała FLASH, z uwzględnieniem dawki, DADR i LETd jednocześnie” – podsumowują naukowcy. „Ta nowatorska metoda ułatwi dostarczanie konforemnych pól protonowych z szybkością FLASH do badań przedklinicznych i klinicznych”.
Starszy autor Liyong Lin mówi Świat Fizyki że zespół ma nadzieję dalej rozwijać swoje oprogramowanie do takich zastosowań. „Biuro Transferu Technologii firmy Emory zachęciło nas do założenia nowej firmy Radiotherapy Biological Optimization (RBO) Solutions” — wyjaśnia Lin. „RBO zostało zaakceptowane przez program pomocy wnioskodawcom National Institutes of Health w celu przedłożenia grantu R41 na transfer technologii dla małych firm do National Cancer Institute do 5 kwietnia. IBA, największy dostawca terapii cząsteczkowej, oraz dział dozymetrii IBA poprą wniosek RBO o grant R41. ”
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- Platoblockchain. Web3 Inteligencja Metaverse. Wzmocniona wiedza. Dostęp tutaj.
- Źródło: https://physicsworld.com/a/patient-specific-ridge-filters-enable-conformal-flash-proton-therapy/
- :Jest
- $W GÓRĘ
- 1
- 10
- 2023
- 3d
- a
- zdolność
- bezwzględny
- do przyjęcia
- wykonać
- Księgowość
- Osiągać
- Korzyść
- Wszystkie kategorie
- i
- aplikacje
- podejście
- kwiecień
- SĄ
- Szyk
- Montaż
- Wsparcie
- At
- autor
- BE
- Belka
- Ulepsz Swój
- pomiędzy
- Najwyższa
- biologia
- ciało
- biznes
- by
- CAN
- Rak
- Leczenie raka
- walizka
- Etui
- centralny
- Izba
- Charles
- Dzieci
- kliknij
- Kliniczne
- Zamknij
- koledzy
- połączenie
- sukcesy firma
- porównanie
- stwierdza,
- kontrola
- kontrolowanych
- Konwencjonalny
- mógłby
- pokrywa
- pokrycie
- Kryteria
- dostarczyć
- dostarczona
- dostarcza
- dostawa
- wymagania
- wykazać
- demonstruje
- W zależności
- opisane
- Wnętrze
- zaprojektowany
- rozwijać
- rozwinięty
- rozwijanie
- różnica
- 分配
- Dystrybucje
- podział
- eliminuje
- umożliwiać
- zachęcać
- popierać
- energia
- ewaluację
- przykład
- przekracza
- doskonała
- wykazujące
- Objaśnia
- ułatwiać
- Łąka
- filtrować
- filtry
- Migać
- Elastyczność
- STRUMIEŃ
- W razie zamówieenia projektu
- Nasz formularz
- Framework
- od
- pełny
- funkcjonować
- dalej
- wygenerowane
- cel
- dobry
- przyznać
- głowiasty
- Serce
- wyższy
- przytrzymanie
- ma nadzieję,
- hotspot
- Jednak
- HTML
- HTTPS
- obraz
- podnieść
- PODATEK
- in
- Zwiększać
- wzrosła
- wzrastający
- indywidualny
- wpływ
- Informacja
- Instytut
- zintegrowany
- Przedstawia
- badać
- IPO
- problem
- IT
- JEGO
- dziennik
- jpg
- Klawisz
- duży
- poziomy
- LIMIT
- miejscowy
- lokalizacji
- Utrzymywanie
- poważny
- Mapy
- marginesy
- Maksymalna szerokość
- Maksymalizuj
- maksymalny
- Pomiary
- Poznaj nasz
- metoda
- Nowoczesne technologie
- wielokrotność
- narodowy
- węzeł
- powieść
- cel
- of
- oferta
- Biurowe
- on
- koncepcja
- optymalizacja
- Optymalizuje
- optymalizacji
- parametr
- parametry
- Terapia cząsteczkowa
- przebiegi
- Przechodzący
- ścieżka
- pacjent
- pacjenci
- Szczyt
- fizyczny
- kołki
- krok po kroku
- planowanie
- plany
- plato
- Analiza danych Platona
- PlatoDane
- punkt
- potencjał
- Detaliczność
- Przewiduje
- priorytetowe
- Program
- wniosek
- zaproponować
- protony
- zapewniać
- pod warunkiem,
- zapewnia
- Radioterapia
- zasięg
- Kurs
- ceny
- zrealizować
- rozsądny
- odbieranie
- zmniejszyć
- redukcja
- regularny
- pozostały
- usuwanie
- usuwanie
- Wymaga
- Badania naukowe
- Badacze
- odpowiedź
- Efekt
- ryzyko
- s
- podobny
- jednocześnie
- mały
- small business
- mniejszy
- Tworzenie
- Rozwiązania
- kilka
- specyficzny
- Spot
- rozpiętość
- standard
- Startowy
- startup
- Nadal
- badania naukowe
- Badanie
- Zatwierdź
- taki
- systemy
- dostosowane
- cel
- cele
- zespół
- Technologia
- mówi
- że
- Połączenia
- Te
- trzy
- próg
- Przez
- poprzez
- miniatur
- do
- Kwota produktów:
- tradycyjny
- przenieść
- leczenie
- prawdziwy
- us
- sprzedawca
- zweryfikować
- Tom
- kłęby
- DOBRZE
- który
- Podczas
- KIM
- będzie
- w
- zefirnet