Radioterapia jest jedną z najpowszechniejszych metod leczenia nowotworów, skutecznie wydłużającą czas przeżycia i zwiększającą odsetek wyleczeń pacjentów chorych na raka. Jednakże uszkodzenia kości wywołane radioterapią – w tym zmniejszenie masy kostnej, zwiększona łamliwość kości oraz większe ryzyko złamań i martwicy kości – pozostają częstym problemem, na który obecnie brakuje skutecznych środków zaradczych.
Promieniowanie powoduje te uszkodzenia poprzez hamowanie wzrostu, przeżycia i dojrzewania komórek tworzących kości zwanych osteoblastami, hamując w ten sposób tworzenie kości. Potencjalnym lekarstwem może być ekspozycja na nieinwazyjne pola elektromagnetyczne (EMF), o których wiadomo, że stymulują wzrost i różnicowanie osteoblastów oraz mogą łagodzić skutki napromieniania. Teraz zespół badawczy w Chinach zidentyfikował optymalny kształt fali EMF, aby zmaksymalizować skuteczność takiego leczenia, opisując swoje ustalenia w Postępy nauki.
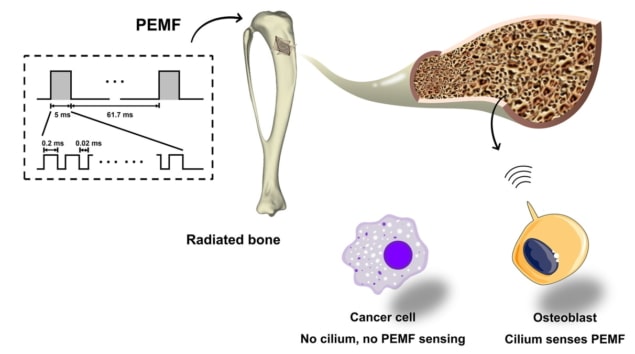
Da Jing, z Czwarta Wojskowa Akademia Medycznai współpracownicy najpierw poddali komórki kostne stymulacji polem elektromagnetycznym przy użyciu różnych kształtów fal, w tym pola elektromagnetycznego sinusoidalnego, pola elektromagnetycznego o pojedynczym impulsie i pola elektromagnetycznego o impulsowym impulsie (PEMF). Aby ocenić odpowiedź komórek, monitorowano w czasie rzeczywistym wewnątrzkomórkowe jony wapnia (Ca2+) sygnalizacja, jedna z najwcześniejszych odpowiedzi komórkowych na bodźce zewnętrzne.
Zespół odkrył, że PEMF indukuje silniejszy wewnątrzkomórkowy Ca2+ sygnalizacja w napromieniowanych osteoblastach niż inne przebiegi, charakteryzujące się unikalnym Ca2+ oscylacje z wieloma Ca2+ kolce. Dalsze analizy wykazały, że niezidentyfikowany wcześniej kształt fali PEMF o natężeniu pola magnetycznego 2 mT i częstotliwości 15 Hz wywołał najsilniejszą odpowiedź w osteoblastach. Natomiast ten kształt fali PEMF nie miał wpływu na inne typy napromienianych komórek kostnych (osteoklasty i osteocyty).
Następnie naukowcy sprawdzili, czy PEMF podawany przy użyciu tych optymalnych parametrów może złagodzić utratę kości wywołaną promieniowaniem in vivo. W badaniach na szczurach poddano jedną kończynę tylną działaniu dwóch dawek promieniowania ogniskowego po 8 Gy (w odstępie jednego dnia), a 45 dni później wykorzystano mikro-CT do oceny struktury kości. Napromieniowane kończyny wykazywały znaczną utratę kości beleczkowej, w tym około 50% zmniejszenie frakcji objętościowej kości i gęstości mineralnej kości w porównaniu ze stroną nienapromienianą.
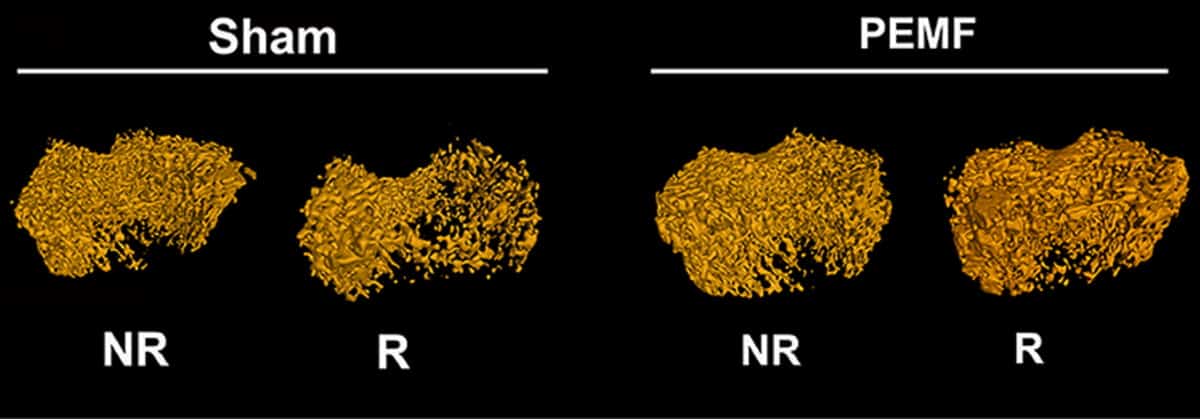
Druga grupa szczurów codziennie otrzymywała PEMF na całe ciało (2 godziny dziennie) przez 45 dni po napromienianiu. Zabieg ten przywrócił masę kostną i właściwości mechaniczne napromienianych kończyn tylnych do poziomu kończyn nienapromienianych, ratując osteoblasty. Zespół zauważa, że PEMF nie miał wpływu na masę ciała zwierząt ani spożycie pokarmu.
Po wykazaniu, że ekspozycja na PEMF może złagodzić utratę masy kostnej wywołaną promieniowaniem, istotne jest również, aby PEMF nie wpływał niekorzystnie na leczenie nowotworu. Mając to na uwadze, naukowcy porównali wrażliwość osteoblastów i różnych komórek nowotworowych (raka piersi, raka okrężnicy, czerniaka złośliwego i komórek kostniakomięsaka) na PEMF.
Napromienianie zmniejszało żywotność komórek i sprzyjało apoptozie we wszystkich typach komórek. Co najważniejsze, chociaż PEMF poprawiał żywotność osteoblastów i hamował apoptozę osteoblastów, nie miał wpływu na żywotność ani apoptozę żadnej komórki nowotworowej w żadnym punkcie czasowym.
Żywy biotusz może usprawnić naprawę i regenerację kości
Naukowcy przypisują tę selektywność obecności rzęsek pierwotnych – organelli czuciowych, które wykrywają i tłumaczą zewnątrzkomórkowe sygnały mechaniczne – które działają jak czujniki PEMF. Te pierwotne rzęski są bardzo liczne w osteoblastach, ale nie występują w większości komórek nowotworowych. W eksperymencie, w którym zablokowano wytwarzanie rzęsek pierwotnych w napromieniowanych osteoblastach, wzrost przeżycia i różnicowania osteoblastów za pośrednictwem PEMF prawie całkowicie zniknął.
„Biorąc pod uwagę, że spośród wszystkich typów komórek kostnych osteoblasty są szczególnie wrażliwe na promieniowanie, ten schemat PEMF, który indukuje specyficzną aktywację osteoblastów, wydaje się obiecującą i wysoce skuteczną metodą zapobiegania uszkodzeniom kości wywołanym promieniowaniem” – podsumowują naukowcy.