Możliwość połączenia elektroniki i czujników optycznych z ludzkim ciałem na poziomie pojedynczych komórek może pewnego dnia umożliwić zdalne monitorowanie i kontrolę poszczególnych komórek w czasie rzeczywistym. Postępy w produkcji elektroniki umożliwiły tworzenie tranzystorów i czujników o rozdzielczości nanoskali, a innowacyjne techniki nanowzorowania umożliwiają montaż tych urządzeń na elastycznych podłożach. Jednakże takie procesy zazwyczaj wymagają stosowania agresywnych środków chemicznych, wysokich temperatur lub technik próżniowych, które są nieodpowiednie dla żywych komórek i tkanek.
Aby pokonać te przeszkody, zespół badawczy na Uniwersytecie Johnsa Hopkinsa opracował nietoksyczny, opłacalny i charakteryzujący się wysoką rozdzielczością proces drukowania nanowzorów złota na żywych tkankach i komórkach. Zgłaszanie swoich ustaleń w nano Letterswykazują, że nowa technika może „tatuować” żywe komórki i tkanki elastycznymi układami złotych nanokropek i nanodrutów. Docelowo tę metodę można zastosować do integracji inteligentnych urządzeń z żywą tkanką do zastosowań takich jak bionika i biosensoria.
„Gdybyśmy mieli technologie umożliwiające śledzenie stanu izolowanych komórek, być może moglibyśmy diagnozować i leczyć choroby znacznie wcześniej, a nie czekać, aż cały narząd ulegnie uszkodzeniu” – wyjaśnia kierownik zespołu Dawid Gracias w oświadczeniu prasowym. „Mówimy o umieszczeniu czegoś w rodzaju elektronicznego tatuażu na żywym obiekcie dziesiątki razy mniejszym od główki szpilki. To pierwszy krok w kierunku mocowania czujników i elektroniki do żywych komórek.”
Dziękuję Luo Gu i współpracownicy opracowali trzyetapowy proces drukowania nanotransferowego w celu łączenia nanowzorów złota z żywymi komórkami. W pierwszym etapie wykorzystali konwencjonalną litografię nanoimprintową (NIL) do nadrukowania układów złotych nanokropek lub nanodrutów na waflach krzemowych pokrytych polimerem. Następnie rozpuścili polimer, uwalniając nanomacierze do przeniesienia na szklane szkiełka nakrywkowe.
Następnie badacze funkcjonalizowali powierzchnię złota cysteaminą i pokryli złote macierze NIL alginianową hydrożelową warstwą transferową. Wykazali, że dzięki temu podejściu można w niezawodny sposób przenieść układy nanokropek i nanodrutów o wymiarach 8 × 8 mm ze szkła na miękkie i elastyczne hydrożele. W ostatnim etapie złote macierze NIL są sprzęgane z żelatyną, aby umożliwić ich przeniesienie na żywe komórki lub tkankę. Oddzielenie hydrożelowej warstwy transferowej powoduje odsłonięcie złotego wzoru.
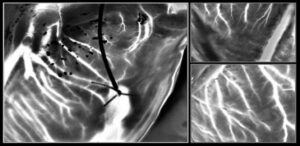
Naukowcy zbadali zachowanie żywych komórek fibroblastów wysianych na układach złotych kropek o średnicy 250 nm (odstęp między środkami 550 nm) lub złotych drutach o szerokości 300 nm (odstęp 450 nm) na hydrożelach alginianowych. Około 24 godziny po zaszczepieniu komórki na hydrożelu nadrukowanym nanodrutem korzystnie migrowały równolegle do nanodrutów, podczas gdy komórki na nanokropkach wykazywały przypadkową, ale nieco szybszą migrację. Komórki na nanodrutach również wykazywały mniej więcej dwukrotnie większe wydłużenie niż komórki na nanokropkach. Odkrycia te pokazują zdolność złotych tablic NIL do kierowania orientacją i migracją komórek.
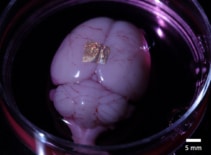
Oprócz tego, że jest biokompatybilny z komórkami i tkankami, hydrożel alginianowy może również przenosić złote macierze NIL na żywe narządy i komórki. Aby to zademonstrować, naukowcy umieścili wydrukowane nanodrutem hydrożele na korze mózgowej całego mózgu i koronowym wycinku mózgu.
Po 2 godzinach w pożywce hodowlanej i dysocjacji hydrożelu nanodruty pozostały związane z powierzchnią całego mózgu. Natomiast nanodruty w wycinku mózgu nie przylegały, co sugeruje, że siła adhezji różni się w zależności od rodzaju komórek i metod hodowli. Naukowcy zauważają, że potrzebne są dalsze badania, aby scharakteryzować i zoptymalizować mechanizmy adhezji w celu uzyskania solidnego, długotrwałego wiązania.
Na koniec, aby ocenić druk biotransferowy na poziomie pojedynczych komórek, badacze hodowali jednowarstwowe arkusze komórkowe na hydrożelach alginianowych ze złotym nadrukiem NIL. Po 24 godzinach przeniesiono hydrożele zaszczepione fibroblastami na szkiełka nakrywkowe pokryte żelatyną i umożliwiono komórkom przyczepienie się do szkiełek nakrywkowych przez noc.
Po zdysocjowaniu hydrożelu alginianowego mikroskopia fluorescencyjna wykazała, że fibroblasty ozdobione nanokropkami złota miały żywotność około 97%, podczas gdy te ozdobione nanodrutami miały żywotność około 98%, co wskazuje, że proces drukowania jest biokompatybilny z żywymi komórkami. Odblaskowe kolory widoczne na wzorzystym arkuszu komórek fibroblastów sugerują, że kształt złotej macierzy NIL został zachowany.
Proces wytwarzania jest również zgodny z fotolitografią w mikroskali, co umożliwiło naukowcom stworzenie sześciokątnych i trójkątnych plam o szerokości 200 µm ze złotych układów NIL. Następnie metodą biotransferu wydrukowali je na arkuszach komórek, co doprowadziło do selektywnego wzrostu komórek fibroblastów na mikropłatkach. Filmy nagrane przez 16 godzin pokazały, że komórki z nadrukowanymi na wierzchu plamami nanodrutów wydają się zdrowe i zdolne do migracji, a układy pozostają na miękkich komórkach nawet podczas ruchu.

Mały czujnik jednocześnie mierzy aktywność elektryczną i mechaniczną komórek serca
„Wykazaliśmy, że możemy przyczepiać złożone nanowzorce do żywych komórek, zapewniając jednocześnie, że komórka nie umrze” – mówi Gracias. „To bardzo ważny wynik, że komórki mogą żyć i poruszać się wraz z tatuażami, ponieważ często występuje znaczna niezgodność między żywymi komórkami a metodami stosowanymi przez inżynierów do wytwarzania elektroniki”.
Gracias i współpracownicy doszli do wniosku, że ich proces nanowzorowania w połączeniu ze standardowymi technikami mikrofabrykacji „otwiera możliwości opracowania nowych substratów do hodowli komórkowych, materiałów biohybrydowych, urządzeń bionicznych i bioczujników”. Następnie planują spróbować dołączyć bardziej złożone nanoobwody, które mogą pozostać na miejscu przez dłuższy czas, a także eksperymentować z różnymi typami komórek.
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- PlatoData.Network Pionowe generatywne AI. Wzmocnij się. Dostęp tutaj.
- PlatoAiStream. Inteligencja Web3. Wiedza wzmocniona. Dostęp tutaj.
- PlatonESG. Motoryzacja / pojazdy elektryczne, Węgiel Czysta technologia, Energia, Środowisko, Słoneczny, Gospodarowanie odpadami. Dostęp tutaj.
- Platon Zdrowie. Inteligencja w zakresie biotechnologii i badań klinicznych. Dostęp tutaj.
- ChartPrime. Podnieś poziom swojej gry handlowej dzięki ChartPrime. Dostęp tutaj.
- Przesunięcia bloków. Modernizacja własności offsetu środowiskowego. Dostęp tutaj.
- Źródło: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- :ma
- :Jest
- :nie
- $W GÓRĘ
- 16
- 200
- 24
- 8
- a
- zdolność
- Zdolny
- O nas
- działalność
- przylegać
- zaliczki
- Po
- również
- wśród
- an
- i
- pojawił się
- aplikacje
- podejście
- w przybliżeniu
- SĄ
- na około
- Szyk
- AS
- Montaż
- oszacować
- At
- dołączać
- BE
- bo
- jest
- pomiędzy
- ciało
- obligacja
- Mózg
- ale
- CAN
- Komórki
- charakteryzować
- kliknij
- koledzy
- połączony
- zgodny
- kompleks
- stwierdza,
- kontrast
- kontrola
- Konwencjonalny
- opłacalne
- mógłby
- Stwórz
- kultura
- dzień
- wykazać
- zaprojektowany
- rozwinięty
- oprogramowania
- urządzenia
- ZROBIŁ
- Umierać
- różne
- choroby
- Nie
- Wcześniej
- Elektroniczny
- Elektronika
- umożliwiać
- włączony
- Inżynierowie
- zapewnienie
- Cały
- Parzyste
- Objaśnia
- szybciej
- finał
- Ustalenia
- i terminów, a
- elastyczne
- W razie zamówieenia projektu
- od
- dalej
- GAO
- ogólnie
- szkło
- Złoto
- Wzrost
- poprowadzi
- miał
- Have
- głowa
- Zdrowie
- zdrowy
- Serce
- Wysoki
- wysoka rozdzielczość
- Hopkins
- Jednak
- HTTPS
- człowiek
- obraz
- ważny
- in
- indywidualny
- Informacja
- Innowacyjny
- integrować
- odosobniony
- problem
- IT
- kalesony
- Johns Hopkins University
- jpg
- warstwa
- lider
- prowadzący
- niech
- poziom
- lubić
- relacja na żywo
- życie
- długoterminowy
- dłużej
- zrobiony
- materiały
- Maksymalna szerokość
- może
- środków
- mechaniczny
- Mechanizmy
- Media
- Łączyć
- metoda
- metody
- Mikroskopia
- migrować
- migrował
- migracja
- monitorowanie
- jeszcze
- ruch
- przeniósł
- Kino
- dużo
- potrzebne
- Nowości
- Następny
- przedmiot
- Przeszkody
- of
- często
- on
- ONE
- na
- koncepcja
- Szanse
- Optymalizacja
- or
- koniec
- Przezwyciężać
- w ciągu nocy
- Parallel
- Łatki
- Wzór
- okresy
- Fizyka
- Świat Fizyki
- Miejsce
- krok po kroku
- plato
- Analiza danych Platona
- PlatoDane
- ustawione
- możliwy
- naciśnij
- druk
- wygląda tak
- procesów
- Putting
- przypadkowy
- SZCZUR
- real
- w czasie rzeczywistym
- nagrany
- pozostał
- pozostały
- zdalny
- Raportowanie
- wymagać
- Badania naukowe
- Badacze
- Rozkład
- dalsze
- Ujawnił
- krzepki
- w przybliżeniu
- mówią
- widziany
- selektywny
- czujniki
- Shape
- arkusz
- pokazał
- pokazane
- znaczący
- Krzem
- jednocześnie
- Plaster
- mniejszy
- mądry
- Miękki
- coś
- standard
- Zestawienie sprzedaży
- pobyt
- Ewolucja krok po kroku
- jest determinacja.
- badania naukowe
- taki
- sugerować
- Powierzchnia
- rozmawiać
- zespół
- Techniki
- Technologies
- kilkadziesiąt
- niż
- że
- Połączenia
- ich
- następnie
- Te
- one
- to
- tych
- miniatur
- czas
- czasy
- do
- Top
- w kierunku
- śledzić
- przenieść
- leczyć
- prawdziwy
- próbować
- Dwa razy
- typy
- Ostatecznie
- uniwersytet
- aż do
- posługiwać się
- używany
- Odkurzać
- początku.
- zdolność do życia
- czekać
- była
- we
- DOBRZE
- natomiast
- który
- Podczas
- cały
- szeroki
- w
- świat
- zefirnet