Zablokowane naczynia krwionośne spowodowane chorobą sercowo-naczyniową mogą prowadzić do poważnych konsekwencji, w tym zawału serca lub udaru mózgu. Stan ten można leczyć przez chirurgiczne ominięcie blokady za pomocą naczynia z innego miejsca w ciele pacjenta. Gdy nie jest to wykonalne, na ogół stosuje się syntetyczny przeszczep naczyniowy. Syntetyczne przeszczepy mają jednak wysoki wskaźnik niepowodzeń z powodu przewlekłego stanu zapalnego spowodowanego odrzucaniem przez organizm obcej substancji. Inną opcją są przeszczepy naczyniowe wytwarzane metodą inżynierii tkankowej (TEVG), które są obiecujące in vivo wyników, ale ich stworzenie wymaga długotrwałych, złożonych i kosztownych procesów.
Teraz naukowcy z Laboratorium INSERM do bioinżynierii tkanek (BioTis U1026) na Uniwersytecie w Bordeaux z powodzeniem wyprodukowali TEVG o małej średnicy przy użyciu nici ludzkiej błony owodniowej (HAM) w połączeniu ze strategią tkania inspirowaną tekstyliami. Opis procesu w Biofabrykacja, twierdzą, że te przeszczepy mają niezwykłe właściwości, które uzasadniają przeprowadzkę in vivo laboratoryjne testy na zwierzętach.
HAM, najbardziej wewnętrzna warstwa błon otaczających płód podczas rozwoju, zapewnia żywotne biologiczne „rusztowanie” dla inżynierii tkankowej. Wykazuje właściwości przeciwzapalne, działanie przeciwdrobnoustrojowe, niską immunogenność (zdolność do wywoływania odpowiedzi immunologicznej), zgodność z krwią, zdolność trzymania szwów i wysoką wytrzymałość mechaniczną. Jest również rutynowo wyrzucany przez szpitale, w związku z czym jest powszechnie dostępny i niedrogi.
Produkcja przędzy
Główny śledczy Nicolasa L'Heureux i współpracownicy stworzyli przędzę HAM z błon płodowych pobranych od wyrażających zgodę pacjentek po cesarskim cięciu. Przygotowywali membrany do użycia przez wielokrotne płukanie tkanek w wodzie destylowanej, cięcie membran na prostokątne arkusze o wymiarach 10 x 18 cm i ręczne oddzielanie owodni i kosmówki (błony wewnętrzne i zewnętrzne). Następnie zmotoryzowane urządzenie tnące pocięło arkusze HAM na wstążki o szerokości 5 lub 10 mm.
Aby stworzyć mechanicznie mocne nici, naukowcy przymocowali te wstążki do obracającego się urządzenia, które skręcało je z prędkością 5, 7.5 lub 10 obrotów na cm. Średnica przędzy zmniejszyła się po skręceniu, osiągając plateau przy 7.5 obrotach/cm, podczas gdy ostateczne naprężenie rozciągające znacznie wzrosło po skręceniu przy 7.5 i 10 obrotach/cm.
Przędze HAM (wstążki i nici) suszono w temperaturze pokojowej, nawijano na szpule i przechowywano w temperaturze -80°C w procesie znanym jako dewitalizacja, ponieważ zabija komórki. W razie potrzeby naukowcy ponownie uwodnili przędzę w wodzie destylowanej.
Ponieważ ich celem było dostarczenie gotowego implantu, naukowcy zbadali wpływ decelularyzacji i sterylizacji promieniowaniem gamma na wstęgi HAM. Histologia wykazała, że decelularyzacja skutecznie usuwała składniki komórkowe, które pozostały po dewitalizacji, nie wpływała na wytrzymałość HAM i zwiększała jej rozciągliwość.
Kiedy suche wstążki HAM były sterylizowane promieniowaniem gamma, stawały się cieńsze, sztywniejsze i mniej rozciągliwe. Utrzymywanie nawodnienia wstążek HAM podczas sterylizacji zapobiegło wielu z tych efektów. Naukowcy zaobserwowali, że sterylizacja na mokro nie wpłynęła na zdolność HAM do wspomagania przylegania i wzrostu komórek śródbłonka.
Tkanie naczyń
Na ostatnim etapie naukowcy złożyli przędze HAM w TEVG. Użyli wykonanego na zamówienie okrągłego krosna do utkania TVEG wokół trzpienia ze stali nierdzewnej. Aby stworzyć tkaną rurkę, obwodowa przędza („wątek”) została umieszczona pomiędzy ruchomym i nieruchomym zestawem naprężonych podłużnych wstążek („osnowa”). Dwa zestawy osnowy przesunięto tak, aby krzyżowały się z wątkiem, ponownie przeciągnięto między nimi przędzę obwodową i proces powtórzono 50 razy.
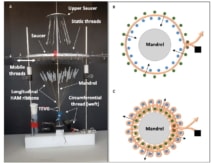
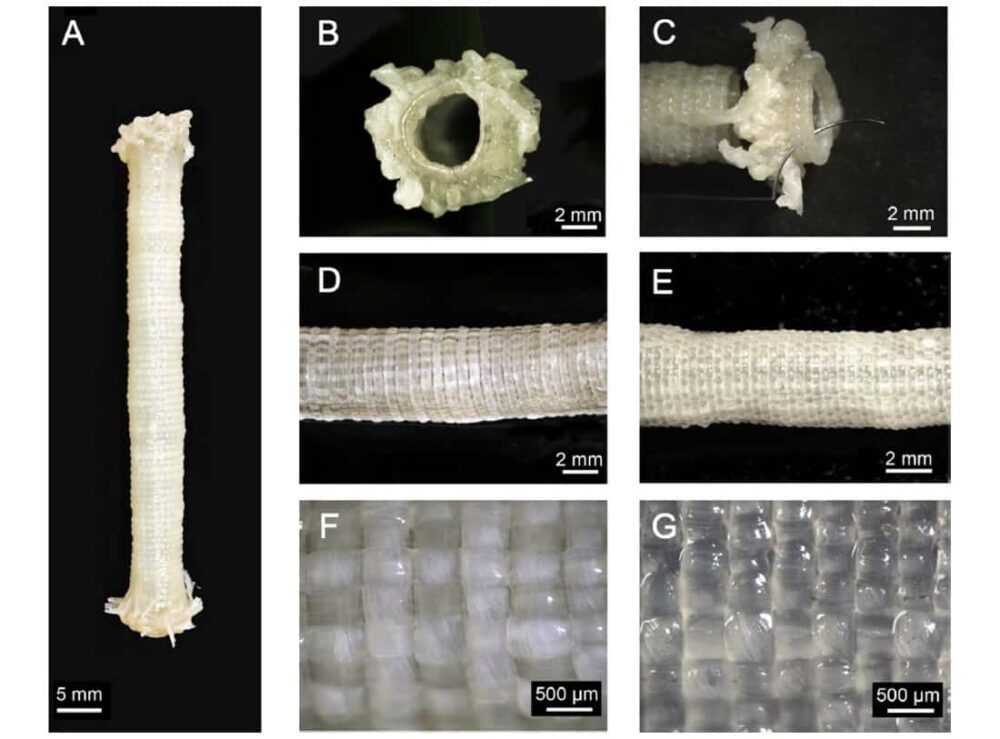
Zespół użył 51 podłużnych wstążek (o szerokości 5 mm) i jednej podwójnej obwodowej nici do utkania TVEG o średniej średnicy wewnętrznej 4.4 ± 0.2 mm. Tkane TEVG były wytrzymałe mechanicznie, z lepszą wytrzymałością utrzymywania szwów i średnim ciśnieniem rozrywającym niż tętnice piersiowe człowieka, preferowane naczynie do operacji pomostowania serca.
Ponieważ jednak przepuszczalność przezścienna była potencjalnie zbyt wysoka, zespół wyprodukował drugi zestaw TVEG, używając podłużnych taśm o szerokości 10 mm i tego samego gwintu obwodowego. W ten sposób powstały TEVG o większej średnicy wewnętrznej 5.2 ± 0.4 mm. Ściany wykazywały zwiększoną gęstość przędzy i drastycznie zmniejszoną przepuszczalność przezścienną. Ciśnienie rozrywające wzrosło, a siła utrzymywania szwu pozostała taka sama.
„Połączenie niedrogiego HAM z metodą tkania zmniejsza koszty produkcji TEVG, unikając stosowania komórek i bioreaktorów, które są niezbędne w innych metodach” – piszą autorzy. „Żadna obecnie stosowana metoda montażu nie pozwala na niedrogą produkcję TVEG na bazie HAM o sprawdzonych właściwościach mechanicznych kompatybilnych z implantacją tętniczą”.

W kierunku in vitro wytwarzanie naczyń krwionośnych
Naukowcy zwracają uwagę, że inspirowane tekstyliami strategie montażu z wykorzystaniem tkania, dziania i splatania są już szeroko stosowane w produkcji urządzeń medycznych. Dlatego nie powinno być trudno zaprojektować maszyny do obsługi przędzy HAM i umożliwić masową produkcję TVEG po przeprowadzeniu udanych badań klinicznych. Dodają, że średnicę przędzy, wytrzymałość mechaniczną i inne właściwości mechaniczne można łatwo modyfikować, aby spełnić różne wymagania specyfikacji.
Następnie naukowcy planują ocenić wpływ decelularyzacji i sterylizacji promieniami gamma po złożeniu na różne właściwości tkanego TVEG, szczególnie w odniesieniu do przepuszczalności i rozciągliwości.