A mielina é uma camada protetora que se forma ao redor dos nervos para isolá-los e acelerar a transmissão de impulsos elétricos. A desmielinização, perda desta camada isolante, contribui para muitas doenças neurológicas, incluindo esclerose múltipla, doença de Alzheimer, acidente vascular cerebral e demência. Uma técnica eficaz para detectar esta condição potencialmente reversível poderia melhorar o diagnóstico de doenças cerebrais e permitir o monitoramento de possíveis tratamentos. Atualmente, entretanto, nenhum exame de imagem pode identificar com precisão a desmielinização.
Para colmatar esta lacuna, investigadores do Centro Gordon de imagens médicas no Massachusetts General Hospital e na Harvard Medical School estão investigando o uso de um novo radiotraçador PET – 18F-3-fluoro-4-aminopiridina (18F-3F4AP) – para visualizar lesões desmielinizadas no cérebro. Eles testaram agora o traçador em humanos pela primeira vez, relatando suas descobertas no Revista Europeia de Medicina Nuclear e Imagem Molecular.
“Ter uma ferramenta de imagem específica para a desmielinização pode ajudar a compreender melhor a contribuição da desmielinização para diferentes doenças e monitorar melhor uma doença ou a resposta à terapia – por exemplo, uma terapia remielinizante”, diz o primeiro autor. Pedro Brugarolas Em uma declaração de imprensa.
18F-3F4AP é uma versão radiofluorada do medicamento para esclerose múltipla 4-aminopiridina. O traçador, que entra no cérebro por difusão passiva, liga-se aos axônios desmielinizados de maneira semelhante à própria droga. Estudos anteriores demonstraram que o PET com 18O F-3F4AP pode detectar lesões em um modelo de desmielinização em ratos, e que o traçador tem propriedades adequadas para gerar imagens do cérebro de macacos rhesus, o que levou a equipe a investigar seu uso em humanos.
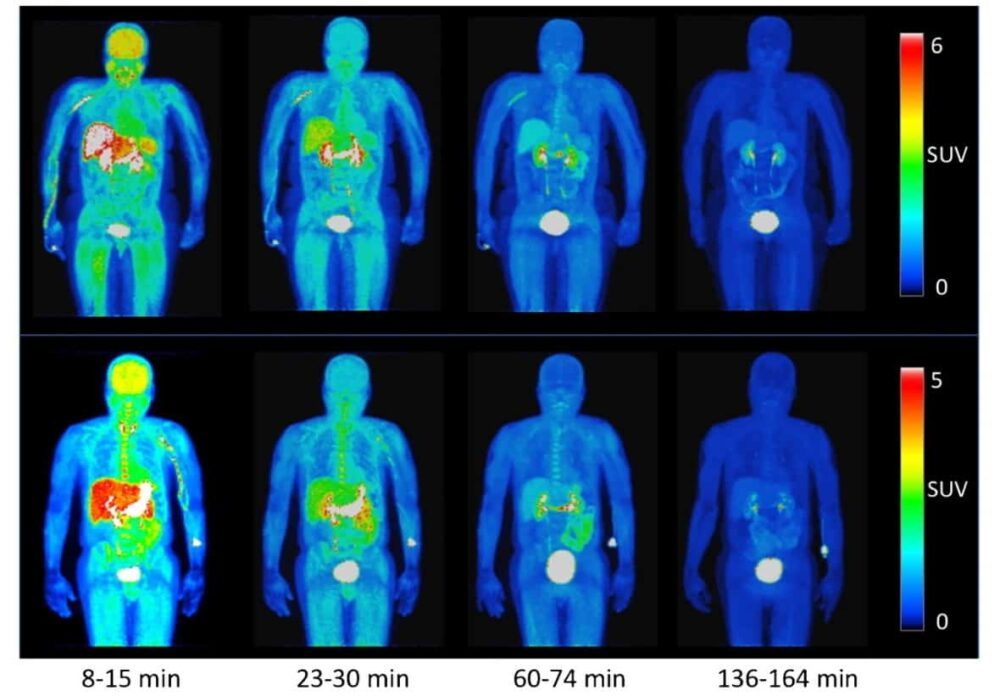
Brugarolas e colegas realizaram PET em quatro voluntários saudáveis após administrar 368±17.9 MBq de 18F-3F4AP. Após uma tomografia computadorizada de baixa dosagem, eles iniciaram a PET imediatamente após a injeção do traçador, registrando uma série de imagens em sete posições do scanner para cobrir todo o corpo. Para capturar a cinética do traçador e maximizar a qualidade da imagem, o tempo inicial de varredura por posição foi de 1 min, aumentando para 2, 4 e 8 min por posição. Toda a aquisição do PET levou 4 horas.
As imagens PET resultantes e as curvas de tempo de atividade (TACs) revelaram que o traçador se distribuiu rapidamente por todo o corpo, incluindo o cérebro, e foi rapidamente eliminado por excreção renal. 8–14 minutos após a injeção, foi observada atividade máxima no fígado, rins, bexiga urinária, baço, estômago e cérebro. Aos 22-28 minutos, a maior atividade ocorreu nos rins, ducto biliar e bexiga urinária. Após 60 minutos, a maior parte da atividade foi eliminada dos órgãos e acumulada na bexiga urinária.
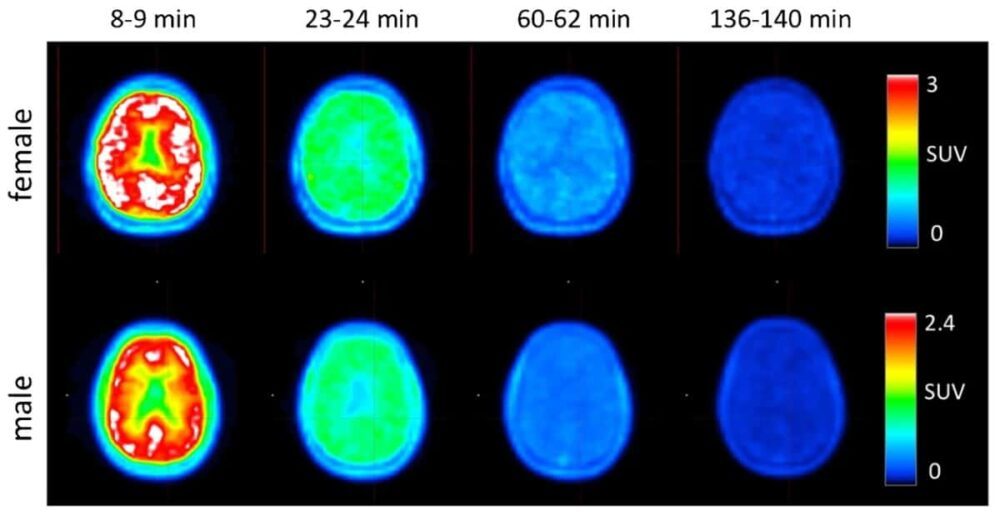
A equipe também utilizou os TACs integrados para realizar a dosimetria. A dose efetiva média foi de 12.2 ± 2.2 µSv/MBq para os quatro participantes, sem diferenças observadas entre voluntários do sexo masculino e feminino. Os investigadores observam que esta dose eficaz é significativamente inferior à estimada a partir de estudos com primatas não humanos (21.6 ± 0.6 µSv/MBq), provavelmente devido à depuração mais rápida observada em humanos do que em macacos rhesus. Esta dose também foi menor do que para outros traçadores PET, como 18F-FDG.
É importante ressaltar que o traçador e o procedimento de imagem foram bem tolerados por todos os participantes, sem ocorrência de eventos adversos durante o exame. Não houve diferenças significativas nos sinais vitais dos voluntários (temperatura, pressão arterial e saturação de oxigênio) antes e depois do exame, e nenhuma alteração significativa nos resultados de metabólitos sanguíneos e eletrocardiograma obtidos 30 dias antes e depois do exame.

PET tracer mede desmielinização em ratos
Os pesquisadores concluem que 18O F-3F4AP entra prontamente no cérebro e é seguro para uso em humanos, com um nível aceitável de dose de radiação. Eles sugerem que suas descobertas abrem portas para novos estudos que investiguem a capacidade do traçador de detectar lesões desmielinizadas em diferentes populações de pacientes.
Brugarolas conta Mundo da física que a equipe está atualmente realizando dois pequenos estudos clínicos usando o novo traçador: para investigar seu valor para imagem de esclerose múltipla; e avaliar seu uso em pacientes com lesão cerebral traumática, comprometimento cognitivo leve e doença de Alzheimer.