HONG KONG, 17 de fevereiro de 2022 – (ACN Newswire) – SinoMab BioScience Limited (“SinoMab” ou a “Empresa”, juntamente com suas subsidiárias, o “Grupo”, código de ações: 3681.HK), uma empresa biofarmacêutica com sede em Hong Kong empresa dedicada à pesquisa, desenvolvimento, fabricação e comercialização de produtos terapêuticos para o tratamento de doenças imunológicas, tem o prazer de anunciar que, em 11 de fevereiro de 2022 (horário local EST), um pedido de Novo Medicamento Investigacional ("IND"), para a Empresa O produto terapêutico para asma SM17 (anticorpo monoclonal humanizado anti-IL17RB para injeção) de primeira classe (FIC) foi submetido e aceito pela Food and Drug Administration ("FDA") dos EUA. A Empresa planeja iniciar o estudo First-In-Human nos EUA no primeiro trimestre de 2022, assim que o IND for aprovado pela FDA.
 |
O SM17 é o primeiro anticorpo monoclonal do mundo direcionado ao IL17BR co-desenvolvido pela SinoMab e LifeArc (uma instituição de caridade de pesquisa médica com sede no Reino Unido). O SM17 possui uma ampla gama de indicações, incluindo indicações com grande volume de mercado, como asma e doenças com altas taxas de mortalidade, como fibrose pulmonar idiopática. Comparando com outros produtos do mercado, o SM17 possui vantagens de diferenciação. Com os dados pré-clínicos e o mecanismo de ação exclusivo do SM17, a empresa acredita que o SM17 tem potencialmente um efeito mais amplo e benéfico no tratamento da asma do que outros biológicos aprovados.
No mercado global, o número de pacientes com asma está aumentando gradualmente e deve chegar a 247.5 milhões em 2023 e aumentar ainda mais para 267.7 milhões em 2030. O número de pacientes com asma na RPC está aumentando em um ritmo maior do que a taxa global e está previsto para atingir 25.6 milhões até 2023 e aumentar ainda mais para 27.8 milhões até 2030. Em termos de tamanho do mercado, o mercado global de asma está projetado para atingir US$ 25.1 bilhões até 2023 e US$ 34.6 bilhões até 2030. No entanto, o mercado de asma no A CRP deverá atingir RMB36.4 bilhões em 2023 e RMB65.0 bilhões em 2030. Em termos de opções de tratamento, o tratamento tradicional da asma é baseado em corticosteróides inalatórios, mas são propensos a efeitos adversos graves, especialmente em adolescentes. A resistência aos medicamentos também pode se desenvolver se usada por um longo tempo. Espera-se que a introdução do SM17 forneça uma melhor opção de tratamento em termos de equilíbrio entre eficácia e segurança.
Dr. Shui On LEUNG, Presidente, Diretor Executivo e Diretor Executivo da SinoMab disse que: "após a aceitação do pedido IND para SN1011 para o tratamento de esclerose múltipla pelo NMPA, a aceitação do pedido SM17 IND pelo FDA demonstra a execução eficiente do programa de P&D de novos medicamentos da Companhia. Ainda há uma necessidade médica não atendida de terapias adicionais eficazes, principalmente para pacientes que não respondem aos tratamentos atuais. Estamos, portanto, confiantes nas enormes perspectivas de desenvolvimento clínico do SM17. Nosso núcleo produtos, incluindo SM03, SN1011 e SM17, está progredindo na pesquisa e desenvolvimento clínico sem problemas, impulsionando a empresa a avançar firmemente para a comercialização. No futuro, aceleraremos a implementação de nossos projetos para trazer benefícios aos pacientes e criar valor para os acionistas por meio da inovação."
Sobre SM17
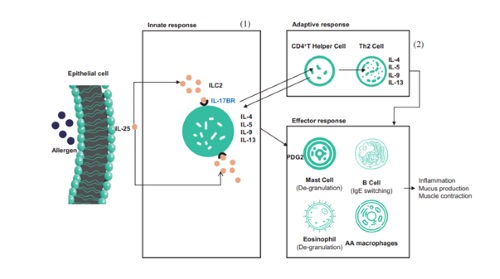
O SM17 é conhecido por ser o primeiro anticorpo monoclonal IgG4-k humanizado do mundo para o desenvolvimento de novos medicamentos, que tem como alvo o IL-17RB. E IL-17RB é uma glicoproteína transmembranar tipo I única pertencente à família de receptores IL-17. A ligação de SM17 a IL-17RB poderia suprimir as respostas imunes Th2 induzidas por uma categoria de citocinas chamada "alarmin", que mostrou estar implicada na patogênese da doença alérgica e nas respostas virais das vias aéreas. Espera-se que uma abordagem alternativa direcionada a mediadores a montante da cascata inflamatória Th2, como "alarminas", tenha um efeito mais amplo na inflamação das vias aéreas e forneça um controle mais eficaz da asma do que as terapias atualmente disponíveis, e produtos com mecanismo de ação semelhante ao SM17 têm sido aprovado pela FDA.
Sobre SinoMab BioScience Limited
A SinoMab BioScience Limited (código de estoque: 3681.HK) dedica-se à pesquisa, desenvolvimento, fabricação e comercialização de produtos terapêuticos para o tratamento de doenças imunológicas. O principal produto da empresa, SM03, é um potencial mAb global primeiro no alvo contra CD22 para o tratamento de artrite reumatóide (AR) e está atualmente em ensaio clínico de Fase III para artrite reumatóide na China, que foi reconhecido como um dos importantes projetos de Desenvolvimento Significativo de Novos Medicamentos do Décimo Segundo Período do Plano Quinquenal e do Décimo Terceiro Período do Plano Quinquenal. Além disso, a Companhia possui outros potenciais candidatos a medicamentos de primeira linha e de primeira linha, alguns dos quais já em estágio clínico, com suas indicações abrangendo artrite reumatóide (AR), lúpus eritematoso sistêmico (LES), pênfigo vulgar (PV), linfoma não Hodgkin (LNH), asma e outras doenças com grandes necessidades clínicas não atendidas.
Copyright 2022 ACN Newswire. Todos os direitos reservados. www.acnnewswire.comSinoMab BioScience Limited ("SinoMab" ou a "Empresa", juntamente com suas subsidiárias, o "Grupo", código de ações: 3681.HK), uma empresa biofarmacêutica com sede em Hong Kong dedicada à pesquisa, desenvolvimento, fabricação e comercialização de terapêuticas para o tratamento de doenças imunológicas
- 11
- 2022
- 7
- acelerar
- Notícias da ACN
- Açao Social
- Adicional
- vantagens
- Todos os Produtos
- já
- Anunciar
- Aplicação
- abordagem
- disponível
- acredita
- Benefícios
- bilhão
- presidente
- Caridade
- chefe
- diretor executivo
- China
- código
- comercialização
- Empresa
- confiante
- ao controle
- direitos autorais
- poderia
- Atual
- dados,
- dedicado
- desenvolver
- Desenvolvimento
- Diretor
- Doença
- doenças
- condução
- droga
- Drogas
- efeito
- Eficaz
- enorme
- especialmente
- executivo
- Diretora Executiva
- esperado
- família
- fda
- Primeiro nome
- seguinte
- comida
- futuro
- Global
- Alta
- HTTPS
- Incluindo
- Crescimento
- Inovação
- conhecido
- grande
- Limitado
- local
- longo
- principal
- Fazendo
- fabrica
- mercado
- médico
- milhão
- Oficial
- Opção
- Opções
- Outros
- fase
- Produto
- Produtos
- Agenda
- projetos
- fornecer
- Trimestre
- R & D
- alcance
- Preços
- pesquisa
- Segurança
- Dito
- periodo
- semelhante
- Tamanho
- Etapa
- estoque
- Estudo
- apresentado
- Através da
- tempo
- juntos
- tradicional
- tratamento
- julgamento
- nos
- único
- Unido
- Reino Unido
- valor
- QUEM