A capacidade de fundir sensores eletrônicos e ópticos com o corpo humano no nível de célula única poderá um dia permitir o monitoramento e controle remoto de células individuais em tempo real. Os avanços na fabricação de eletrônicos tornaram possível a criação de transistores e sensores com resolução em nanoescala, enquanto técnicas inovadoras de nanopadronização permitem a montagem desses dispositivos em substratos flexíveis. Tais processos, no entanto, geralmente requerem produtos químicos agressivos, altas temperaturas ou técnicas de vácuo que são inadequadas para células e tecidos vivos.
Para superar esses obstáculos, uma equipe de pesquisa da Universidade Johns Hopkins desenvolveu um processo não tóxico, de alta resolução e econômico para imprimir nanopadrões de ouro em tecidos e células vivas. Relatando suas descobertas em Nano Letters, eles demonstram que a nova técnica pode “tatuar” células e tecidos vivos com matrizes flexíveis de nanopontos e nanofios de ouro. Em última análise, o método poderia ser usado para integrar dispositivos inteligentes com tecidos vivos para aplicações como biônica e biossensor.
“Se tivéssemos tecnologias para monitorar a saúde de células isoladas, talvez pudéssemos diagnosticar e tratar doenças muito mais cedo e não esperar até que todo o órgão fosse danificado”, explica o líder da equipe. David Gracias em um comunicado à imprensa. “Estamos falando de colocar algo como uma tatuagem eletrônica em um objeto vivo dezenas de vezes menor que a cabeça de um alfinete. É o primeiro passo para conectar sensores e componentes eletrônicos em células vivas.”
graças, Luo Gu e colegas projetaram um processo de impressão por nanotransferência de três estágios para unir nanopadrões de ouro a células vivas. Na primeira etapa, eles usaram litografia de nanoimpressão convencional (NIL) para imprimir matrizes de nanopontos ou nanofios de ouro em pastilhas de silício revestidas com polímero. Eles então dissolveram o polímero, liberando os nanoarranjos para transferência para lamínulas de vidro.
Em seguida, os pesquisadores funcionalizaram a superfície do ouro com cisteamina e revestiram as matrizes NIL de ouro com uma camada de transferência de hidrogel de alginato. Eles mostraram que esta abordagem poderia transferir de forma confiável matrizes de nanopontos e nanofios de 8 × 8 mm do vidro para os hidrogéis macios e flexíveis. Na etapa final, as matrizes NIL de ouro são conjugadas com gelatina para permitir sua transferência para células ou tecidos vivos. A dissociação da camada de transferência de hidrogel expõe então o padrão dourado.
Os pesquisadores investigaram o comportamento de células vivas de fibroblastos semeadas em matrizes de pontos dourados de 250 nm de diâmetro (espaçamento centro a centro de 550 nm) ou fios de ouro de 300 nm de largura (espaçamento de 450 nm) em hidrogéis de alginato. Cerca de 24 horas após a semeadura, as células no hidrogel impresso com nanofios migraram preferencialmente paralelamente aos nanofios, enquanto aquelas nos nanopontos exibiram migração aleatória, mas um pouco mais rápida. As células nos nanofios também exibiram aproximadamente o dobro do alongamento daquelas nos nanopontos. Estas descobertas demonstram a capacidade dos arranjos NIL de ouro para guiar a orientação e migração celular.
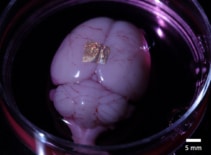
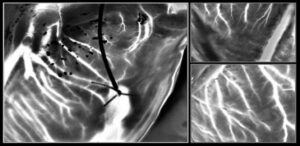
Além de ser biocompatível com células e tecidos, o hidrogel de alginato também pode transferir matrizes NIL de ouro para órgãos e células vivas. Para demonstrar isso, os pesquisadores posicionaram hidrogéis impressos com nanofios no córtex cerebral de um cérebro inteiro e em uma fatia coronal do cérebro.
Após 2 h em meio de cultura e dissociação do hidrogel, os nanofios permaneceram ligados à superfície de todo o cérebro. Em contraste, os nanofios na fatia do cérebro não aderiram, sugerindo que a força de adesão varia entre os diferentes tipos de células e métodos de cultura. Os pesquisadores observam que são necessários mais estudos para caracterizar e otimizar os mecanismos de adesão para uma ligação robusta a longo prazo.
Finalmente, para avaliar a impressão de biotransferência no nível unicelular, os pesquisadores cultivaram folhas de células monocamadas em hidrogéis de alginato impressos em matriz NIL dourada. Após 24 h, eles viraram os hidrogéis semeados de fibroblastos em lamelas revestidas de gelatina e deixaram as células se fixarem nas lamelas durante a noite.
Após dissociar o hidrogel de alginato, a microscopia de fluorescência revelou que os fibroblastos padronizados com nanopontos de ouro tinham viabilidade de aproximadamente 97%, enquanto aqueles padronizados com nanofios tinham viabilidade de aproximadamente 98%, indicando que o processo de impressão é biocompatível com células vivas. As cores reflexivas vistas na folha de células de fibroblastos padronizadas sugerem que a forma da matriz NIL dourada foi mantida.
O processo de fabricação também é compatível com fotolitografia em microescala, o que permitiu aos pesquisadores criar manchas hexagonais e triangulares de 200 µm de largura de matrizes NIL de ouro. Eles então os imprimiram por biotransferência em folhas de células, levando ao crescimento seletivo de células de fibroblastos nas micromanchas. Filmes gravados ao longo de 16 horas mostraram que as células com manchas de nanofios impressas na parte superior pareciam saudáveis e capazes de migrar, com as matrizes permanecendo nas células moles mesmo enquanto elas se moviam.

Pequeno sensor mede simultaneamente a atividade elétrica e mecânica nas células do coração
“Mostramos que podemos anexar nanopadrões complexos a células vivas, garantindo ao mesmo tempo que a célula não morra”, diz Gracias. “É um resultado muito importante que as células possam viver e se mover com as tatuagens porque muitas vezes há uma incompatibilidade significativa entre as células vivas e os métodos que os engenheiros usam para fabricar eletrônicos.”
Gracias e colegas concluem que o seu processo de nanopadronização, combinado com técnicas padrão de microfabricação, “abre oportunidades para o desenvolvimento de novos substratos de cultura celular, materiais biohíbridos, dispositivos biônicos e biossensores”. Em seguida, eles planejam tentar anexar nanocircuitos mais complexos que possam permanecer no local por períodos mais longos, além de fazer experiências com diferentes tipos de células.
- Conteúdo com tecnologia de SEO e distribuição de relações públicas. Seja amplificado hoje.
- PlatoData.Network Gerativa Vertical Ai. Capacite-se. Acesse aqui.
- PlatoAiStream. Inteligência Web3. Conhecimento Amplificado. Acesse aqui.
- PlatãoESG. Automotivo / EVs, Carbono Tecnologia Limpa, Energia, Ambiente, Solar, Gestão de resíduos. Acesse aqui.
- PlatoHealth. Inteligência em Biotecnologia e Ensaios Clínicos. Acesse aqui.
- ChartPrime. Eleve seu jogo de negociação com ChartPrime. Acesse aqui.
- BlockOffsets. Modernizando a Propriedade de Compensação Ambiental. Acesse aqui.
- Fonte: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- :tem
- :é
- :não
- $UP
- 16
- 200
- 24
- 8
- a
- habilidade
- Capaz
- Sobre
- atividade
- aderir
- avanços
- Depois de
- tb
- entre
- an
- e
- apareceu
- aplicações
- abordagem
- aproximadamente
- SOMOS
- por aí
- Ordem
- AS
- Montagem
- avaliar
- At
- anexar
- BE
- Porque
- ser
- entre
- corpo
- vínculo
- Cérebro
- mas a
- CAN
- Células
- caracterizar
- clique
- colegas
- combinado
- compatível
- integrações
- conclui
- contraste
- ao controle
- convencional
- relação custo-benefício
- poderia
- crio
- Cultura
- dia
- demonstrar
- projetado
- desenvolvido
- Desenvolvimento
- Dispositivos/Instrumentos
- DID
- morrem
- diferente
- doenças
- Não faz
- Mais cedo
- Eletrônico
- Eletrônicos
- permitir
- habilitado
- Engenheiros
- assegurando
- Todo
- Mesmo
- Explica
- mais rápido
- final
- descobertas
- Primeiro nome
- flexível
- Escolha
- da
- mais distante
- GAO
- geralmente
- vidro
- Dourado
- Growth
- guia
- tinha
- Ter
- cabeça
- Saúde
- saudável
- Coração
- Alta
- de alta resolução
- Hopkins
- Contudo
- HTTPS
- humano
- imagem
- importante
- in
- Individual
- INFORMAÇÕES
- inovadores
- integrar
- isolado
- emitem
- IT
- johns
- Johns Hopkins University
- jpg
- camada
- líder
- principal
- deixar
- Nível
- como
- viver
- vida
- longo prazo
- mais
- moldadas
- materiais
- max-width
- talvez
- medidas
- mecânico
- mecanismos
- Mídia
- ir
- método
- métodos
- Microscopia
- migrado
- migrou
- migração
- monitoração
- mais
- mover
- movido
- Filmes
- muito
- necessário
- Novo
- Próximo
- objeto
- obstáculos
- of
- frequentemente
- on
- ONE
- para
- aberto
- oportunidades
- Otimize
- or
- Acima de
- Superar
- durante a noite
- Paralelo
- Patches
- padrão
- períodos
- Física
- Mundo da física
- Lugar
- plano
- platão
- Inteligência de Dados Platão
- PlatãoData
- posicionado
- possível
- imprensa
- Impressão
- impressão
- processo
- processos
- Colocar
- acaso
- RAT
- reais
- em tempo real
- gravado
- permaneceu
- remanescente
- remoto
- Relatórios
- requerer
- pesquisa
- pesquisadores
- Resolução
- resultar
- Revelado
- uma conta de despesas robusta
- grosseiramente
- diz
- visto
- seletivo
- sensor
- Shape
- folha
- mostrou
- mostrando
- periodo
- Silício
- simultaneamente
- Fatia
- menor
- smart
- Suave
- algo
- padrão
- Declaração
- ficar
- Passo
- força
- caso
- tal
- sugerir
- superfície
- falando
- Profissionais
- técnicas
- Tecnologias
- dezenas
- do que
- que
- A
- deles
- então
- Este
- deles
- isto
- aqueles
- miniaturas
- tempo
- vezes
- para
- topo
- para
- pista
- transferência
- tratar
- verdadeiro
- tentar
- Twice
- tipos
- Em última análise
- universidade
- até
- usar
- usava
- Vácuo
- muito
- viabilidade
- esperar
- foi
- we
- BEM
- enquanto que
- qual
- enquanto
- inteiro
- Largo
- de
- mundo
- zefirnet