Vasos sanguíneos bloqueados causados por doenças cardiovasculares podem levar a consequências graves, incluindo ataque cardíaco ou derrame. A condição pode ser tratada contornando cirurgicamente o bloqueio usando um vaso de outra parte do corpo do paciente. Quando isso não é viável, um enxerto vascular sintético é geralmente usado. Os enxertos sintéticos apresentam altas taxas de falha, no entanto, devido à inflamação crônica causada pela rejeição do corpo a uma substância estranha. Outra opção são os enxertos vasculares de tecidos humanos (TEVGs), que mostram resultados promissores in vivo resultados, mas requerem processos demorados, complexos e caros para criar.
Agora, pesquisadores da Laboratório do INSERM para a Bioengenharia de Tecidos (BioTis U1026) da Universidade de Bordeaux fabricaram com sucesso TEVGs de pequeno diâmetro usando fios de membrana amniótica humana (HAM) combinados com uma estratégia de tecelagem inspirada em têxteis. Descrevendo o processo em Biofabricação, eles afirmam que esses enxertos têm propriedades notáveis que justificam a mudança para in vivo testes em animais de laboratório.
HAM, a camada mais interna de membranas que envolve um feto durante o desenvolvimento, fornece um “andaime” biológico viável para a engenharia de tecidos. Apresenta propriedades anti-inflamatórias, efeitos antimicrobianos, baixa imunogenicidade (capacidade de provocar uma resposta imune), compatibilidade sanguínea, capacidade de sutura e alta resistência mecânica. Também descartado rotineiramente pelos hospitais e, conseqüentemente, é amplamente disponível e acessível.
Produção de fios
Investigador principal Nicolas L'Heureux e colegas criaram fios HAM a partir de membranas fetais coletadas de pacientes que consentiram após partos cesáreos. Eles prepararam as membranas para uso enxaguando os tecidos repetidamente em água destilada, cortando as membranas em folhas retangulares de 10 x 18 cm e separando manualmente o âmnio e o córion (membranas interna e externa). Um dispositivo de corte motorizado cortou as folhas HAM em fitas de 5 ou 10 mm de largura.
Para criar fios mecanicamente fortes, os pesquisadores prenderam essas fitas a um dispositivo rotativo que as torceu em 5, 7.5 ou 10 revoluções/cm. O diâmetro do fio diminuiu após a torção, estabilizando em 7.5 rotações/cm, enquanto a tensão de tração máxima aumentou significativamente após a torção em 7.5 e 10 rotações/cm.
Os fios HAM (fitas e linhas) foram secos em temperatura ambiente, enrolados e armazenados a -80°C, processo conhecido como desvitalização, pois mata as células. Quando necessário, os pesquisadores reidratavam os fios em água destilada.
Como o objetivo era fornecer um implante pronto para uso, os pesquisadores examinaram os efeitos da descelularização e esterilização com irradiação gama nas fitas HAM. A histologia mostrou que a descelularização removeu efetivamente os componentes celulares que permaneceram após a desvitalização, não afetou a força do HAM e aumentou sua elasticidade.
Quando as fitas HAM secas foram esterilizadas por gama, elas se tornaram mais finas, mais rígidas e menos elásticas. Manter as fitas HAM hidratadas durante a esterilização evitou muitos desses efeitos. Os pesquisadores observaram que a esterilização úmida não afetou a capacidade do HAM de suportar a adesão e o crescimento das células endoteliais.
Tecendo os vasos
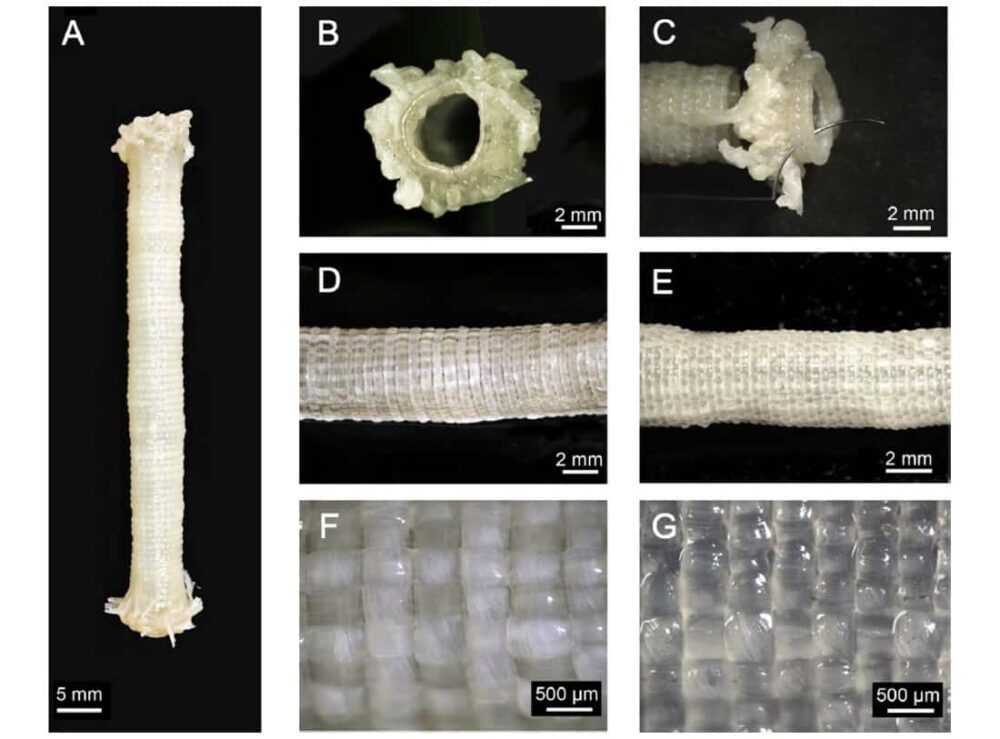
Na etapa final, os pesquisadores montaram os fios HAM em TEVGs. Eles usaram um tear circular feito sob medida para tecer TVEGs em torno de um mandril de aço inoxidável. Para criar um tubo tecido, um fio circunferencial (a “trama”) foi inserido entre um conjunto móvel e um fixo de fitas longitudinais tensionadas (a “urdidura”). Os dois conjuntos de urdidura foram movidos para cruzar a trama, o fio circunferencial foi passado novamente entre eles e o processo foi repetido 50 vezes.
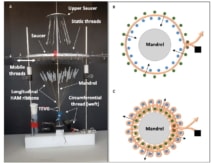
A equipe usou 51 fitas longitudinais (5 mm de largura) e um fio circunferencial de fita dupla para tecer TVEGs com um diâmetro interno médio de 4.4 ± 0.2 mm. Os TEVGs tecidos eram mecanicamente robustos, com força de retenção de sutura superior e pressão de ruptura média àquelas das artérias mamárias internas humanas, o vaso preferido para cirurgia de bypass cardíaco.
No entanto, como a permeabilidade transmural era potencialmente muito alta, a equipe produziu um segundo conjunto de TVEGs usando fitas longitudinais de 10 mm de largura e o mesmo design de rosca circunferencial. Isso criou TEVGs com um diâmetro interno maior de 5.2 ± 0.4 mm. As paredes apresentaram aumento da densidade do fio e redução drástica da permeabilidade transmural. A pressão de ruptura aumentou e a força de retenção da sutura permaneceu a mesma.
“Combinar HAM barato com um método de montagem de tecelagem diminui os custos para produzir TEVGs, evitando o uso de células e biorreatores, que são necessários em outros métodos”, escrevem os autores. “Nenhum método de montagem usado hoje permite a produção barata de TVEGs baseados em HAM com propriedades mecânicas comprovadas compatíveis com implantação arterial.”

Em direção in vitro fabricação de vasos sanguíneos
Os pesquisadores apontam que as estratégias de montagem de inspiração têxtil usando tecelagem, tricô e trança já são amplamente utilizadas para produzir dispositivos médicos. Assim, não deve ser difícil projetar máquinas para manusear fios HAM e permitir a produção em massa de TVEGs após a realização de estudos clínicos bem-sucedidos. Eles acrescentam que o diâmetro do fio, a resistência mecânica e outras propriedades mecânicas podem ser facilmente modificadas para atender a vários requisitos de especificação.
Em seguida, os pesquisadores planejam avaliar o impacto da descelularização e esterilização gama pós-montagem das várias propriedades do tecido TVEG, principalmente no que diz respeito à permeabilidade e elasticidade.