Последний шерстистый мамонт бродил по обширной арктической тундре 4,000 лет назад. Их гены до сих пор живут в величественном животном — азиатском слоне.
Обладая 99.6-процентным сходством в генетическом составе, азиатские слоны являются идеальной отправной точкой для смелого плана по возвращению мамонта – или чего-то близкого к нему – от вымирания. Проект, запущенный биотехнологической компанией Колоссальный в 2021 году вызвала удивление своей невероятной целью.
Общий план действий звучит просто.
Первым шагом является секвенирование и сравнение геномов мамонта и слона. Затем ученые определят гены, лежащие в основе физических особенностей (длинная шерсть, жировые отложения), которые позволили мамонтам выжить при отрицательных температурах, а затем вставят их в клетки слонов с помощью редактирования генов. Наконец, команда перенесет ядро, в котором находится ДНК, из отредактированных клеток в яйцо слона и имплантирует эмбрион в суррогатную мать.
Проблема? Азиатские слоны находятся под угрозой исчезновения, и их клетки, особенно яйца, трудно найти.
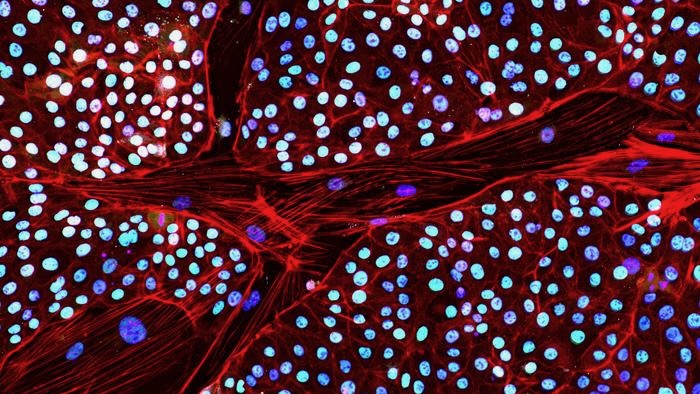
На прошлой неделе компания сообщил об основном обходном пути. Впервые они превратили клетки кожи слона в стволовые клетки, каждая из которых потенциально может стать любой клеткой или тканью организма.
Это достижение упрощает проверку результатов редактирования генов в лаборатории перед тем, как совершить потенциальную беременность, которая у слонов длится до 22 месяцев. Ученые могли бы, например, уговорить модифицированные стволовые клетки слона стать волосковыми клетками и проверить изменения генов, которые придают мамонту легендарную толстую теплую шерсть.
Эти индуцированные плюрипотентные стволовые клетки (иПСК) особенно сложно получить из клеток слона. Животные «представляют собой совершенно особый вид, и мы только начали прикасаться к их фундаментальной биологии». — сказал Доктор Эриона Хисолли, возглавляющая отдел биологических наук в Colossal, в пресс-релизе.
Поскольку для этого подхода нужен только образец кожи азиатского слона, он имеет большое значение для защиты исчезающего вида. Эта технология также может способствовать сохранению живых слонов, обеспечивая программы разведения искусственных яиц, изготовленных из клеток кожи.
«Слоны могут получить приз «труднее всего перепрограммировать»» — сказал Доктор Джордж Черч, генетик из Гарварда и соучредитель Colossal, «но знание того, как это сделать, в любом случае поможет многим другим исследованиям, особенно в отношении исчезающих видов».
Повернуть время вспять
Почти два десятилетия назад японский биолог доктор Шинья Яманака произвел революцию в биологии, вернув зрелые клетки в состояние, подобное стволовым.
Впервые продемонстрированный на мышах метод, получивший Нобелевскую премию, требует всего лишь четырех белков, которые вместе называются факторами Яманаки. Перепрограммированные клетки, часто происходящие из клеток кожи, могут развиваться в различные ткани под дальнейшим химическим контролем.
Индуцированные плюрипотентные стволовые клетки (ИПСК), как их называют, изменили биологию. Они имеют решающее значение для процесса создания органоидов мозга — миниатюрных клубков нейронов, которые искрятся активностью — и могут быть внедрены в яйцеклетки или модели ранних человеческих эмбрионов.
Технология хорошо зарекомендовала себя на мышах и людях. Не так для слонов. «В прошлом множество попыток создать ИПСК слонов не увенчались успехом», — сказал Хисолли.
Большинство клеток слона погибло при лечении стандартным рецептом. Другие превратились в стареющие клетки-зомби — живые, но неспособные выполнять свои обычные биологические функции — или мало изменившиеся по сравнению со своей первоначальной идентичностью.
Дальнейшее расследование выявило виновника: белок под названием TP53. Этот белок, известный своей способностью бороться с раком, часто называют генетическим привратником. Когда ген TP53 включен, белок побуждает предраковые клетки самоуничтожаться, не причиняя вреда своим соседям.
К сожалению, TP53 также препятствует перепрограммированию iPSC. Некоторые из факторов Яманаки имитируют первые стадии роста рака, которые могут привести к самоуничтожению отредактированных клеток. У слонов имеется целых 29 копий гена «защитника». Вместе они могли бы легко раздавить клетки с мутировавшей ДНК, в том числе те, гены которых были отредактированы.
«Мы знали, что p53 будет иметь большое значение», — Черч заявил домен New York Times.
Чтобы обойти «привратника», команда разработала химический коктейль, подавляющий выработку TP53. С последующей дозой факторов репрограммирования они смогли создать первые ИПСК слона из клеток кожи.
Серия тестов показала, что трансформированные клетки выглядели и вели себя так, как ожидалось. У них были гены и белковые маркеры, которые часто можно увидеть в стволовых клетках. Когда им позволили развиться в кластер клеток, они сформировали трехслойную структуру, необходимую для раннего развития эмбриона.
«Мы действительно отчаянно ждали этого», — сказал Черч. заявил природа. Команда опубликовала свои результаты, которые еще не прошли рецензирование, на сервере препринтов bioRxiv.
Долгий путь вперед
Текущий план компании по возвращению мамонта основан на технологиях клонирования, а не на iPSC.
Но эти клетки ценны как заменители яйцеклеток слона или даже эмбрионов, что позволяет ученым продолжать свою работу, не причиняя вреда исчезающим животным.
Например, они могут трансформировать новые стволовые клетки в яйцеклетки или сперматозоиды — на данный момент это настоящий подвиг. достигнуто только на мышах— для дальнейшего генетического редактирования. Другая идея состоит в том, чтобы напрямую превратить их в эмбрионоподобные структуры, оснащенные генами мамонта.
Компания также занимается разработкой искусственные матки чтобы помочь вырастить любые отредактированные эмбрионы и потенциально довести их до срока. В 2017 году в искусственной матке родился здоровый ягненок, а сейчас искусственные матки переход к испытаниям на людях. Эти системы уменьшат потребность в суррогатных слонах и предотвратят угрозу их естественным репродуктивным циклам.
Поскольку исследование представляет собой препринт, его результаты еще не проверены другими экспертами в этой области. Остается много вопросов. Например, сохраняют ли перепрограммированные клетки свой статус стволовых клеток? Могут ли они быть преобразованы в несколько типов тканей по требованию?
Возрождение мамонта — конечная цель Колоссала. Но доктор Винсент Линч из Университета Буффало, который уже давно пытается получить ИПСК из слонов, считает, что результаты могли бы иметь более широкий охват.
Слоны удивительно устойчивы к раку. Никто не знает почему. Поскольку ИПСК, использованные в исследовании, лишены TP53, гена, защищающего от рака, они могут помочь ученым определить генетический код, который позволяет слонам бороться с опухолями, а также потенциально вдохновить нас на новые методы лечения.
Затем команда надеется воссоздать черты мамонта, такие как длинные волосы и жировые отложения, на моделях клеток и животных, изготовленных из генетически отредактированных клеток слона. Если все пойдет хорошо, они будут использовать технику, подобную той, которая использовалась при клонировании овцы Долли, чтобы родить первых телят.
Можно ли называть этих животных мамонтами, до сих пор остается предметом споров. Их геном не будет точно соответствовать вымершему виду. Кроме того, биология и поведение животных сильно зависят от взаимодействия с окружающей средой. Наш климат резко изменился с тех пор, как 4,000 лет назад вымерли мамонты. Арктическая тундра — их старый дом — быстро тает. Могут ли воскресшие животные приспособиться к среде, к которой они не были приспособлены?
Животные также учатся друг у друга. Без живого мамонта, который мог бы показать детенышу, как быть мамонтом в естественной среде обитания, он может вести себя совершенно по-другому.
У Colossal есть общий план решения этих сложных вопросов. Тем временем эта работа поможет проекту продвинуться вперед, не подвергая слонов риску. по данным Церковь.
«Это важный шаг» — сказал Бен Ламм, соучредитель и генеральный директор Colossal. «Каждый шаг приближает нас к нашим долгосрочным целям по возвращению этого культового вида».
Изображение Фото: Колоссальные биологические науки
- SEO-контент и PR-распределение. Получите усиление сегодня.
- PlatoData.Network Вертикальный генеративный ИИ. Расширьте возможности себя. Доступ здесь.
- ПлатонАйСтрим. Интеллект Web3. Расширение знаний. Доступ здесь.
- ПлатонЭСГ. Углерод, чистые технологии, Энергия, Окружающая среда, Солнечная, Управление отходами. Доступ здесь.
- ПлатонЗдоровье. Биотехнологии и клинические исследования. Доступ здесь.
- Источник: https://singularityhub.com/2024/03/12/colossal-creates-elephant-stem-cells-for-the-first-time-in-quest-to-revive-the-woolly-mammoth/
- :имеет
- :является
- :нет
- $UP
- 000
- 2017
- 2021
- 22
- 29
- a
- способность
- в состоянии
- достигнутый
- регулировать
- принять
- продвижение
- тому назад
- Все
- разрешено
- Позволяющий
- позволяет
- причислены
- an
- и
- животное
- животные
- Другой
- любой
- подхода
- арктический
- МЫ
- около
- искусственный
- AS
- азиатский
- At
- попытки
- избежать
- назад
- BE
- , так как:
- становиться
- было
- до
- начал
- поведение
- поведения
- за
- Бен
- большой
- биология
- биотехнология
- рождение
- тело
- булавка
- Мозг
- приносить
- Приведение
- Приносит
- шире
- Строительство
- но
- by
- под названием
- CAN
- рак
- Вызывать
- ячейка
- Клетки
- Генеральный директор
- изменение
- менялась
- химический
- церковь
- климат
- Закрыть
- ближе
- Кластер
- коктейль
- код
- соучредитель
- как
- совершение
- Компания
- Компании
- сравнить
- полностью
- СОХРАНЕНИЕ
- продолжать
- может
- создает
- кредит
- критической
- Текущий
- циклы
- сделка
- дебаты
- десятилетия
- Спрос
- убивают
- зависеть
- Производный
- в отчаянии
- развивать
- развивающийся
- Развитие
- умер
- различный
- трудный
- непосредственно
- Г-жа
- do
- дозировать
- dr
- драматично
- дублированный
- каждый
- Рано
- легче
- легко
- яйца
- слон
- Развитие эмбриона
- инженерии
- Окружающая среда
- оборудованный
- особенно
- Даже
- точно,
- пример
- ожидаемый
- эксперты
- вымирание
- факторы
- далеко
- подвиг
- поле
- бороться
- в заключение
- First
- Впервые
- Что касается
- сформированный
- найденный
- 4
- Замораживание
- от
- плодотворный
- фундаментальный
- далее
- Привратник
- дал
- редактирование гена
- Общие
- порождать
- генетический
- Юрий
- получить
- Дайте
- цель
- Цели
- идет
- будет
- Рост
- руководство
- было
- Hair
- Жесткий
- вредный
- Гарвардский
- Есть
- главы
- здоровый
- здоровенный
- помощь
- мешает
- надеется,
- дома
- Как
- How To
- HTML
- HTTPS
- человек
- Людей
- знаковых
- идея
- определения
- Личность
- if
- in
- В том числе
- внушать
- взаимодействие
- в
- IT
- ЕГО
- Японский
- JPEG
- всего
- известный
- знает
- лаборатория
- Фамилия
- запустили
- УЧИТЬСЯ
- изучение
- такое как
- мало
- жить
- жизнью
- Длинное
- долгосрочный
- смотрел
- искать
- линчевать
- сделанный
- поддерживать
- основной
- сделать
- ДЕЛАЕТ
- макияж
- многих
- Совпадение
- зрелый
- Май..
- то время
- может быть
- Модели
- важный
- месяцев
- полет на Луну
- с разными
- множество
- натуральный
- природа
- Необходимость
- потребности
- соседи
- Нейроны
- Новые
- следующий
- нет
- сейчас
- воспитание
- of
- от
- .
- Старый
- on
- ONE
- только
- or
- оригинал
- Другое
- Другое
- наши
- внешний
- общий
- мимо
- рецензируемых
- процент
- ИДЕАЛЬНОЕ
- Выполнять
- физический
- план
- Платон
- Платон Интеллектуальные данные
- ПлатонДанные
- Точка
- потенциал
- потенциально
- приз
- Проблема
- процесс
- Производство
- Программы
- Проект
- защищающий
- Белкове продукты
- Белки
- обеспечение
- опубликованный
- Полагая
- поиск
- Вопросы
- поднятый
- ассортимент
- быстро
- на самом деле
- рецепт
- полагается
- оставаться
- требуется
- стойкий
- восстановление
- Итоги
- Возрождать
- революция
- Снижение
- Дорога
- Сказал
- образец
- Ученые
- поцарапать
- видел
- Последовательность
- Серии
- сервер
- набор
- овца
- показывать
- показал
- с
- Кожа
- So
- уже
- некоторые
- удалось
- звуки
- Искриться
- особый
- сквош
- этапы
- стандарт
- Начало
- Область
- Статус:
- ножка
- Стволовые клетки
- Шаг
- По-прежнему
- простой
- сильно
- Структура
- структур
- исследования
- Кабинет
- последующее
- поддержка
- Поверхность
- системы
- снасти
- команда
- техника
- технологии
- Технологии
- срок
- тестXNUMX
- тестов
- который
- Ассоциация
- их
- Их
- тогда
- Эти
- они
- вещи
- Думает
- этой
- те
- Thrive
- время
- в
- вместе
- к
- перевод
- Transform
- преобразован
- лечение
- лечение
- пыталась
- Опухоли
- Оказалось
- два
- Типы
- окончательный
- не в состоянии
- Университет
- призывы
- us
- используемый
- через
- обычный
- VALIDATE
- ценный
- Огромная
- очень
- прошедшая проверка
- Винсент
- Ожидание
- теплый
- законопроект
- Путь..
- we
- неделя
- ЧТО Ж
- пошел
- были
- когда
- который
- КТО
- зачем
- будете
- без
- Работа
- бы
- лет
- еще
- йорк
- зефирнет











