Кибератаки на больницы могут иметь разрушительные последствия, особенно для отделений радиологии и лучевой терапии, функционирование которых особенно зависит от технологий. В качестве примера можно привести общенациональную кибератаку на службы общественного здравоохранения Ирландии в мае 2021 года, в результате которой запланированное лучевое лечение некоторых онкологических больных было прервано на срок до 12 дней.
После этого инцидента медицинские физики из Университетская клиника Голуэй и Национальный университет Ирландии Голуэй начали разрабатывать собственный инструмент, помогающий создавать пересмотренные планы лучевой терапии после перерывов. Инструмент под названием EQD2VH – рассчитывает планы компенсации лечения и обеспечивает визуальное сравнение всех вариантов плана, а также индивидуальный анализ каждой структуры в плане пациента. Исследователи описывают новый программный инструмент в Журнал прикладной клинической медицинской физики.
Лучевая терапия чаще всего проводится в течение нескольких недель сериями небольших доз радиации (обычно 2 Гр), называемых фракциями. Незапланированные пробелы в лечении – будь то из-за кибератак, поломок оборудования или болезни пациентов – могут привести к значительным неудачам. Во время таких перерывов раковые клетки быстро заселяются в опухолевой ткани, что приводит к снижению радиобиологической дозы до планового целевого объема (ПТВ).

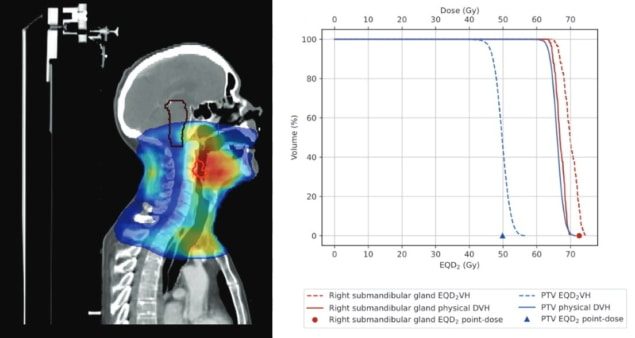
Чтобы решить эту проблему, EQD2VH использует информацию гистограммы «доза-объем» (DVH), извлеченную из исходных планов пациентов, для расчета пробелов в лечении. Ведущий автор Кэти О'Ши из Национального университета Ирландии в Голуэе и его коллеги объясняют, что программное обеспечение преобразует физическую дозу в каждом бункере для доз (диапазон доз между точками данных в DVH) в биологически эффективную дозу (BED). Это объясняет как эффекты репопуляции в PTV, так и эффекты сублетального повреждения невосстановленных нормальных тканей в органах риска (OAR).
После изменения преобразования BED для учета изменений дозы в каждой структуре с использованием метода переменной дозы инструмент преобразует BED для каждой структуры в эквивалентную дозу во фракциях 2 Гр (EQD2). Это нормализует каждую обработку по обычному фракционированию и позволяет суммировать планы с различными схемами фракционирования. Результирующий EQD2 DVH на основе DVH обеспечивает двухмерное представление влияния стратегий компенсации перерывов в лечении на распределение доз PTV и OAR по сравнению с назначенным планом лечения.
Чтобы оценить EQD2В качестве инструмента принятия клинических решений исследователи выбрали пять высокоприоритетных пациентов с быстро растущими опухолями, перерывы в лечении которых не должны превышать двух дней. Сюда вошли четыре пациента с раком головы и шеи, проходящие лучевую терапию с модулированной интенсивностью, и один пациент с раком легких, проходящий 3D-конформную лучевую терапию, у которых перерывы в лечении составляли 12 или 13 дней. Эти случаи позволили команде оценить использование EQD.2ВГ для пациентов как с традиционным (2 Гр), так и с нетрадиционным (2.2 Гр) фракционированием и разным периодом перерыва в лечении (от 46 до XNUMX дней после начала терапии).
Пересмотренные планы лечения для каждого пациента были основаны на их первоначальных планах с измененной дозой на фракцию или количеством фракций. О'Ши объясняет, что в пересмотренном плане и графике лечения каждого пациента использовалась комбинация фракционирования два раза в день, лечения по выходным и увеличения дозы до целевого объема, чтобы уменьшить эффекты репопуляции клеток.
Планы ограничивали лечение шестью фракциями в неделю и исключали фракционирование два раза в день в последовательные дни. Если назначенное лечение не могло быть завершено в требуемые сроки, исследователи исследовали планы с использованием гипофракционирования (доставки увеличенной дозы за фракцию). Они смогли визуально и количественно сравнить различные пересмотренные планы с первоначальным планом пациента, чтобы определить, какой из них обеспечит лучшую дозу для PTV и наименьшую дозу для OAR.
Исследователи отмечают, что двумерное представление каждой отдельной структуры в EQD2VH обеспечивает более глубокий анализ, чем метод расчета точечной дозы 1D, рекомендованный Королевским колледжем радиологов (RCR), который в настоящее время используется для устранения пробелов в лучевой терапии. Одномерное представление распределения дозы внутри объема не учитывает то, что OAR обычно имеет неравномерное распределение дозы, и может привести к завышенной оценке дозы OAR. Кроме того, EQD2Инструмент VH может создавать планы на любую продолжительность перерыва в лечении, тогда как рекомендации RCR основаны на стандартном перерыве в четыре-пять дней.
Дополнительные преимущества нового инструмента включают возможность контролировать каждое OAR в плане пациента, чтобы свести к минимуму дальнейшее увеличение дозы, которое может вызвать более острую токсичность. Пользователи также могут рассчитать влияние различной продолжительности перерывов в лечении на лечение пациента. Эта возможность может помочь определить, следует ли переводить пациента в другую клинику, если перерыв в запланированной клинике слишком велик, или же пациент может безопасно дождаться возобновления лечения.

Как COVID-19 повлиял на предоставление лучевой терапии?
ЭКД2VH также может учитывать изменения в общей продолжительности лечения и сублетальные повреждения нормальных тканей, чего коммерческие системы могут быть не в состоянии сделать. Самое главное, что для работы этого инструмента не требуется подключение к сети больницы — его можно использовать, даже если серверы больницы все еще повреждены кибератакой.
«Мы все еще оцениваем EQD2ВГ как инструмент принятия решений», — говорит главный исследователь Маргарет Мур из университетской больницы Голуэя. «Это часть текущего проекта по рассмотрению пациентов, получающих многократное повторное лечение для паллиативных режимов, где доза на фракцию нестандартна и где может быть рассмотрен выбор схем фракционирования. Преобразование лечебной дозы из нескольких курсов лечения с разными фракционированиями в EQD2 позволяет накапливать радиобиологическую дозу, поражающую ткани и ОАР, для общего обзора дозы, что может помочь в принятии решения о выборе дальнейшего лечения».