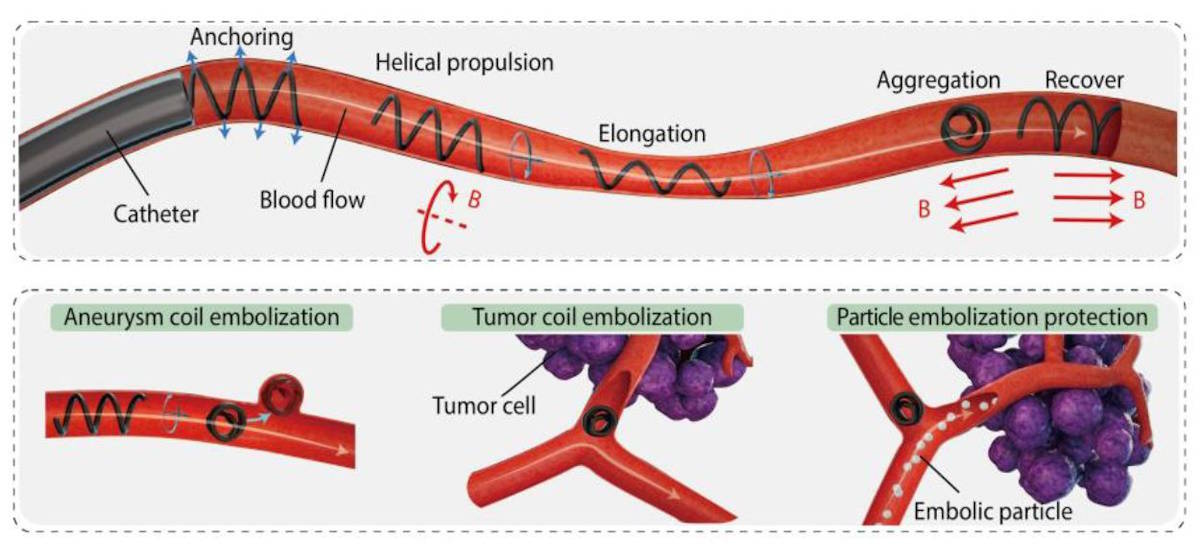
Группа исследователей в Китае разработала новые «микрофибреботы» с магнитной спиралью и использовала их для эмболизации артериального кровотечения у кролика, открыв путь к ряду контролируемых и менее инвазивных методов лечения аневризм и опухолей головного мозга.
Пытаясь остановить кровотечение при аневризмах или остановить приток крови к опухолям головного мозга (процесс, известный как эмболизация), хирурги обычно проводят тонкий катетер через бедренную артерию и проводят его через кровеносные сосуды для доставки эмболических агентов. Несмотря на широкое использование, эти катетеры трудно провести через сложную сосудистую сеть.
Пытаясь решить эту проблему, группа исследователей из Хуачжунского университета науки и технологий (г.ХУСТ) создали крошечных магнитных, мягких микрофибреботов, которые могут выполнять такие процедуры удаленно. Устройства, изготовленные из намагниченного волокна, скрученного в форме спирали, могут подходить к сосудам разного размера и двигаться как штопор под воздействием внешнего магнитного поля. Результаты исследования, представленные в Робототехника, продемонстрировали, как эти устройства были успешно использованы для остановки артериального кровотечения у кролика.
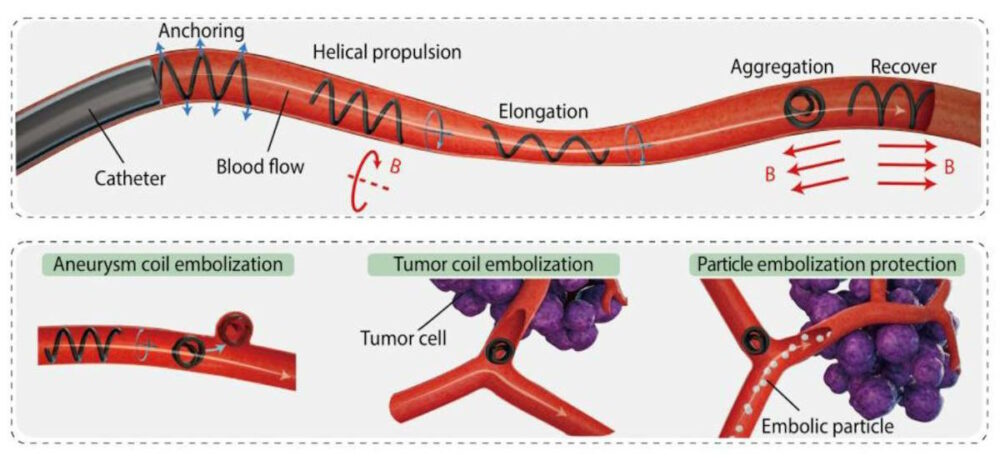
Как соавтор Цзяньфэн Чжан объясняет, что микрофибреботы изготавливаются с использованием тепловой энергии для вытягивания магнитно-мягких композитных материалов в микроволокна, которые затем «намагничиваются и формуются, чтобы придать им спиральную магнитную полярность». Управляя магнитным полем, магнитный робот из мягкого микроволокна продемонстрировал обратимую морфологическую трансформацию (удлинение или агрегацию) и спиральное движение через кровоток (как вверх, так и вниз по течению). Это позволяет ему проходить через сложные сосудистые системы и выполнять роботизированную эмболизацию в субмиллиметровой области.
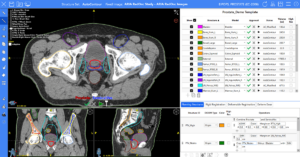
«В статье показано, как мы выступали в пробирке эмболизацию аневризм и опухолей на нейроваскулярной модели, а также выполнил роботизированную навигацию и эмболизацию под рентгеноскопией в реальном времени в в естественных условиях Модель бедренной артерии кролика», — говорит Занг. «Эти эксперименты демонстрируют потенциальную клиническую ценность этой работы и открывают путь для будущих вариантов хирургической эмболизации с помощью робота».
Функция привязки
По словам первого автора Сюруи Лю, аспиранта HUST, каждый микрофибребот обладает функцией крепления, аналогичной функции сосудистого стента, что позволяет ему стабильно прикрепляться к внутренней стенке кровеносных сосудов посредством контактного трения, чтобы избежать вымывания кровоток.
«Его спиральное распределение намагниченности обеспечивает роботу из микроволокна чистое направление намагничивания вдоль его центральной оси. Применяя внешнее магнитное поле, соответствующее направлению суммарной намагниченности, робота можно удлинить», — говорит она.
«И наоборот, когда внешнее магнитное поле противоположно направлению чистой намагниченности, робот будет собираться», — добавляет она. «Мягкость и высокая прочность этого робота из микроволокна гарантируют, что его функция морфологической реконструкции остается полностью обратимой после более чем тысячи циклов агрегации и удлинения».
Многообещающая альтернатива
В отличие от магнитно-мягких роботов, о которых сообщалось в более ранних исследованиях, Занг подтверждает, что характеристики направления спирального намагничивания новых роботов позволяют их режимам деформации и движения ортогонально развязываться независимо от управляющего магнитного поля, обеспечивая «уникальную гибкость управления магнитным полем».
«Эта функция не только позволяет одному роботу из микроволокна двигаться с высокой скоростью против потока крови под действием вращающегося магнитного поля, но также позволяет независимо контролировать форму и движение нескольких роботов из микроволокна», — объясняет Занг.
«Кроме того, эти устройства совместимы с широко используемыми интервенционными катетерами, что максимально увеличивает их потенциал для использования в клинических условиях», — добавляет он.
Столкнувшись с проблемами традиционных методов, таких как катетерная эмболизация, особенно с точки зрения их эксплуатационных ограничений и недостаточной точности, а также с рисками для здоровья, связанными с воздействием радиации врачей в течение длительных периодов времени (согласно рентгенологическому руководству система) – Занг отмечает, что развитие технологии магнитных микрофибреботов предоставляет врачам новые средства улучшения существующих методов лечения.
Магнитные микророботы выстраиваются в очередь для терапии стволовыми клетками
«Разработка микрофибреботов открывает новую перспективу в лечении сосудистой эмболизации и показывает потенциал их применения в технологии минимально инвазивного хирургического лечения. Эта технология обеспечивает эффективное дополнение или альтернативу традиционной технологии катетерной эмболизации, поскольку позволяет точно контролировать окклюзию кровотока», — говорит он.
Занг отмечает, что, хотя эта технология демонстрирует потенциал, все еще существуют проблемы, которые необходимо преодолеть перед ее клиническим применением. К ним относятся структурная оптимизация микрофибреботов, повышение биосовместимости материалов и разработка систем позиционирования и отслеживания кровеносных сосудов. «Исследовательская группа работает над решением этих ключевых проблем для продвижения применения технологии», — добавляет он.
- SEO-контент и PR-распределение. Получите усиление сегодня.
- PlatoData.Network Вертикальный генеративный ИИ. Расширьте возможности себя. Доступ здесь.
- ПлатонАйСтрим. Интеллект Web3. Расширение знаний. Доступ здесь.
- ПлатонЭСГ. Углерод, чистые технологии, Энергия, Окружающая среда, Солнечная, Управление отходами. Доступ здесь.
- ПлатонЗдоровье. Биотехнологии и клинические исследования. Доступ здесь.
- Источник: https://physicsworld.com/a/magnetic-microbots-show-promise-for-treating-aneurysms-and-brain-tumours/
- :имеет
- :является
- :нет
- $UP
- 160
- 80
- a
- Действие
- адрес
- Добавляет
- продвижение
- После
- против
- агенты
- совокупный
- агрегирование
- позволяет
- вдоль
- причислены
- альтернатива
- Несмотря на то, что
- an
- Ведущий
- привязанного
- и
- Применение
- Приложения
- Применение
- МЫ
- гайд
- AS
- At
- попытки
- автор
- избежать
- прочь
- Ось
- BE
- не являетесь
- Кровотечение
- Заблокировать
- кровь
- изоферменты печени
- Дно
- Мозг
- но
- by
- CAN
- нести
- ячейка
- центральный
- вызов
- проблемы
- характеристика
- Китай
- нажмите на
- Клинический
- клиницисты
- Соавтор
- катушка
- обычно
- совместим
- комплемент
- комплекс
- последовательный
- обращайтесь
- контраст
- контроль
- управление
- создали
- циклы
- разъединены
- доставить
- демонстрировать
- убивают
- развитый
- Развитие
- Устройства
- различный
- трудный
- направление
- распределение
- Врачи
- рисовать
- каждый
- Ранее
- Эффективный
- усилие
- включить
- позволяет
- позволяет
- энергетика
- обеспечивает
- существующий
- Эксперименты
- Объясняет
- подвергаться
- и, что лучший способ
- Фэшн
- Особенность
- поле
- Во-первых,
- соответствовать
- поток
- Что касается
- трение
- от
- полностью
- функция
- будущее
- собирать
- в общем
- Дайте
- руководство
- инструкция
- he
- Медицина
- High
- Как
- HTTP
- HTTPS
- изображение
- улучшение
- in
- включают
- повышение
- независимые
- самостоятельно
- информация
- внутренний
- в
- агрессивный
- вопрос
- вопросы
- IT
- ЕГО
- JPG
- Основные
- известный
- Меньше
- недостатки
- линия
- Длинное
- сделанный
- Магнитное поле
- материалы
- макс-ширина
- Максимизировать
- означает
- методы
- модель
- Режимы
- БОЛЕЕ
- двигаться
- движение
- с разными
- Узкий
- Откройте
- Навигация
- сеть
- сетей
- Новые
- Заметки
- роман
- of
- только
- открытый
- оперативный
- противоположность
- оптимизация
- Опции
- or
- внешний
- Преодолеть
- панель
- особенно
- pass
- вымостить
- Мощение
- Выполнять
- выполнены
- периодов
- перспектива
- кандидат наук
- Физика
- Мир физики
- Платон
- Платон Интеллектуальные данные
- ПлатонДанные
- пунктов
- позиционирование
- обладает
- потенциал
- Точно
- Точность
- представлены
- Предварительный
- Процедуры
- процесс
- обещание
- силовая установка
- приводит
- обеспечение
- кролик
- ассортимент
- реального времени
- область
- районы
- Связанный
- остатки
- удаленно
- Сообщается
- исследованиям
- исследователи
- Итоги
- рисках,
- робот
- Роботы
- прочность
- Run
- говорит
- Наука
- Наука и технологии
- селективный
- настройки
- Форма
- она
- показывать
- показ
- Шоу
- аналогичный
- одинарной
- Размеры
- мягкая
- скорость
- спиральный
- ножка
- По-прежнему
- Stop
- структурный
- "Студент"
- Успешно
- такие
- хирургический
- система
- системы
- команда
- Технологии
- terms
- чем
- который
- Ассоциация
- их
- Их
- тогда
- Там.
- тепловой
- Эти
- этой
- тысяча
- Через
- миниатюрами
- время
- в
- топ
- Отслеживание
- традиционный
- трансформация
- лечения
- лечение
- лечение
- правда
- под
- Университет
- использование
- используемый
- через
- ценностное
- Судно
- с помощью
- стена
- Путь..
- we
- ЧТО Ж
- были
- когда
- , которые
- в то время как
- широко
- будете
- Работа
- работает
- Мир
- рентгеновский
- зефирнет