Глубокая стимуляция мозга (DBS), при которой электроды, имплантированные в мозг, доставляют электрические импульсы к определенным мишеням, является эффективным клиническим методом лечения ряда неврологических состояний. DBS в настоящее время используется для лечения двигательных расстройств, таких как болезнь Паркинсона, эссенциальный тремор и дистония, а также таких состояний, как эпилепсия и обсессивно-компульсивное расстройство. Однако лечение требует хирургического вмешательства на головном мозге для введения электродов стимуляции, что может вызвать многочисленные побочные эффекты.
Чтобы устранить необходимость в инвазивной хирургии, исследователи из Пхоханского университета науки и технологий (POSTECH) в Корее разрабатывают стратегию неинвазивной нервной стимуляции на основе пьезоэлектрических наночастиц. Наночастицы выполняют две функции: временное открытие гематоэнцефалического барьера (ГЭБ) и стимуляцию высвобождения дофамина — обе функции контролируются внешним сфокусированным ультразвуком.
Пьезоэлектрические наночастицы представляют интерес как нейростимуляторы, поскольку в ответ на внешние раздражители, такие как ультразвук, например, они деформируются и выделяют постоянный ток. Исследователи предполагают, что этот ток можно затем использовать для стимуляции дофаминергических нейронов для высвобождения нейротрансмиттеров.
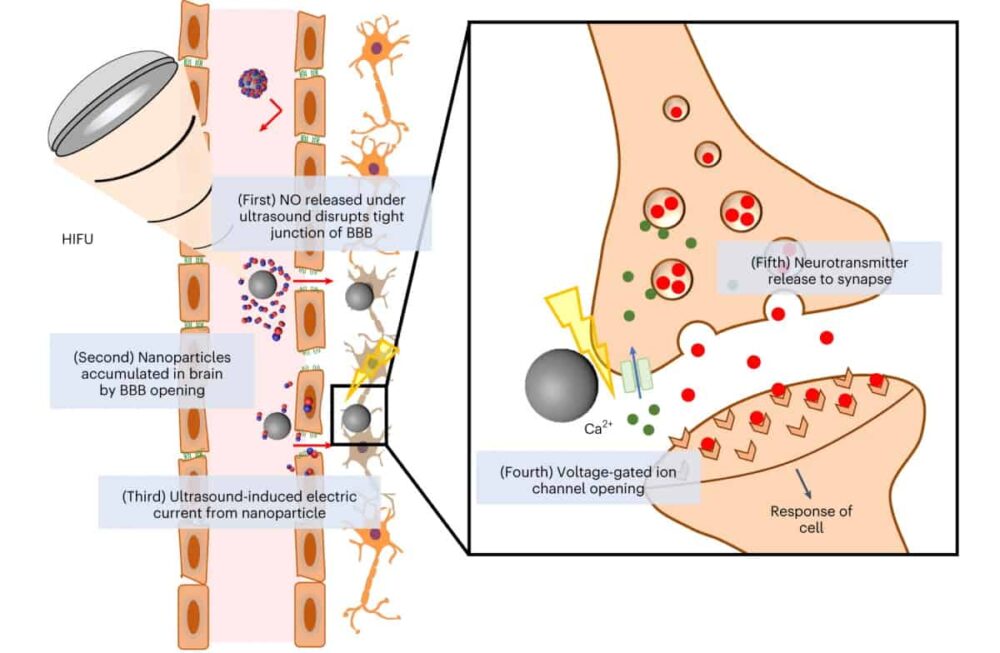
Одной из ключевых проблем является доставка наночастиц в мозг, в частности, как провести их через ГЭБ. Чтобы достичь этого, исследователи обратились к оксиду азота (NO), высокореактивной молекуле, которая демонстрирует потенциал для разрушения ГЭБ. Они разработали многофункциональную систему, описанную в Природа Биомедицинская инженерия, содержащий наночастицу титаната бария, покрытую NO-высвобождающим BNN6 и полидофамином (pDA). В ответ на ультразвук эти наночастицы должны генерировать как NO, так и постоянный ток.
Чтобы проверить свой подход, ведущий автор Вон Джон Ким и его коллеги впервые исследовали способность наночастиц выделять NO. В ответ на воздействие высокоинтенсивного сфокусированного ультразвука (HIFU) в течение 5 с наночастицы мгновенно высвобождали NO. Они также оценили пьезоэлектрические свойства с помощью установки патч-зажим. В то время как растворитель без наночастиц, покрытых pDA, не проявлял всплески тока, в присутствии наночастиц наблюдались отчетливые всплески тока с интенсивностью, пропорциональной интенсивности ультразвука.
Предполагается, что DBS электрически стимулирует нервную систему, открывая Ca2+ каналов близлежащих нейронов, а затем ускоряет высвобождение нейротрансмиттера в синапсе. Чтобы выяснить, может ли ток, генерируемый наночастицами, обеспечить аналогичную нервную стимуляцию, команда исследовала кальций.2+ динамика нейроноподобных клеток. Внутриклеточный кальций2+ концентрация значительно увеличивалась в клетках, получавших как наночастицы, так и ультразвук, тогда как ни ультразвук, ни только наночастицы не оказывали никакого эффекта.
Клетки, обработанные наночастицами, стимулированными ультразвуком, также генерировали повышенную внеклеточную концентрацию дофамина, что указывает на Ca.2+ высвобождение нейротрансмиттеров, опосредованное притоком. Опять же, никаких существенных изменений не наблюдалось ни с ультразвуком, ни с наночастицами. Испытания с использованием непьезоэлектрических наночастиц показали незначительные изменения концентрации Ca.2+ притока и высвобождения нейротрансмиттеров, что указывает на то, что эти эффекты возникают в основном в ответ на пьезоэлектрическую стимуляцию.
Затем исследователи провели серию в естественных условиях исследования. Чтобы исследовать NO-опосредованное открытие ГЭБ, они внутривенно вводили мышам пьезоэлектрические наночастицы, высвобождающие NO, а затем применяли HIFU к целевым участкам мозга под ультразвуковым контролем.
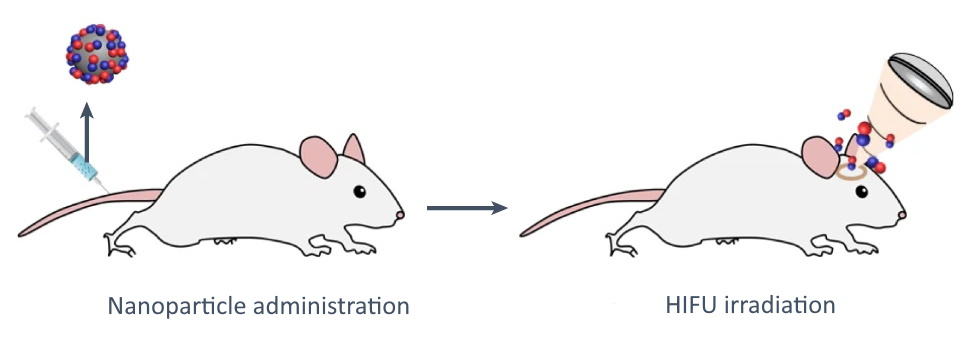
Через два часа после инъекции просвечивающая электронная микроскопия выявила значительно большее количество наночастиц, накопленных в мозге животных по сравнению с контрольными группами, демонстрируя, что высвобождение NO временно нарушает плотные контакты в ГЭБ. Исследователи также показали, что через 2 часа после применения HIFU ГЭБ больше не был проницаемым, подтверждая, что NO-опосредованное нарушение ГЭБ носит временный характер.
Наконец, команда оценила терапевтические эффекты наночастиц, используя мышиную модель болезни Паркинсона. Мышам вводили наночастицы с последующим многократным применением HIFU в субталамическом ядре (место нацеливания DBS, одобренное Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США) для восстановления уровня дофамина в головном мозге.
DBS с использованием наночастиц, управляемых ультразвуком, улучшала поведенческие функции животных, включая координацию движений и двигательную активность. У мышей наблюдалось постепенное улучшение двигательной функции при ежедневной HIFU-стимуляции в течение 10 дней, при этом двигательная активность почти восстанавливалась к 16-му дню. Команда предполагает, что пьезоэлектрические наночастицы индуцировали высвобождение нейротрансмиттера, что значительно облегчало симптомы болезни Паркинсона, не вызывая какой-либо значительной токсичности. .

Персонализированная стимуляция мозга может лечить неизлечимую депрессию
«Мы надеемся, что чувствительные к ультразвуку пьезоэлектрические наночастицы, высвобождающие NO, можно будет в дальнейшем превратить в минимально инвазивные терапевтические подходы для лечения нейродегенеративных заболеваний», — заключают они.
В настоящее время группа использует фундаментальные исследования для определения основных механизмов NO-опосредованного открытия ГЭБ. «Мы также разрабатываем материалы нового поколения, модулирующие NO, чтобы максимизировать их клиническое использование, а также свести к минимуму их нежелательные побочные эффекты», — объясняет первый автор. Тэджон Ким.