Kibernetski napadi na bolnišnice imajo lahko uničujoče posledice, zlasti za oddelke za radiologijo in radioterapijo, katerih delovanje je še posebej odvisno od tehnologije. Primer je kibernetski napad po vsej državi na irske javne zdravstvene službe maja 2021, ki je za do 12 dni prekinil načrtovano radioterapijo pri nekaterih bolnikih z rakom.
Po tem incidentu so medicinski fiziki pri Univerzitetna bolnišnica Galway in Nacionalna univerza Irske Galway začeli razvijati interno orodje za pomoč pri ustvarjanju revidiranih načrtov zdravljenja z radioterapijo po prekinitvah. Orodje – imenovano EQD2VH – izračuna kompenzacijske načrte zdravljenja in omogoča vizualno primerjavo vseh možnosti načrta ter individualno analizo posamezne strukture v pacientovem načrtu. Raziskovalci opisujejo novo programsko orodje v Journal of Applied Clinical Medical Physics.
Radioterapija se najpogosteje izvaja več tednov v seriji majhnih odmerkov sevanja (običajno 2 Gy), imenovanih frakcije. Nenačrtovane vrzeli v zdravljenju – bodisi zaradi kibernetskih napadov, okvar strojev ali bolezni bolnika – lahko povzročijo precejšnje ovire. Med takimi vrzelmi se rakave celice hitro ponovno naselijo v tumorskem tkivu, kar povzroči zmanjšanje radiobiološke doze na načrtovani ciljni volumen (PTV).

Za rešitev te težave je EQD2VH uporablja podatke histograma odmerek-volumen (DVH), pridobljene iz prvotnih načrtov bolnika, da izvede izračun vrzeli med zdravljenjem. Vodilna avtorica Katie O'Shea z Nacionalne univerze Irske Galway in sodelavci pojasnjujejo, da programska oprema pretvori fizični odmerek v vsakem odmerku (razpon odmerka med podatkovnimi točkami v DVH) v biološko učinkovit odmerek (BED). To pojasnjuje učinke repopulacije v PTV in učinke subletalne poškodbe nepopravljenega normalnega tkiva v ogroženih organih (OAR).
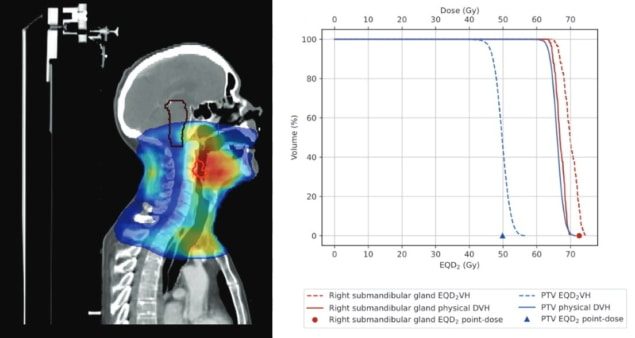
Po spremembi pretvorbe BED za upoštevanje variacij odmerka v vsaki strukturi z uporabo metode spremenljivega odmerka orodje pretvori BED za vsako strukturo v ekvivalentno dozo v frakcijah 2 Gy (EQD2). To normalizira vsako obdelavo na običajno frakcioniranje in omogoča seštevanje načrtov z različnimi shemami frakcioniranja. Rezultat EQD2 DVH na osnovi DVH zagotavlja 2D predstavitev vpliva strategij kompenzacije vrzeli pri zdravljenju na porazdelitev odmerka PTV in OAR v primerjavi s predpisanim načrtom zdravljenja.
Za oceno EQD2VH kot orodje za klinično odločanje so raziskovalci izbrali pet visoko prioritetnih bolnikov s hitro rastočimi tumorji, katerih vrzeli v zdravljenju ne bi smele preseči dveh dni. To je vključevalo štiri bolnike z rakom glave in vratu, ki so bili podvrženi intenzivnostno modulirani radioterapiji, in enega bolnika s pljučnim rakom, ki je bil podvržen 3D konformni radioterapiji, ki so imeli 12 ali 13 dni presledkov med zdravljenjem. Ti primeri so ekipi omogočili oceno uporabe EQD2VH za bolnike s konvencionalno (2 Gy) in nekonvencionalno (2.2 Gy) frakcioniranjem ter različnimi časi presledkov med zdravljenjem (od devet do 46 dni njihove terapije).
Revidirani načrti zdravljenja za vsakega bolnika so temeljili na njihovih prvotnih načrtih s spremenjenim odmerkom na frakcijo ali številom frakcij. O'Shea pojasnjuje, da je revidirani načrt in urnik vsakega pacienta uporabljal kombinacijo frakcioniranja dvakrat na dan, zdravljenja ob koncu tedna in povečanega odmerka do ciljnega volumna za zmanjšanje učinkov repopulacije celic.
Načrti so omejili zdravljenje na šest frakcij na teden in izključevali frakcioniranje dvakrat na dan v zaporednih dneh. Če predpisanega zdravljenja ni bilo mogoče dokončati v zahtevanem časovnem okviru, so raziskovalci raziskali načrte z uporabo hipofrakcioniranja (dostava povečanega odmerka na frakcijo). Lahko so vizualno in kvantitativno primerjali različne revidirane načrte z bolnikovim prvotnim načrtom, da bi ugotovili, kateri bi zagotovil najboljši odmerek za PTV in najmanjši odmerek za OAR.
Raziskovalci ugotavljajo, da je 2D predstavitev vsake posamezne strukture v EQD2VH zagotavlja bolj poglobljeno analizo kot 1D metoda izračuna točkovnega odmerka, ki jo priporoča Royal College of Radiologs (RCR), ki se trenutno uporablja za obvladovanje vrzeli v radioterapiji. 1D predstavitev porazdelitve odmerka znotraj prostornine ne upošteva OAR-jev, ki imajo običajno neenakomerno porazdelitev odmerka in bi lahko precenila odmerek OAR. Poleg tega EQD2Orodje VH lahko ustvari načrte za poljubno dolžino vrzeli med zdravljenjem, medtem ko smernice RCR temeljijo na standardni vrzeli štirih do petih dni.
Dodatne prednosti novega orodja vključujejo zmožnost spremljanja vsakega OAR v pacientovem načrtu za zmanjšanje nadaljnjih povečanj odmerka, ki bi lahko povzročila večjo akutno toksičnost. Uporabniki lahko tudi izračunajo vpliv različnih dolžin prekinitve zdravljenja na bolnikovo zdravljenje. Ta zmožnost lahko pomaga ugotoviti, ali bolnika premestiti v drugo kliniko, če je vrzel na načrtovani kliniki predolga, ali pa lahko varno počaka na nadaljevanje zdravljenja.

Kako je COVID-19 vplival na zagotavljanje radioterapije?
EQD2VH lahko povzroči tudi spremembe v celotnem času zdravljenja in subletalne poškodbe normalnega tkiva, česar komercialni sistem morda ne bo zmogel. Najpomembneje je, da orodja za delovanje ni treba povezati z bolnišničnim omrežjem – uporablja se lahko tudi, če so bolnišnični strežniki še vedno poškodovani zaradi kibernetskega napada.
»Še vedno ocenjujemo EQD2VH kot orodje za odločanje,« pravi glavna raziskovalka Margaret Moore iz Univerzitetne bolnišnice Galway. »To je del trenutnega projekta, ki pregleduje paciente, ki prejemajo večkratno ponovno zdravljenje za paliativne režime, kjer je odmerek na frakcijo nestandarden in kjer je morda treba upoštevati izbiro shem frakcioniranja. Pretvarjanje odmerka zdravljenja iz številnih zdravljenj z različnimi frakcioniranji v EQD2 omogoča zbiranje radiobiološke doze za ciljna tkiva in OAR za celoten pregled doze, ki lahko pomaga pri odločanju za izbiro nadaljnjega zdravljenja.«