HONG KONG, Feb 17, 2022 – (ACN Newswire) – SinoMab BioScience Limited ("SinoMab" or the "Company", together with its subsidiaries, the "Group", stock code: 3681.HK), a Hong Kong-based biopharmaceutical company dedicated to the research, development, manufacturing and commercialization of therapeutics for the treatment of immunological diseases, is pleased to announce that, on 11 February 2022 (EST local time), an Investigational New Drug application ("IND"), for the Company's First-in-Class (FIC) asthma therapeutic product SM17 (Humanized anti-IL17RB monoclonal antibody for injection) has been submitted and accepted by the U.S. Food and Drug Administration ("FDA"). The Company plans to initiate the First-In-Human study in the U.S. in first quarter of 2022, once IND is approved by FDA.
 |
SM17 เป็นโมโนโคลนอลแอนติบอดีตัวแรกของโลกที่มีเป้าหมายไปที่ IL17BR ซึ่งพัฒนาโดย SinoMab และ LifeArc (องค์กรการกุศลด้านการวิจัยทางการแพทย์ที่ตั้งอยู่ในสหราชอาณาจักร) SM17 มีข้อบ่งชี้ที่หลากหลาย รวมถึงการบ่งชี้ที่มีปริมาณการตลาดสูง เช่น โรคหอบหืดและโรคที่มีอัตราการเสียชีวิตสูง เช่น โรคพังผืดในปอดที่ไม่ทราบสาเหตุ เมื่อเปรียบเทียบกับผลิตภัณฑ์อื่นๆ ในตลาด SM17 มีข้อได้เปรียบที่แตกต่าง ด้วยข้อมูลพรีคลินิกและกลไกการออกฤทธิ์เฉพาะของ SM17 บริษัทเชื่อว่า SM17 อาจมีผลในวงกว้างและเป็นประโยชน์มากกว่าในการรักษาโรคหอบหืดมากกว่าสารชีวภาพที่ผ่านการรับรองอื่นๆ
ในตลาดโลก จำนวนผู้ป่วยโรคหอบหืดค่อยๆ เพิ่มขึ้น และคาดว่าจะถึง 247.5 ล้านคนภายในปี 2023 และเพิ่มขึ้นอีกเป็น 267.7 ล้านคนภายในปี 2030 จำนวนผู้ป่วยโรคหอบหืดในสาธารณรัฐประชาชนจีนเพิ่มขึ้นในอัตราที่สูงกว่าอัตราทั่วโลกและ คาดการณ์ว่าจะถึง 25.6 ล้านในปี 2023 และเพิ่มขึ้นอีกเป็น 27.8 ล้านในปี 2030 ในแง่ของขนาดตลาด ตลาดโรคหอบหืดทั่วโลกคาดว่าจะสูงถึง 25.1 พันล้านดอลลาร์ในปี 2023 และ 34.6 พันล้านดอลลาร์สหรัฐภายในปี 2030 อย่างไรก็ตาม ตลาดโรคหอบหืดใน คาดว่า PRC จะแตะระดับ 36.4 พันล้านหยวนภายในปี 2023 และ 65.0 พันล้านหยวนภายในปี 2030 ในแง่ของทางเลือกการรักษา การรักษาโรคหอบหืดแบบดั้งเดิมนั้นใช้คอร์ติโคสเตียรอยด์ที่สูดดม แต่มักเกิดผลข้างเคียงที่รุนแรง โดยเฉพาะในวัยรุ่น การดื้อยาสามารถพัฒนาได้หากใช้เป็นเวลานาน การเปิดตัว SM17 คาดว่าจะเป็นทางเลือกในการรักษาที่ดีขึ้นในแง่ของความสมดุลของประสิทธิภาพและความปลอดภัย
Dr. Shui On LEUNG ประธาน กรรมการบริหาร และประธานเจ้าหน้าที่บริหารของ SinoMab กล่าวว่า: "หลังจากการยอมรับแอปพลิเคชัน IND สำหรับ SN1011 สำหรับการรักษาโรคปลอกประสาทเสื่อมแข็งโดย NMPA การยอมรับแอปพลิเคชัน SM17 IND โดย FDA อย่างเต็มที่ แสดงให้เห็นถึงการดำเนินการอย่างมีประสิทธิภาพของโครงการ R&D ด้านยาใหม่ของบริษัท ยังคงมีความต้องการทางการแพทย์ที่ไม่ได้รับการตอบสนองสำหรับการรักษาที่มีประสิทธิภาพเพิ่มเติม โดยเฉพาะอย่างยิ่งสำหรับผู้ป่วยที่ไม่ตอบสนองต่อการรักษาในปัจจุบัน เราจึงมั่นใจในโอกาสที่มหาศาลของการพัฒนาทางคลินิกของ SM17 หลักของเรา ผลิตภัณฑ์ต่างๆ ซึ่งรวมถึง SM03, SN1011 และ SM17 กำลังก้าวหน้าในการวิจัยและพัฒนาทางคลินิกอย่างราบรื่น ขับเคลื่อนบริษัทให้ก้าวไปสู่การค้าอย่างมั่นคง ในอนาคต เราจะเร่งดำเนินการโครงการของเราให้เป็นประโยชน์แก่ผู้ป่วยและสร้างมูลค่าให้กับผู้ถือหุ้นผ่านนวัตกรรม"
เกี่ยวกับ SM17
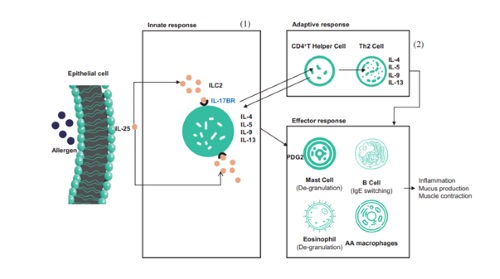
SM17 เป็นที่ทราบกันดีว่าเป็นโมโนโคลนอลแอนติบอดี IgG4-k ที่มีลักษณะของมนุษย์ตัวแรกของโลกสำหรับการพัฒนายาใหม่ซึ่งมีเป้าหมายที่ IL-17RB และ IL-17RB เป็นไกลโคโปรตีนชนิดทรานส์เมมเบรนเดี่ยวที่เป็นของแฟมิลีรีเซพเตอร์ IL-17 การผูกมัดของ SM17 กับ IL-17RB สามารถยับยั้งการตอบสนองของภูมิคุ้มกัน Th2 ที่เกิดจากไซโตไคน์ประเภทหนึ่งที่เรียกว่า "อลาร์มิน" ซึ่งแสดงให้เห็นว่ามีความเกี่ยวข้องในการเกิดโรคของโรคภูมิแพ้และการตอบสนองของไวรัสทางเดินหายใจ แนวทางทางเลือกที่กำหนดเป้าหมายตัวกลางทางต้นน้ำของน้ำตกอักเสบ Th2 เช่น "สัญญาณเตือน" คาดว่าจะมีผลในวงกว้างต่อการอักเสบของทางเดินหายใจ และเพื่อให้การควบคุมโรคหอบหืดมีประสิทธิภาพมากกว่าการรักษาที่มีอยู่ในปัจจุบัน และผลิตภัณฑ์ที่มีกลไกการทำงานคล้ายคลึงกันกับ SM17 ได้รับการอนุมัติจากอย.
เกี่ยวกับ SinoMab BioScience Limited
SinoMab BioScience Limited (รหัสสินค้า: 3681.HK) ทุ่มเทให้กับการวิจัย พัฒนา การผลิต และการจำหน่ายยารักษาโรคสำหรับการรักษาโรคทางภูมิคุ้มกัน ผลิตภัณฑ์เรือธงของบริษัท SM03 เป็น mAb ที่เป็นเป้าหมายแรกในระดับโลกเมื่อเทียบกับ CD22 สำหรับการรักษาโรคข้ออักเสบรูมาตอยด์ (RA) และขณะนี้อยู่ในการทดลองทางคลินิกระยะที่ XNUMX สำหรับโรคข้ออักเสบรูมาตอยด์ในประเทศจีน ซึ่งได้รับการยอมรับว่าเป็นหนึ่งในโรคพิเศษที่สำคัญ โครงการการพัฒนายาใหม่ที่สำคัญของระยะเวลาแผนห้าปีที่สิบสองและระยะเวลาแผนห้าปีที่สิบสาม นอกจากนี้ บริษัทยังมียาที่มีศักยภาพอันดับหนึ่งและหนึ่งในกลุ่มยา ซึ่งบางรายอยู่ในขั้นตอนทางคลินิกแล้ว โดยมีข้อบ่งชี้ครอบคลุมถึงโรคข้ออักเสบรูมาตอยด์ (RA), โรคลูปัส erythematosus (SLE), pemphigus vulgaris (PV), มะเร็งต่อมน้ำเหลืองชนิดนอนฮอดจ์กิน (NHL), โรคหอบหืด และโรคอื่นๆ ที่มีความต้องการทางคลินิกที่สำคัญที่ไม่ได้รับการตอบสนอง
ลิขสิทธิ์ 2022 ACN Newswire สงวนลิขสิทธิ์. www.acnnewswire.comSinoMab BioScience Limited ("SinoMab" หรือ "บริษัท" ร่วมกับบริษัทในเครือ "กลุ่ม" รหัสหุ้น: 3681.HK) ซึ่งเป็นบริษัทชีวเภสัชภัณฑ์ในฮ่องกงที่ทุ่มเทให้กับการวิจัย พัฒนา การผลิต และการจำหน่ายยารักษาโรคเพื่อรักษาโรคทางภูมิคุ้มกัน
- 11
- 2022
- 7
- เร่งความเร็ว
- เอซีเอ็นนิวส์ไวร์
- การกระทำ
- เพิ่มเติม
- ข้อได้เปรียบ
- ทั้งหมด
- แล้ว
- ประกาศ
- การใช้งาน
- เข้าใกล้
- ใช้ได้
- เชื่อ
- ประโยชน์ที่ได้รับ
- พันล้าน
- ประธานกรรมการ
- การกุศล
- หัวหน้า
- ประธานเจ้าหน้าที่บริหาร
- สาธารณรัฐประชาชนจีน
- รหัส
- การค้า
- บริษัท
- มั่นใจ
- ควบคุม
- ลิขสิทธิ์
- ได้
- ปัจจุบัน
- ข้อมูล
- ทุ่มเท
- พัฒนา
- พัฒนาการ
- ผู้อำนวยการ
- โรค
- โรค
- การขับขี่
- ยาเสพติด
- ยาเสพติด
- ผล
- มีประสิทธิภาพ
- มหาศาล
- โดยเฉพาะอย่างยิ่ง
- ผู้บริหารงาน
- ผู้อำนวยการบริหาร
- ที่คาดหวัง
- ครอบครัว
- องค์การอาหารและยา
- ชื่อจริง
- ดังต่อไปนี้
- อาหาร
- อนาคต
- เหตุการณ์ที่
- จุดสูง
- HTTPS
- รวมทั้ง
- เพิ่ม
- นักวิเคราะห์ส่วนบุคคลที่หาโอกาสให้เป็นไปได้มากที่สุด
- ที่รู้จักกัน
- ใหญ่
- ถูก จำกัด
- ในประเทศ
- นาน
- สำคัญ
- การทำ
- การผลิต
- ตลาด
- ทางการแพทย์
- ล้าน
- เจ้าหน้าที่
- ตัวเลือกเสริม (Option)
- Options
- อื่นๆ
- ระยะ
- ผลิตภัณฑ์
- ผลิตภัณฑ์
- โครงการ
- โครงการ
- ให้
- หนึ่งในสี่
- วิจัยและพัฒนา
- พิสัย
- ราคา
- การวิจัย
- ความปลอดภัย
- กล่าวว่า
- สำคัญ
- คล้ายคลึงกัน
- ขนาด
- ระยะ
- สต็อก
- ศึกษา
- ส่ง
- ตลอด
- เวลา
- ร่วมกัน
- แบบดั้งเดิม
- การรักษา
- การทดลอง
- เรา
- เป็นเอกลักษณ์
- พร้อมใจกัน
- สหราชอาณาจักร
- ความคุ้มค่า
- WHO