การบำบัดด้วยภูมิคุ้มกัน - การควบคุมระบบภูมิคุ้มกันของร่างกายเพื่อต่อสู้กับมะเร็ง - มีศักยภาพในการปฏิวัติการรักษามะเร็ง แต่ในขณะที่มะเร็งเม็ดเลือด เช่น มะเร็งเม็ดเลือดขาวและมะเร็งต่อมน้ำเหลืองตอบสนองได้ดีต่อการบำบัดด้วยภูมิคุ้มกันมะเร็ง เนื้องอกที่เป็นก้อนจะแสดงการตอบสนองที่จำกัด
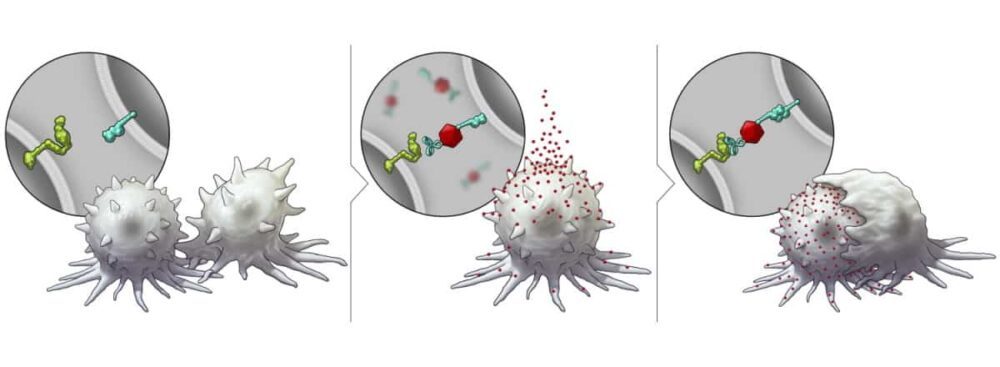
เหตุผลหนึ่งที่เป็นไปได้สำหรับความไม่เท่าเทียมกันนี้คือการแสดงออกที่หลากหลายของโปรตีนพื้นผิวในมะเร็งชนิดต่างๆ ตัวอย่างเช่น โปรตีน SLAMF7 ที่จับกับเยื่อหุ้มเซลล์ – ซึ่งกระตุ้นระบบภูมิคุ้มกันและกระตุ้นเซลล์ทำลายเซลล์ (การกลืนกิน) เซลล์มะเร็งโดยเซลล์ภูมิคุ้มกัน – แสดงออกโดยเซลล์มะเร็งในเลือด แต่ไม่ใช่โดยเนื้องอกที่เป็นของแข็ง
นักวิจัยที่ ศูนย์มะเร็งมหาวิทยาลัยนอร์ทเทกซัส ได้พัฒนาแพลตฟอร์มนาโนเทคโนโลยีที่กระตุ้นการแสดงออกของ SLAMF7 อธิบายไว้ใน นาโนเทคโนโลยีธรรมชาติแพลตฟอร์มดังกล่าวมีพื้นฐานมาจากอนุภาคนาโนที่เปลี่ยนรูปเป็นเนื้องอกแบบคู่ (BiTNs) ซึ่งประกอบด้วยแกนโพลีเมอร์ที่เชื่อมกับลิแกนด์ที่กำหนดเป้าหมายเป็นเนื้องอกและ SLAMF7
“ด้วยแพลตฟอร์มใหม่นี้ ตอนนี้เรามีกลยุทธ์ในการแปลงเนื้องอกที่เป็นก้อน อย่างน้อยในทางภูมิคุ้มกันวิทยา ให้มีลักษณะคล้ายกับเนื้องอกทางโลหิตวิทยา ซึ่งมักจะมีอัตราการตอบสนองต่อการรักษาด้วยภูมิคุ้มกันบำบัดสูงกว่ามาก” เหวินเจียงซึ่งเป็นผู้นำการศึกษาร่วมกับ เบ็ตตี้ คิม. “หากเราสามารถแปลและรับรองแนวทางนี้ในคลินิกได้ อาจช่วยให้เราเข้าใกล้ระดับสูงสุดของกิจกรรมจากยาภูมิคุ้มกันบำบัดกับมะเร็งที่ปกติแล้วตอบสนองได้ไม่ดี”
ในหลอดทดลอง และ ในร่างกาย การประเมินผล
นักวิจัยได้ตรวจสอบแพลตฟอร์มเป็นครั้งแรก ในหลอดทดลองโดยใช้เซลล์มะเร็งเต้านม HER2-positive พวกเขาสร้าง BiTNs เฉพาะเซลล์สำหรับการใช้งานนี้โดยการเชื่อมอนุภาคนาโนกับแอนติบอดีต่อต้าน HER2 เพื่อจับกับเซลล์เนื้องอก และ SLAMF7 เพื่อกระตุ้นการตอบสนองทางภูมิคุ้มกัน นาโนคอนจูเกตที่เป็นผลลัพธ์ – BiTNเธอ – เลือกเซลล์มะเร็งเต้านมที่มี HER2 เป็นบวกและระบุเซลล์เหล่านั้นด้วย SLAMF7
ทีมงาน BiTN ยืนยันว่าเธอ- เซลล์มะเร็งที่มีฉลากกระตุ้นให้เกิดฟาโกไซโทซิสในระดับที่สูงขึ้นเมื่อเทียบกับอนุภาคนาโนที่ไม่ต่อกัน บีทีเอ็นเธอ ยังทำให้เซลล์มะเร็งเต้านมไวต่อการรักษาด้วยแอนติบอดีต่อต้าน CD47 ซึ่งจะบล็อกสัญญาณ "อย่ากินฉัน" จากเซลล์เนื้องอก ทำให้กิจกรรมฟาโกไซติกเพิ่มขึ้น
ต่อไป ทีมประเมิน BiTNเธอ ในหนูที่มีเนื้องอกมะเร็งเต้านมของเซลล์ TUBO ซึ่งแสดงเซลล์ HER2 หรือ 4T1 เวอร์ชันหนูที่ไม่มีตัวรับนี้ การรักษาด้วย BiTNเธอ ร่วมกับสารต้าน CD47 ช่วยลดภาระของเนื้องอกและยืดอายุการรอดชีวิตของหนูที่มีเนื้องอก TUBO; ไม่พบผลต้านมะเร็งในเนื้องอก 4T1
นักวิจัยทราบว่าการรักษาแบบผสมผสานนำไปสู่การยับยั้งเนื้องอกอย่างมีนัยสำคัญเมื่อเทียบกับ BiTNs หรือ anti-CD47 เพียงอย่างเดียว การศึกษาความเป็นพิษระยะยาวพบว่าไม่มีความแตกต่างอย่างมีนัยสำคัญในการนับเม็ดเลือดระหว่างหนูที่ไม่ได้รับการรักษาและหนูที่ได้รับการรักษา
เพื่อแสดงให้เห็นถึงความเก่งกาจของแพลตฟอร์ม BiTN นักวิจัยได้ปรับแต่งอนุภาคนาโนเพื่อกำหนดเป้าหมายไปยังตัวรับเนื้องอกอีกตัวหนึ่ง ซึ่งก็คือตัวรับโฟเลตที่แสดงออกโดยมะเร็งเต้านมที่มีผลลบสามเท่า พวกเขาสร้าง BiTNFo โดยการแทนที่แอนติบอดีต่อต้าน HER2 ด้วยโฟเลต บีทีเอ็นFo กำหนดเป้าหมายและเปลี่ยนเซลล์มะเร็งเป็นเซลล์ที่แสดง SLAMF7 ตามที่คาดไว้ การบ่มเซลล์ 4T1 ด้วย BiTNFo และแอนติ-CD47 ทำให้เกิดฟาโกไซโทซิสมากกว่าที่พบในเซลล์ทูโบ
“เนื่องจากสิ่งเหล่านี้เป็นโครงสร้างเชิงวิศวกรรม จึงสามารถใช้เป็นวิธีแบบปลั๊กแอนด์เพลย์เพื่อรวมเอาสารที่กำหนดเป้าหมายเนื้องอกหรือโมเลกุลภูมิคุ้มกันต่างๆ ลงบนพื้นผิวของอนุภาคนาโน” คิมกล่าวในแถลงการณ์
นักวิจัยยังได้ทดสอบ BiTNFo ในแบบจำลองหนูที่แพร่กระจาย 4T1 ที่เกิดขึ้นเอง การรักษาเนื้องอกหลักด้วย BiTNFo และแอนติซีดี47 ก่อนตัดไหม การรวมกันนี้ยับยั้งการกลับเป็นซ้ำของโรคในท้องถิ่น แต่ไม่ได้ลดการแพร่กระจายที่ห่างไกลหรือยืดอายุการรอดชีวิตโดยรวม อย่างไรก็ตาม การเพิ่มสารต้าน PD1 ในการรักษา นำไปสู่การยับยั้งการแพร่กระจายเป็นเวลานาน โดยหนูสองในเจ็ดตัวแสดงการอยู่รอดโดยปราศจากเนื้องอกในระยะยาว
การบำบัดด้วยภูมิคุ้มกันและการฉายรังสีรักษาเนื้องอกในสมองในหนู
สุดท้าย เพื่อเพิ่มความเกี่ยวข้องในการแปลของโมเดลนี้ ทีมวิจัยได้ตรวจสอบระบบการรักษาหลังการผ่าตัด ที่นี่ เนื้องอกในหนูถูกตัดออกในวันที่ 12 โดยไม่มีการรักษาล่วงหน้า จากนั้นในวันที่ 15 สัตว์ได้รับการรักษาด้วย BiTN รวมกันสามเท่าFo, แอนติ-CD47 และแอนติ-PD1 การรักษาหลังการผ่าตัดนี้ยับยั้งการแพร่กระจายและการรอดชีวิตที่ยาวนาน ซึ่งบ่งชี้ว่าแม้ไม่มีการรักษาในเนื้องอก BiTNs ก็สามารถช่วยกำจัดเซลล์เนื้องอกที่ตกค้างและลดโรคทางระบบได้
ต่อไป นักวิจัยกำลังมุ่งเน้นไปที่การแปลเทคโนโลยีใหม่นี้ในคลินิก “เพื่อให้การแปลผลทางคลินิกง่ายขึ้น เรากำลังสำรวจกลยุทธ์ที่ใช้โปรตีนเป็นหลัก ซึ่งเราจะพัฒนาโปรตีนที่มีความจำเพาะแบบคู่ที่สามารถทำหน้าที่คล้ายกับ BiTN” Jiang กล่าว โลกฟิสิกส์. "สิ่งนี้จะต้องมีวิศวกรรมโปรตีน/แอนติบอดี แต่น่าจะง่ายกว่าในการปฏิบัติตามกฎระเบียบ"