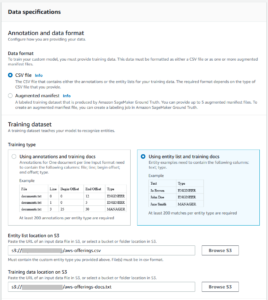
İlaçlarını piyasada satmak için ABD Gıda ve İlaç Dairesi (FDA) veya Japon İlaç ve Tıbbi Cihaz Kurumu (PMDA) gibi düzenleyici kurumlardan onay isteyen ilaç şirketleri, ilaçlarının amacına uygun olarak güvenli ve etkili olduğunu kanıtlamak için kanıt sunmalıdır. kullanmak. Doktorlar, istatistikçiler, kimyagerler, farmakologlar ve diğer klinik bilim adamlarından oluşan bir ekip, klinik araştırma sunum verilerini ve önerilen etiketlemeyi gözden geçirir. İnceleme, ilacın sağlık yararlarının risklerinden daha ağır bastığını kanıtlamak için yeterli istatistiksel kanıt olduğunu tespit ederse, ilaç satışa onaylanır.
Klinik araştırma sunum paketi, tablolaştırılmış veriler, analiz verileri, araştırma meta verileri ve istatistiksel tablolar, listeler ve rakamlardan oluşan istatistiksel raporlardan oluşur. ABD FDA söz konusu olduğunda, elektronik ortak teknik belge (eCTD), FDA'nın Biyolojik Değerlendirme ve Araştırma Merkezi'ne (CBER) ve İlaç Değerlendirme ve Araştırma Merkezi'ne başvuruların, değişikliklerin, eklerin ve raporların sunulması için standart formattır ( CDER). FDA ve Japon PMDA için, tablo halindeki verileri CDISC Standart Veri Tablolama Modeli'nde (SDTM), analiz verilerini CDISC Analiz Veri Kümesi Modelinde (ADAM) ve CDISC Define-XML'de (Operasyonel Veri Modeline dayalı olarak) deneme meta verilerini göndermek yasal bir gerekliliktir. (ODM)).
Bu yazıda RStudio'yu nasıl kullanabileceğimizi gösteriyoruz. Amazon Adaçayı Yapıcı bu tür düzenleyici gönderim çıktıları oluşturmak için. Bu gönderi, klinik araştırma gönderme sürecini, klinik araştırma araştırma verilerini nasıl alabileceğimizi, verileri nasıl tablolaştırıp analiz edebileceğimizi ve ardından istatistiksel raporlar (özet tablolar, veri listeleri ve şekiller (TLF)] oluşturabileceğimizi açıklar. Bu yöntem, ilaç müşterilerinin AWS ortamlarında depolanan klinik verilere sorunsuz bir şekilde bağlanmasına, R kullanarak işlemesine ve klinik deney araştırma sürecini hızlandırmasına yardımcı olabilir.
İlaç geliştirme süreci
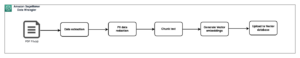
İlaç geliştirme süreci, aşağıdaki şekilde gösterildiği gibi genel olarak beş ana adıma ayrılabilir.
Bir ilacın yaklaşık 10 potansiyel molekül arasından başarılı bir onay alması ortalama 15-1 yıl ve yaklaşık 3-10,000 milyar ABD doları alır. Araştırmanın erken aşamalarında (ilaç keşif aşaması), klinik öncesi araştırmalara doğru ilerleyen umut verici ilaç adayları belirlenir. Klinik öncesi aşamada, araştırmacılar ilacın toksisitesini deneyerek bulmaya çalışırlar. in vitro laboratuvarda deneyler ve in vivo hayvanlar üzerinde deneyler. Klinik öncesi testlerden sonra ilaçlar, güvenlik ve etkinliklerini belirlemek için insanlar üzerinde test edilmeleri gereken klinik araştırma araştırma aşamasına geçer. Araştırmacılar klinik deneyler tasarlar ve klinik deney protokolünde çalışma planını detaylandırır. İlaç güvenliğini ve dozajını belirlemek için küçük Faz 1 çalışmalardan, ilaç etkililiğini ve yan etkilerini belirlemek için daha büyük Faz 2 çalışmalarına ve ilaç etkililiğini, güvenliğini ve dozunu belirlemek için daha da büyük Faz 3 ve 4 denemelerine kadar farklı klinik araştırma aşamalarını tanımlarlar. advers reaksiyonların izlenmesi. Başarılı insan klinik deneylerinden sonra, ilaç sponsoru ilacı pazarlamak için bir Yeni İlaç Başvurusu (NDA) sunar. Düzenleyici kurumlar tüm verileri gözden geçirir, reçete etiketleme bilgileri üzerinde sponsorla birlikte çalışır ve ilacı onaylar. İlacın onaylanmasından sonra düzenleyici kurumlar, tam ürünün güvenliğini sağlamak için pazar sonrası güvenlik raporlarını gözden geçirir.
1997 yılında, ilaç şirketleri, CRO'lar, biyoteknoloji, akademik kurumlar, sağlık hizmeti sağlayıcıları ve devlet kurumlarından oluşan küresel, kar amacı gütmeyen bir kuruluş olan Clinical Data Interchange Standards Consortium (CDISC) gönüllü grup olarak başlatıldı. CDISC, toplamadan gönderimlere kadar veri akışını kolaylaştırmak için veri standartları yayınlamış ve ortaklar ile sağlayıcılar arasında veri alışverişini kolaylaştırmıştır. CDISC aşağıdaki standartları yayınlamıştır:
- CDASH (Klinik Veri Toplama Standartları Uyumlaştırması) – Toplanan veriler için standartlar
- SDTM (Çalışma Veri Tablolama Modeli) – Tablolanmış verilerin gönderilmesi için standartlar
- ADaM (Analiz Veri Modeli) – Analiz verileri için standartlar
- GÖNDER (Klinik Olmayan Verilerin Değişimi Standardı) – Klinik olmayan veriler için standartlar
- PRM (Protokol Temsil Modeli) – Protokol standartları
Bu standartlar, eğitimli gözden geçirenlerin, standart araçları kullanarak verileri daha etkili ve hızlı bir şekilde analiz etmesine yardımcı olarak ilaç onay sürelerini kısaltabilir. Tüm tablo halindeki verilerin SDTM formatını kullanarak gönderilmesi ABD FDA ve Japon PMDA tarafından düzenleyici bir gerekliliktir.
Klinik araştırma araştırma gönderileri için R
SAS ve R, ilaç endüstrisinde kullanılan en çok kullanılan istatistiksel analiz yazılımlarından ikisidir. SDTM standartlarının geliştirilmesi CDISC tarafından başlatıldığında, SAS ilaç endüstrisinde ve FDA'da neredeyse evrensel kullanımdaydı. Ancak R, açık kaynak olması ve sürekli olarak yeni paketler ve kütüphaneler eklendiği için günümüzde muazzam bir popülerlik kazanıyor. Öğrenciler, akademik çalışmaları ve araştırmaları sırasında öncelikle R'yi kullanır ve R'ye olan bu aşinalığı işlerine de taşırlar. R ayrıca gelişmiş derin öğrenme entegrasyonları gibi yeni ortaya çıkan teknolojiler için destek sunar.
AWS gibi bulut sağlayıcıları artık ilaç müşterilerinin altyapılarını barındırmak için tercih ettikleri platform haline geldi. AWS, bulutta makine öğrenimi (ML) modelleri oluşturmayı, eğitmeyi ve dağıtmayı zahmetsiz hale getiren SageMaker gibi yönetilen hizmetler de sağlar. SageMaker ayrıca bir web tarayıcısı aracılığıyla herhangi bir yerden RStudio IDE'ye erişim sağlar. Bu gönderi, istatistiksel programcıların ve biyoistatistikçilerin klinik verilerini R ortamına nasıl alabileceklerini, R kodunun nasıl çalıştırılabileceğini ve sonuçların nasıl saklandığını ayrıntılarıyla anlatır. Klinik deney veri bilimcilerinin XPT dosyalarını R ortamına almalarına, SDTM ve ADaM için R veri çerçeveleri oluşturmalarına ve son olarak bir Amazon Basit Depolama Hizmeti (Amazon S3) nesne depolama paketi.
SageMaker'da RStudio
2 Kasım 2021'de, AWS ile işbirliği içinde RStudio PBC açıkladı genel kullanılabilirliği SageMaker'da RStudio, endüstrinin buluttaki ilk tam olarak yönetilen RStudio Workbench IDE'si. Kendi kendini yöneten RStudio ortamlarınızı yalnızca birkaç basit adımda kolayca SageMaker'a geçirmek için artık mevcut RStudio lisansınızı getirebilirsiniz. Bu heyecan verici işbirliği hakkında daha fazla bilgi edinmek için şu adrese göz atın: Amazon SageMaker'da RStudio duyurusu.
RStudio Workbench ile birlikte, R geliştiricileri için RStudio paketi ayrıca RStudio Connect ve RStudio Paket Yöneticisi'ni de sunar. RStudio Connect, veri bilimcilerin öngörüler, gösterge tabloları ve web uygulamaları yayınlamasına izin vermek için tasarlanmıştır.. Veri bilimcilerin karmaşık çalışmalarından makine öğrenimi ve veri bilimi içgörülerini paylaşmayı ve karar vericilerin eline vermeyi kolaylaştırır. RStudio Connect ayrıca içeriği barındırmayı ve yönetmeyi basit ve geniş tüketim için ölçeklenebilir hale getirir.
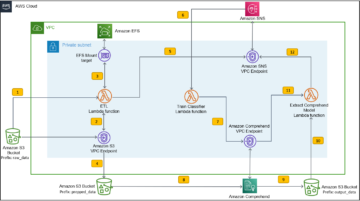
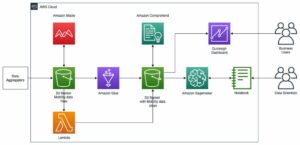
Çözüme genel bakış
Aşağıdaki bölümlerde, SageMaker'da RStudio'da uzak bir havuzdan veya S3 klasöründen ham verileri nasıl içe aktarabileceğimizi tartışıyoruz. Doğrudan bağlanmak da mümkündür Amazon İlişkisel Veritabanı Hizmeti (Amazon RDS) ve veri ambarları gibi Amazon Kırmızıya Kaydırma (görmek Amazon Redshift ile R'yi Bağlama) doğrudan RStudio'dan; ancak bu, bu yazının kapsamı dışındadır. Veriler birkaç farklı kaynaktan alındıktan sonra, onu işler ve bir tablo için R veri çerçeveleri oluştururuz. Ardından tablo veri çerçevesini bir RTF dosyasına dönüştürür ve sonuçları bir S3 kovasında saklarız. Gönderide kullanılan R paketlerinin müşteri tarafından düzenleyici gönderiler için kullanım için doğrulanmış olması koşuluyla, bu çıktılar daha sonra potansiyel olarak yasal gönderim amaçları için kullanılabilir.
SageMaker'da RStudio'yu kurun
Ortamınızda SageMaker üzerinde RStudio kurulumuna ilişkin talimatlar için bkz. SageMaker'da RStudio'yu kullanmaya başlayın. RStudio'nun SageMaker üzerindeki yürütme rolünün, verilerin depolandığı S3 kovasına veri indirme ve yükleme erişimi olduğundan emin olun. R paketlerini nasıl yöneteceğiniz ve analizinizi SageMaker üzerinde RStudio kullanarak nasıl yayınlayacağınız hakkında daha fazla bilgi edinmek için, bkz. Veri Bilimciler için SageMaker'da Tam Yönetilen RStudio Duyurusu.
Verileri RStudio'ya alın
Bu adımda, R oturumumuz için kullanılabilir hale getirmek için çeşitli kaynaklardan veri alıyoruz. Verileri SAS XPT formatında içe aktarıyoruz; ancak, verileri başka biçimlerde almak istiyorsanız işlem benzerdir. SageMaker'da RStudio kullanmanın avantajlarından biri, kaynak veriler AWS hesaplarınızda depolanıyorsa, SageMaker'ın verilere yerel olarak erişebilmesidir. AWS Kimlik ve Erişim Yönetimi (IAM) rolleri.
Uzak bir havuzda depolanan verilere erişin
Bu adımda, ADaM verilerini şu sistemden içe aktarıyoruz: FDA'nın GitHub deposu. adlı yerel bir dizin oluşturuyoruz. data verileri depolamak ve demografik verileri indirmek için RStudio ortamında (dm.xpt) uzak depodan. Bu bağlamda yerel dizin, varsayılan olarak R oturum ortamınıza eklenen özel Amazon EFS depolama alanınızda oluşturulan bir dizine atıfta bulunur. Aşağıdaki koda bakın:
Bu adım tamamlandığında, görebilirsiniz dm.xpt adresine gidilerek indiriliyor dosyalar, veri, dm.xpt.
Amazon S3'te depolanan verilere erişin
Bu adımda, bir S3 kovasında saklanan verileri hesabımıza indiriyoruz. İçeriği FDA'nın GitHub deposundan S3 kovasına kopyaladık. aws-sagemaker-rstudio bu örnek için. Aşağıdaki koda bakın:
Adım tamamlandığında, görebilirsiniz pp.xpt adresine gidilerek indiriliyor dosyalar, veri, pp.xpt.
XPT verilerini işle
Artık R ortamında SAS XPT dosyalarımız olduğuna göre, bunları R veri çerçevelerine dönüştürmemiz ve işlememiz gerekiyor. kullanıyoruz haven XPT dosyalarını okumak için kütüphane. CDISC SDTM veri kümelerini birleştiriyoruz dm ve pp ADPP veri kümesi oluşturmak için. Ardından ADPP veri çerçevesini kullanarak bir özet istatistik tablosu oluşturuyoruz. Özet tablosu daha sonra RTF formatında dışa aktarılır.
İlk olarak, XPT dosyaları read_xpt cennet kütüphanesinin işlevi. Daha sonra, kullanılarak bir analiz veri seti oluşturulur. sqldf işlevi sqldf kütüphane. Aşağıdaki koda bakın:
Daha sonra, işlevler kullanılarak bir çıktı veri çerçevesi oluşturulur. Tplyr ve dplyr kütüphaneler:
Çıktı veri çerçevesi daha sonra RStudio ortamında çıktı klasöründe bir RTF dosyası olarak depolanır:
Çıktıları Amazon S3'e yükleyin
Çıktı oluşturulduktan sonra verileri bir S3 kovasına geri koyarız. Bunu, eğer bir oturum halihazırda aktif değilse, tekrar bir SageMaker oturumu oluşturarak ve çıktı klasörünün içeriğini aşağıdaki komutu kullanarak bir S3 kovasına yükleyerek başarabiliriz. session$upload_data işlevi:
Bu adımlarla verileri aldık, işledik ve düzenleyici makamlara sunulmak üzere kullanıma sunmak üzere sonuçları yükledik.
Temizlemek
İstenmeyen maliyetlere maruz kalmamak için mevcut oturumunuzdan çıkmanız gerekir. Sayfanın sağ üst köşesinde, güç simgesini seçin. Bu, temel alınan örneği otomatik olarak durduracak ve bu nedenle istenmeyen işlem maliyetlerine maruz kalmayı durduracaktır.
Zorluklar
Gönderi, bir S3 kovasında veya uzak bir depodan depolanan ham verileri almak için gereken adımları özetledi. Bununla birlikte, bir klinik araştırma için birçok başka ham veri kaynağı vardır, bunlar başta Oracle Clinical, Medidata Rave, OpenClinica veya Snowflake gibi EDC (elektronik veri yakalama) sistemlerinde depolanan eCRF (elektronik vaka raporu formları) verileridir; laboratuvar verileri; eCOA (klinik sonuç değerlendirmesi) ve ePRO'dan (elektronik Hasta Tarafından Raporlanan Sonuçlar) veriler; uygulamalardan ve tıbbi cihazlardan gerçek dünya verileri; ve hastanelerde elektronik sağlık kayıtları (EHR'ler). Bu verilerin düzenleyici başvurular için kullanılabilir hale getirilmesinden önce önemli bir ön işleme tabi tutulur. Çeşitli veri kaynaklarına bağlayıcılar oluşturmak ve bunları merkezi bir veri havuzunda (CDR) veya bir klinik veri gölünde toplamak, uygun erişim kontrollerini sürdürürken önemli zorluklar doğurur.
Üstesinden gelinmesi gereken bir diğer önemli zorluk, mevzuata uyum sorunudur. Düzenleyici gönderim çıktılarını oluşturmak için kullanılan bilgisayar sistemi, 21 CFR Bölüm 11, HIPAA, GDPR veya diğer GxP gereksinimleri veya ICH yönergeleri gibi uygun düzenlemelerle uyumlu olmalıdır. Bu, erişim, güvenlik, yedekleme ve denetlenebilirlik denetimlerinin yerinde olduğu doğrulanmış ve nitelikli bir ortamda çalışmak anlamına gelir. Bu aynı zamanda düzenleyici gönderim çıktıları oluşturmak için kullanılan tüm R paketlerinin kullanımdan önce doğrulanması gerektiği anlamına gelir.
Sonuç
Bu gönderide, bir eCTD gönderimi için bazı önemli çıktıların CDISC SDTM, ADaM veri kümeleri ve TLF olduğunu gördük. Bu gönderi, önce birkaç kaynaktan gelen verileri SageMaker'da RStudio'ya alarak bu düzenleyici gönderim çıktılarını oluşturmak için gereken adımları özetledi. Daha sonra alınan verileri XPT formatında nasıl işleyebileceğimizi gördük; SDTM, ADaM ve TLF oluşturmak için R veri çerçevelerine dönüştürün; ve son olarak sonuçları bir S3 kovasına yükleyin.
Gönderide ortaya konan geniş fikirlerle, istatistiksel programcıların ve biyoistatistikçilerin, klinik deney araştırma verilerini SageMaker'da RStudio'ya yükleme, işleme ve analiz etme sürecini uçtan uca kolayca görselleştirebileceğini ve öğrenmeleri bir özel tanımlama tanımlamak için kullanabileceğini umuyoruz. düzenleyici gönderileriniz için uygun iş akışı.
Araştırmacıların, istatistikçilerin ve R programcılarının hayatlarını kolaylaştırmalarına yardımcı olmak için RStudio kullanmanın başka uygulamalarını düşünebiliyor musunuz? Fikirlerinizi duymayı çok isteriz! Ve herhangi bir sorunuz varsa, lütfen bunları yorumlar bölümünde paylaşın.
Kaynaklar
Daha fazla bilgi için aşağıdaki bağlantıları ziyaret edin:
yazarlar hakkında
 Rohit Banga Londra, İngiltere merkezli bir Küresel Klinik Geliştirme Endüstrisi Uzmanıdır. Eğitim yoluyla bir biyoistatistikçidir ve Healthcare ve LifeScience müşterilerinin AWS'de yenilikçi klinik geliştirme çözümleri dağıtmasına yardımcı olur. Sağlık ve Yaşam Bilimi endüstrisindeki gerçek iş sorunlarını çözmek için veri bilimi, AI/ML ve gelişen teknolojilerin nasıl kullanılabileceği konusunda tutkulu. Rohit boş zamanlarında kayak yapmaktan, barbekü yapmaktan ve ailesi ve arkadaşlarıyla vakit geçirmekten hoşlanır.
Rohit Banga Londra, İngiltere merkezli bir Küresel Klinik Geliştirme Endüstrisi Uzmanıdır. Eğitim yoluyla bir biyoistatistikçidir ve Healthcare ve LifeScience müşterilerinin AWS'de yenilikçi klinik geliştirme çözümleri dağıtmasına yardımcı olur. Sağlık ve Yaşam Bilimi endüstrisindeki gerçek iş sorunlarını çözmek için veri bilimi, AI/ML ve gelişen teknolojilerin nasıl kullanılabileceği konusunda tutkulu. Rohit boş zamanlarında kayak yapmaktan, barbekü yapmaktan ve ailesi ve arkadaşlarıyla vakit geçirmekten hoşlanır.
 Georgios Şinas EMEA bölgesinde AI/ML için Uzman Çözüm Mimarıdır. Londra merkezlidir ve İngiltere ve İrlanda'daki müşterilerle yakın bir şekilde çalışmaktadır. Georgios, müşterilerin MLOps uygulamalarına özel bir ilgi duyarak AWS'de üretimde makine öğrenimi uygulamaları tasarlamasına ve dağıtmasına yardımcı olur ve müşterilerin büyük ölçekte makine öğrenimi gerçekleştirmesini sağlar. Boş zamanlarında seyahat etmekten, yemek yapmaktan ve arkadaşları ve ailesiyle vakit geçirmekten hoşlanır.
Georgios Şinas EMEA bölgesinde AI/ML için Uzman Çözüm Mimarıdır. Londra merkezlidir ve İngiltere ve İrlanda'daki müşterilerle yakın bir şekilde çalışmaktadır. Georgios, müşterilerin MLOps uygulamalarına özel bir ilgi duyarak AWS'de üretimde makine öğrenimi uygulamaları tasarlamasına ve dağıtmasına yardımcı olur ve müşterilerin büyük ölçekte makine öğrenimi gerçekleştirmesini sağlar. Boş zamanlarında seyahat etmekten, yemek yapmaktan ve arkadaşları ve ailesiyle vakit geçirmekten hoşlanır.
- AI
- yapay zeka
- AI sanat üreteci
- yapay zeka robotu
- Amazon Adaçayı Yapıcı
- Amazon Basit Depolama Hizmeti (S3)
- yapay zeka
- yapay zeka sertifikası
- bankacılıkta yapay zeka
- yapay zeka robotu
- yapay zeka robotları
- yapay zeka yazılımı
- AWS Makine Öğrenimi
- blockchain
- blockchain konferans ai
- zeka
- konuşma yapay zekası
- kripto konferans ai
- dal-e
- derin öğrenme
- google ai
- Orta (200)
- Yaşam Bilimleri
- makine öğrenme
- Platon
- plato yapay zekası
- Plato Veri Zekası
- Plato Oyunu
- PlatoVeri
- plato oyunu
- ölçek ai
- sözdizimi
- zefirnet