Beyin fonksiyonunda ilerleyici bir kayıpla karakterize edilen nörodejeneratif hastalıklar, öncelikle merkezi sinir sistemindeki sinaptik kayıp ve nöronal hücre ölümünden kaynaklanır. Alzheimer hastalığı (AD) tartışmasız demansa yol açan en yaygın nörodejeneratif hastalıktır.
Tedavilerin eksiklikleri, bilim adamlarının Alzheimer hastalığının nasıl geliştiğini hiçbir zaman tam olarak anlayamadıklarını yansıtıyor. Bilim insanları ayrıca neden kadınların vakaların yaklaşık üçte ikisini oluşturduğunu da bilmiyor.
Araştırmacılar İLE ve Scripps Araştırma Alzheimer hastalığının moleküler etiyolojisine dair bir ipucu keşfettik; Bu ipucu aynı zamanda kadınların neden hastalığa daha duyarlı olduğunu da açıklayabilir.
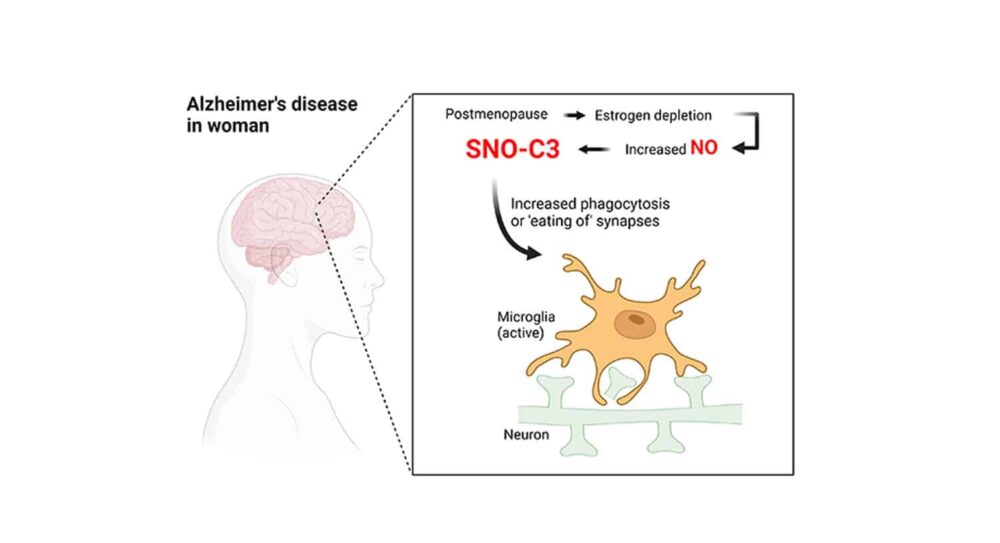
Araştırmacılar, hastalıktan ölen kadınların beyinlerinde, hastalıktan ölen erkeklere kıyasla, kompleman C3 adı verilen inflamatuar bir bağışıklık proteininin özellikle zararlı, kimyasal olarak değiştirilmiş bir formunun çok daha yüksek seviyelerde mevcut olduğunu keşfettiler. Bunu da gösterdiler östrojen— üretim sırasında düşenler menopoz—tipik olarak tamamlayıcı C3'ün bu formunun oluşmasına karşı koruma sağlar.
Çalışmanın kıdemli yazarı Stuart Lipton, MD, Ph.D., profesör ve Step Family Foundation Vakfı Scripps Research Moleküler Tıp Bölümü Başkanı ve La Jolla, Kaliforniya'da klinik nörolog şunları söyledi: "Yeni bulgularımız, tamamlayıcı sistemin bir bileşenindeki kimyasal modifikasyonun Alzheimer'ı tetiklemeye yardımcı olduğunu ve hastalığın neden ağırlıklı olarak kadınları etkilediğini en azından kısmen açıklayabileceğini gösteriyor."
Lipton'un laboratuvarı, kompleman C3'ün değiştirilmiş bir versiyonuyla sonuçlanan protein S-nitrosilasyonu gibi biyokimyasal ve moleküler süreçleri araştırıyor. nörodejeneratif hastalıklar. Nitrik oksit (NO) ile ilgili bir molekül, proteinlerin belirli bir amino asit yapı bloğundaki bir kükürt atomuna (S) güvenli bir şekilde bağlandığında değiştirilmiş bir "SNO-proteini" üreten bu kimyasal işlem, ilk olarak Lipton ve iş arkadaşları tarafından bulundu. .
NO gibi küçük atom kümeleri sıklıkla değişime uğrar. hücrelerdeki proteinler. Bu değişiklikler tipik olarak hedef proteinin fonksiyonlarını etkinleştirir veya devre dışı bırakır. Teknik zorluklardan dolayı S-nitrosilasyon diğer protein modifikasyonlarına göre daha az ilgi görmüştür. Yine de Lipton, bu proteinlerin "SNO fırtınalarının" Alzheimer hastalığı ve diğer nörodejeneratif hastalıkların gelişiminde önemli bir rol oynayabileceğini öne sürüyor.
Lipton'un laboratuvarı, nörodejeneratif bozuklukların nedeni olabilecek kompleman C3'ün değiştirilmiş bir versiyonuyla sonuçlanan protein S-nitrosilasyonu gibi biyokimyasal ve moleküler süreçleri araştırıyor. Nitrik oksit (NO) ile ilgili bir molekül, proteinlerin belirli bir amino asit yapı bloğundaki bir kükürt atomuna (S) güvenli bir şekilde bağlandığında değiştirilmiş bir "SNO-proteini" üreten bu kimyasal işlem, ilk olarak Lipton ve iş arkadaşları tarafından bulundu. .
NO gibi küçük atom kümeleri sıklıkla hücrelerdeki proteinleri değiştirir. Bu değişiklikler tipik olarak hedef proteinin fonksiyonlarını etkinleştirir veya devre dışı bırakır. Teknik zorluklardan dolayı S-nitrosilasyon diğer protein modifikasyonlarına göre daha az ilgi görmüştür. Yine de Lipton, bu proteinlerin "SNO fırtınalarının" Alzheimer hastalığı ve diğer nörodejeneratif hastalıkların gelişiminde önemli bir rol oynayabileceğini öne sürüyor.
Son çalışmada bilim insanları, S-nitrosilasyonu tanımlamak için yepyeni teknikler kullanarak ölüm sonrası 40 insan beyninde değişen protein miktarını ölçtüler. Beyinler erkekler ve kadınlar arasında eşit olarak paylaştırıldı; yarısı Alzheimer hastalığından ölen kişilerden, diğer yarısı da Alzheimer hastalığından ölmeyen kişilerden geldi.
Araştırmacılar bu beyinlerde S-nitrosile edilmiş 1,449 farklı protein keşfettiler. Alzheimer hastalığıyla bağlantılı olan çok sayıda protein, kompleman C3 de dahil olmak üzere en sık değiştirilenler arasındaydı. Şaşırtıcı bir şekilde, kadın Alzheimer beyinleri, erkek Alzheimer beyinlerine göre altı kat daha yüksek S-nitrosillenmiş C3 (SNO-C3) seviyelerine sahipti.
Kompleman sistemi insanın evrimsel olarak daha eski bir parçasıdır bağışıklık sistemi. "Tamamlayıcı kaskadında" iltihaplanmayı tetiklemek için birbirini aktive edebilen, C3 de dahil olmak üzere bir protein ailesinden oluşur.
30 yılı aşkın bir süredir araştırmacılar, nörolojik açıdan sağlıklı beyinlerle karşılaştırıldığında Alzheimer beyinlerinin daha yüksek miktarlarda tamamlayıcı proteinler ve diğer inflamatuar göstergeler sergilediğini biliyorlar. Daha yeni çalışmalar, özellikle tamamlayıcı proteinlerin, mikroglia olarak bilinen beyinde yerleşik bağışıklık hücrelerinin sinapsları bozmasına nasıl neden olabileceğini gösterdi. Bu kavşaklarda nöronlar birbirleriyle iletişim kurar.
Pek çok araştırmacı artık bu sinapsları yok eden mekanizmanın kısmen Alzheimer hastalığının altında yattığından şüpheleniyor. Sinaps kaybının Alzheimer'lı beyinlerdeki bilişsel gerilemeyle önemli bir ilişkisi olduğu kanıtlandı.
Neden Alzheimer hastası kadın beyinlerinde SNO-C3 prevalansı daha yüksek olsun ki? Araştırmacılar, östrojenin kadınların beynini C3 S-nitrosilasyondan koruduğu ve menopozla birlikte östrojen düzeyleri keskin bir şekilde düştüğünde bu korumanın kaybolduğu hipotezini öne sürdüler. Kadınlık hormonu östrojenin bazı koşullar altında beyni koruyucu etkilere sahip olabileceğine dair uzun süredir kanıtlar bulunmaktadır. Bu teori, kültürlü insan kullanılarak yapılan deneylerle doğrulandı. beyin hücreleriBu, beyin hücrelerinde NO üreten bir enzimin aktive edilmesi nedeniyle östrojen (-östradiol) seviyeleri düştükçe SNO-C3'ün arttığını gösterdi. SNO-C3 seviyeleri yükseldiğinde sinapslar mikroglia tarafından yok edilir.
Lipton diyor, "Kadınların Alzheimer'a yakalanma olasılığının neden daha yüksek olduğu uzun zamandır bir gizemdi, ancak bence sonuçlarımız, kadınların yaşlandıkça artan savunmasızlığını mekanik olarak açıklayan bulmacanın önemli bir parçasını temsil ediyor."
Dergi Referans:
- Hongmei Yang, Chang-ki Oh, ve diğerleri. Alzheimer hastalığında C3'ün anormal protein S-nitrosilasyonuna dayanan kadın baskınlığına dair mekanik anlayış. Bilim Gelişmeler. DOI: 10.1126/sciadv.ade0764