Кібератаки на лікарні можуть мати руйнівний вплив, особливо на відділення радіології та променевої терапії, функціонування яких особливо залежить від технологій. Яскравим прикладом є загальнонаціональна кібератака на служби охорони здоров’я Ірландії в травні 2021 року, яка призвела до переривання планової променевої терапії для деяких хворих на рак на термін до 12 днів.
Після цього випадку медичні фізики в Університетська лікарня Голвей і Національний університет Ірландії Голвей почали розробляти власний інструмент, який допоможе створити переглянуті плани лікування променевою терапією після перерв. Інструмент – під назвою EQD2VH – розраховує плани компенсації лікування та дозволяє візуально порівнювати всі варіанти плану, а також індивідуальний аналіз кожної структури в плані пацієнта. Дослідники описують новий програмний інструмент у Журнал прикладної клінічної медичної фізики.
Променева терапія найчастіше проводиться протягом кількох тижнів серією малих доз опромінення (зазвичай 2 Гр), які називаються фракціями. Незаплановані перерви в лікуванні – через кібератаки, поломку обладнання чи хворобу пацієнта – можуть спричинити значні невдачі. Під час таких розривів ракові клітини швидко відновлюють пухлинну тканину, що призводить до зниження радіобіологічної дози до планового цільового об’єму (PTV).

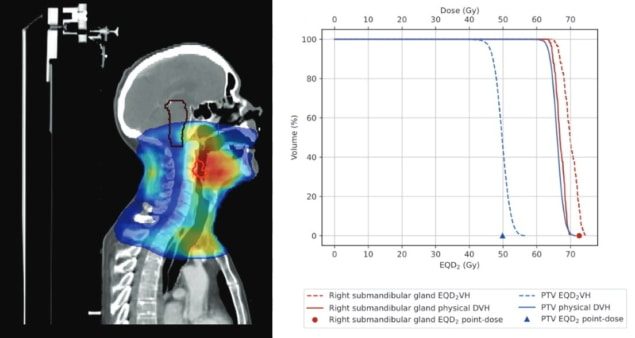
Щоб вирішити цю проблему, EQD2VH використовує інформацію гістограми «доза-об’єм» (DVH), отриману з оригінальних планів пацієнтів, щоб виконати обчислення проміжків у лікуванні. Провідний автор Кеті О’Ші з Національного університету Ірландії в Голуеї та її колеги пояснюють, що програмне забезпечення перетворює фізичну дозу в кожному дозаторі (діапазон доз між точками даних у DVH) у біологічно ефективну дозу (BED). Це пояснює як ефекти репопуляції в PTV, так і ефекти сублетального пошкодження невідновленої нормальної тканини в органах ризику (OARs).
Після модифікації перетворення BED для врахування коливань дози в кожній структурі, використовуючи метод змінної дози, інструмент перетворює BED для кожної структури в еквівалентну дозу у фракціях 2 Гр (EQD2). Це нормалізує кожну обробку до звичайного фракціонування та дає змогу сумувати плани з різними схемами фракціонування. Результат EQD2 DVH на основі DVH надає двовимірне представлення впливу стратегій компенсації розриву лікування на розподіл дози як PTV, так і OAR у порівнянні з призначеним планом лікування.
Щоб оцінити EQD2В якості клінічного інструменту прийняття рішень дослідники відібрали п’ять пацієнтів із високим пріоритетом із швидко зростаючими пухлинами, перерви в лікуванні яких не повинні перевищувати двох днів. Це включало чотирьох пацієнтів із раком голови та шиї, які проходили променеву терапію з модуляцією інтенсивності, і одного пацієнта з раком легенів, який проходив 3D конформну променеву терапію, у якого були перерви в лікуванні 12 або 13 днів. Ці випадки дозволили команді оцінити використання EQD2VH для пацієнтів як із звичайним (2 Гр), так і з нетрадиційним (2.2 Гр) фракціонуванням і різним часом перерви в лікуванні (від дев’яти до 46 днів терапії).
Переглянуті плани лікування для кожного пацієнта базувалися на їхніх початкових планах із зміною дози на фракцію або кількості фракцій. О’Ші пояснює, що у переглянутому плані та розкладі кожного пацієнта використовувалася комбінація фракціонування двічі на день, лікування у вихідні дні та збільшення дози до цільового об’єму, щоб зменшити наслідки репопуляції клітин.
Плани обмежували лікування шістьма фракціями на тиждень і виключали фракціонування двічі на день у послідовні дні. Якщо призначене лікування не можна було завершити в необхідні терміни, дослідники досліджували плани з використанням гіпофракціонування (доставка збільшеної дози на фракцію). Вони змогли візуально та кількісно порівняти різні переглянуті плани з початковим планом пацієнта, щоб визначити, який доставлятиме найкращу дозу для PTV і найменшу дозу для ОАР.
Дослідники відзначають, що 2D представлення кожної окремої структури в EQD2VH забезпечує більш глибокий аналіз, ніж рекомендований Королівським коледжем радіологів (RCR) одновимірний метод розрахунку точкової дози, який зараз використовується для усунення прогалин у променевій терапії. Одновимірне представлення розподілу дози в об’ємі не враховує OAR, які зазвичай мають нерівномірний розподіл дози, і можуть переоцінити дозу OAR. Крім того, EQD2Інструмент VH може створювати плани для будь-якої тривалості перерви в лікуванні, тоді як рекомендації RCR базуються на стандартній перерві в чотири-п’ять днів.
Додаткові переваги нового інструменту включають можливість моніторингу кожного OAR у плані пацієнта, щоб мінімізувати подальше збільшення дози, яке може спричинити більш гостру токсичність. Користувачі також можуть розрахувати вплив різної тривалості перерви в лікуванні на лікування пацієнта. Ця можливість може допомогти визначити, чи потрібно переводити пацієнта в іншу клініку, якщо перерва в запланованій клініці занадто довгий, або чи може пацієнт безпечно чекати відновлення лікування.

Як COVID-19 вплинув на надання променевої терапії?
EQD2VH також може пояснити зміни загального часу лікування та сублетальне пошкодження нормальної тканини, чого комерційна система може бути не в змозі зробити. Найважливіше те, що інструмент не потребує підключення до лікарняної мережі, щоб працювати – його можна використовувати, навіть якщо сервери лікарні все ще пошкоджені кібератакою.
«Ми все ще оцінюємо EQD2VH як інструмент прийняття рішень», – каже головний дослідник Маргарет Мур з університетської лікарні Голуей. «Це частина поточного проекту, який розглядає пацієнтів, які отримують багаторазове повторне лікування для паліативних режимів, де доза на фракцію є нестандартною та де може бути вибір схем фракціонування для розгляду. Перетворення лікувальної дози з кількох процедур із різним фракціонуванням на EQD2 дозволяє накопичувати радіобіологічну дозу для цільових тканин і ОАР для загального огляду дози, що може допомогти у прийнятті рішення щодо вибору подальшого лікування».