Протонна терапія може забезпечити висококонформний розподіл дози на мішень пухлини, мінімізуючи дозу на тканини за межами цільового об’єму. Створення планів лікування, які реалізують цю силу, є головним пріоритетом для дозиметристів і медичних фізиків.
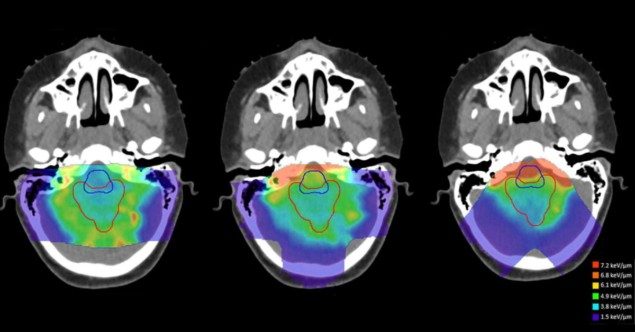
Протони накопичують дозу принципово інакше, ніж рентгенівське випромінювання, інший тип променевої терапії із зовнішнім променем. Коли протон досягає кінця своєї траєкторії, швидкість, з якою його енергія передається тканині – його лінійна передача енергії (LET), виражена в кеВ/мкм – зростає.
Відносна біологічна ефективність (RBE) відображає біологічні наслідки підвищення LET, і фіксоване значення RBE 1.1 часто застосовується для клінічного лікування протонами. Але протонний RBE залежить від багатьох інших факторів, включаючи клінічні кінцеві точки, тип тканини, схему фракціонування, індивідуальну радіочутливість пацієнта, фізичну дозу та невизначеності в експериментальних вимірюваннях. У результаті використання фіксованого значення RBE у протонній терапії, ймовірно, недооцінює RBE у місцях з високим LET, що може призвести до підвищеного ризику токсичності, спричиненої радіацією.
Тим не менш, LET сильно корелює з RBE і є ключовим фактором для визначення змінної RBE в протонній терапії. Таким чином, дослідники досліджують підходи до розрахунку та оцінки LET під час планування лікування. Однак ці інструменти планування біологічного лікування обмежені, і поки вони не будуть розроблені та вивчені далі, клініки повинні визначити власні практики планування лікування, щоб мінімізувати LET за межами цільових обсягів, каже Остін Фот, медичний фізик в Дитяча дослідницька лікарня Святого Іуди в штаті Теннессі.
«Як вплинути на [розподіл LET] — це активна область досліджень, і є кілька чудових методів, які розробляються», — пояснює Фот. «Проблема, з якою ми стикаємося, полягає в тому, що вони недоступні без спеціального програмного забезпечення, розробленого власними силами або за допомогою спеціальних дослідницьких версій додатків, наданих постачальниками... [і є] кілька досліджень, які дають кількісні вказівки щодо того, до чого ми повинні прагнути».
Стратегії планування лікування
На шляху до оцінки та оптимізації плану на основі LET для фотонної терапії Фаут і його команда провели огляд стратегій планування, які є комерційно доступними для клінічних груп для протонної терапії з модуляцією інтенсивності (IMPT). Про їх дослідження повідомили в Журнал прикладної клінічної медичної фізики, представляє деякі вказівки для планувальників лікування протонною терапією. «Ми хотіли розглянути деякі легкодоступні методи планування лікування та те, як вони можуть вплинути на LET», — пояснює Фот.
Дослідники оцінили відмінності в LET, зважених за дозою (LETd) між вісьмома перспективними підходами до планування лікування, застосованими до циліндричного водяного фантома та чотирьох педіатричних випадків пухлини головного мозку (Фоут зазначає, що токсичність, спричинена радіацією, є основною темою для команди). Вони порівняли ці стратегії планування з планом із використанням протилежних бічних пучків (для фантома) або з оригінальним клінічним планом (для пацієнтів), використовуючи вторинні розрахунки Монте-Карло для оцінки як дози, так і LETd.
Дослідники виявили, що геометрія поля лікування найбільше вплинула на розташування зон з високим ЛПТ. Щоб пом’якшити потенційний вплив біологічної невизначеності, пов’язаної з високим LETd, вони пропонують, щоб планувальники лікування використовували великі кути перетину між лікувальними променями та уникали пучків, які зупиняються безпосередньо поблизу критичних структур.
«Це чудова новина, оскільки це означає, що ретельний вибір кількості полів лікування та їх орієнтація щодо сусідніх здорових тканин може бути ефективним», — каже Фот. «З деякими свідомими, попередніми думками, це те, що всі планувальники лікування можуть взяти до уваги під час процесу планування».
Дослідники також виявили, що використання перемикача діапазону значно зменшує середнє значення LETd в клінічному цільовому обсязі. У зв’язку з цим вони рекомендують економно використовувати перемикачі діапазону та альтернативні стратегії обмеження точкового розміщення, і лише тоді, коли клініки можуть розрахувати кінцевий LETd для оцінки порівняно з альтернативними стратегіями планування.
Через малий розмір вибірки дослідники не змогли встановити чітку тенденцію в LETd варіації в клінічних випадках. Вони не оцінювали взаємозв'язок між змінами LET і зміною ймовірності контролю пухлини або нормальних тканинних ускладнень.
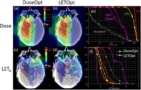
Плани на основі LET оптимізують протонну терапію
Хоча вплив кожного підходу планування на регіони з високим LET був скромним, Фоут каже, що важливо визнати, що стратегії планування лікування та рекомендації команди базуються на доказах і можуть бути легко використані в клінічній практиці.
«Я сподіваюся, що одним із висновків є те, що ми, як галузь, скористаємося комерційними інструментами, які дозволяють розраховувати LET у системі планування лікування. Ще краще, ми хотіли б мати способи оптимізації з урахуванням LET. Це дослідження було хорошим мостом, поки ці інструменти не стануть більш доступними», — каже Фот.