Здатність об’єднати електроніку та оптичні датчики з людським тілом на рівні однієї клітини може одного разу забезпечити дистанційний моніторинг і контроль окремих клітин у реальному часі. Досягнення у виробництві електроніки зробили можливим створення транзисторів і датчиків із нанорозмірною роздільною здатністю, а інноваційні методи створення нанопаттернів дозволяють збирати ці пристрої на гнучких підкладках. Однак такі процеси, як правило, вимагають агресивних хімікатів, високих температур або вакуумних методів, які непридатні для живих клітин і тканин.
Щоб подолати ці перешкоди, дослідницька група з Університету Джона Хопкінса розробила нетоксичний, високороздільний і економічно ефективний процес друку золотих нановізерунків на живих тканинах і клітинах. Повідомляючи про свої висновки в Нано листи, вони демонструють, що нова техніка може «татуювати» живі клітини та тканини гнучкими масивами золотих наноточок і нанодротів. Зрештою, цей метод може бути використаний для інтеграції розумних пристроїв із живою тканиною для таких програм, як біоніка та біосенсор.
«Якби у нас були технології для відстеження здоров’я ізольованих клітин, ми могли б діагностувати та лікувати захворювання набагато раніше, а не чекати, поки весь орган буде пошкоджено», — пояснює керівник групи. Девід Грасіас у заяві для преси. «Ми говоримо про нанесення чогось на зразок електронного татуювання на живий об’єкт, розмір якого в десятки разів менший за головку шпильки. Це перший крок до прикріплення датчиків та електроніки до живих клітин».
Спасибі, Ло Гу і його колеги розробили триетапний процес нанотрансферного друку для прикріплення золотих нановізерунків до живих клітин. На першому етапі вони використовували звичайну наноімпринт-літографію (NIL), щоб надрукувати масиви золотих наноточок або нанодротів на кремнієві пластини з полімерним покриттям. Потім вони розчинили полімер, звільнивши наноматриці для перенесення на скляні покривні скельця.
Далі дослідники функціоналізували поверхню золота цистеаміном і покрили золоті NIL-матриці шаром перенесення альгінатного гідрогелю. Вони показали, що цей підхід може надійно перенести масиви наноточок і нанодротів розміром 8 × 8 мм зі скла на м’які та гнучкі гідрогелі. На останньому етапі золоті NIL-матриці кон’югують з желатином, щоб забезпечити їх перенесення на живі клітини або тканини. Відокремлення шару перенесення гідрогелю відкриває золотий малюнок.
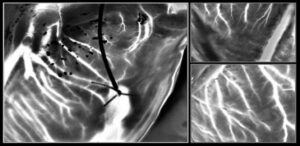
Дослідники досліджували поведінку живих клітин фібробластів, посіяних на масиви золотих точок діаметром 250 нм (відстань від центру до центру 550 нм) або золотих дротів шириною 300 нм (відстань 450 нм) на альгінатних гідрогелях. Приблизно через 24 години після посіву клітини на гідрогелі, надрукованому на нанодротах, переважно мігрували паралельно нанодротам, тоді як клітини на наноточках демонстрували випадкову, але трохи швидшу міграцію. Клітини на нанодротах також показали приблизно вдвічі більше видовження, ніж клітини на наноточках. Ці відкриття демонструють здатність золотих NIL-матриць керувати орієнтацією та міграцією клітин.
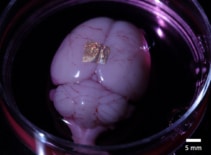
Крім біосумісності з клітинами та тканинами, альгінатний гідрогель також може переносити золоті NIL-матриці на живі органи та клітини. Щоб продемонструвати це, дослідники розташували гідрогелі, надруковані на нанодротах, на корі головного мозку цілого мозку та його коронального зрізу.
Після 2 годин у культуральному середовищі та дисоціації гідрогелю нанонитки залишалися приєднаними до поверхні всього мозку. Навпаки, нанодроти на зрізі мозку не прилипли, що свідчить про те, що сила адгезії різна для різних типів клітин і методів культивування. Дослідники відзначають, що необхідні подальші дослідження, щоб охарактеризувати та оптимізувати механізми адгезії для міцного довгострокового з’єднання.
Нарешті, щоб оцінити біотрансферний друк на рівні однієї клітини, дослідники культивували моношарові клітинні листи на альгінатних гідрогелях, надрукованих золотим NIL-матрицею. Через 24 години вони перевернули засіяні фібробластами гідрогелі на покривні скельця, вкриті желатином, і дали клітинам прикріпитися до покривних скель протягом ночі.
Після дисоціації альгінатного гідрогелю флуоресцентна мікроскопія показала, що фібробласти з візерунком із золотими наноточками мали життєздатність приблизно 97%, а фібробласти з візерунком з нанодротами мали життєздатність приблизно 98%, що вказує на те, що процес друку є біосумісний із живими клітинами. Світловідбиваючі кольори, які можна побачити на клітинному аркуші фібробластів з малюнком, свідчать про те, що форма золотого NIL-матриці була збережена.
Процес виготовлення також сумісний з мікромасштабною фотолітографією, яка дозволила дослідникам створити шестикутні та трикутні ділянки золотих NIL-матриць шириною 200 мкм. Потім вони біотрансфером надрукували їх на клітинних аркушах, що призвело до вибіркового росту клітин фібробластів на мікропатчах. Відео, записані протягом 16 годин, показали, що клітини з надрукованими нагорі ділянками нанодротів виглядають здоровими та здатними до міграції, причому масиви залишаються на м’яких клітинах, навіть коли вони рухаються.

Крихітний датчик одночасно вимірює електричну та механічну активність у клітинах серця
«Ми показали, що можемо прикріплювати складні наноматеріни до живих клітин, гарантуючи, що клітина не загине», — говорить Грасіас. «Це дуже важливий результат, що клітини можуть жити і рухатися разом з татуюваннями, оскільки часто існує значна несумісність між живими клітинами та методами, які інженери використовують для виготовлення електроніки».
Грасіас і його колеги дійшли висновку, що їхній процес створення нанопаттернів у поєднанні зі стандартними методами мікрофабрикації «відкриває можливості для розробки нових субстратів клітинних культур, біогібридних матеріалів, біонічних пристроїв і біосенсорів». Далі вони планують спробувати приєднати більш складні наносхеми, які можуть залишатися на місці довше, а також експериментувати з різними типами клітин.
- Розповсюдження контенту та PR на основі SEO. Отримайте посилення сьогодні.
- PlatoData.Network Vertical Generative Ai. Додайте собі сили. Доступ тут.
- PlatoAiStream. Web3 Intelligence. Розширення знань. Доступ тут.
- ПлатонЕСГ. Автомобільні / електромобілі, вуглець, CleanTech, Енергія, Навколишнє середовище, Сонячна, Поводження з відходами. Доступ тут.
- PlatoHealth. Розвідка про біотехнології та клінічні випробування. Доступ тут.
- ChartPrime. Розвивайте свою торгову гру за допомогою ChartPrime. Доступ тут.
- BlockOffsets. Модернізація екологічної компенсаційної власності. Доступ тут.
- джерело: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- : має
- :є
- : ні
- $UP
- 16
- 200
- 24
- 8
- a
- здатність
- Здатний
- МЕНЮ
- діяльність
- дотримуватися
- аванси
- після
- Також
- серед
- an
- та
- з'явився
- застосування
- підхід
- приблизно
- ЕСТЬ
- навколо
- масив
- AS
- збірка
- оцінити
- At
- приєднувати
- BE
- оскільки
- буття
- між
- тіло
- облігація
- Brain
- але
- CAN
- Клітини
- охарактеризувати
- клацання
- колеги
- комбінований
- сумісний
- комплекс
- укладає
- контрастність
- контроль
- звичайний
- рентабельним
- може
- створювати
- культура
- день
- демонструвати
- призначений
- розвиненою
- розробка
- прилади
- DID
- Померти
- різний
- хвороби
- Ні
- Раніше
- Electronic
- електроніка
- включіть
- включений
- Інженери
- забезпечення
- Весь
- Навіть
- Пояснює
- швидше
- остаточний
- результати
- Перший
- гнучкий
- для
- від
- далі
- GAO
- в цілому
- скло
- золото
- Зростання
- керівництво
- було
- Мати
- голова
- здоров'я
- здоровий
- Серце
- Високий
- висока роздільна здатність
- гопкінги
- Однак
- HTTPS
- людина
- зображення
- важливо
- in
- індивідуальний
- інформація
- інноваційний
- інтегрувати
- ізольований
- питання
- IT
- Johns
- Університет Джонса Хопкінса
- JPG
- шар
- лідер
- провідний
- дозволяти
- рівень
- як
- жити
- життя
- довгостроковий
- довше
- made
- Матеріали
- макс-ширина
- може бути
- заходи
- механічний
- механізми
- Медіа
- Злиття
- метод
- методика
- Мікроскопія
- мігрувати
- мігрували
- міграція
- моніторинг
- більше
- рухатися
- переїхав
- кіно
- багато
- необхідний
- Нові
- наступний
- об'єкт
- перешкодами
- of
- часто
- on
- ONE
- на
- відкрити
- Можливості
- Оптимізувати
- or
- над
- Подолати
- за ніч
- Паралельні
- Патчі
- Викрійки
- періодів
- Фізика
- Світ фізики
- місце
- план
- plato
- Інформація про дані Платона
- PlatoData
- розташовані
- це можливо
- press
- друк
- друк
- процес
- процеси
- Поклавши
- випадковий
- ЩУР
- реальний
- реального часу
- записаний
- залишився
- решті
- віддалений
- Звітність
- вимагати
- дослідження
- Дослідники
- дозвіл
- результат
- Показали
- міцний
- грубо
- говорить
- бачив
- селективний
- датчиків
- Форма
- лист
- показав
- показаний
- значний
- Кремній
- одночасно
- Скибочка
- менше
- розумний
- М'який
- що в сім'ї щось
- standard
- Заява
- залишатися
- Крок
- сила
- Дослідження
- такі
- пропонувати
- поверхню
- говорити
- команда
- методи
- Технології
- тензор
- ніж
- Що
- Команда
- їх
- потім
- Ці
- вони
- це
- ті
- слайдами
- час
- times
- до
- топ
- до
- трек
- переклад
- лікувати
- правда
- намагатися
- Двічі
- Типи
- Зрештою
- університет
- до
- використання
- використовуваний
- Вакуум
- дуже
- життєздатності
- чекати
- було
- we
- ДОБРЕ
- в той час як
- який
- в той час як
- всі
- широкий
- з
- світ
- зефірнет