Уявіть собі армію саморухомих частинок, покритих радіоізотопами, у 2500–10,000 XNUMX разів менших за порошинку, які після ін’єкції в організм шукають і прикріплюються до ракових пухлин, знищуючи їх. Звучить як наукова фантастика? Не так для мишей з раком сечового міхура.
Дослідники з Іспанії повідомляють, що наночастинки, які містять радіоактивний йод і які самі рухаються після реакції з сечовиною, мають здатність відрізняти ракові пухлини сечового міхура від здорових тканин. Ці «наноботи» проникають у позаклітинний матрикс пухлини та накопичуються в ньому, дозволяючи радіонуклідній терапії досягти своєї точної цілі. У дослідженні, проведеному в Інститут біоінженерії Каталонії (IBEC) у Барселоні, у мишей, які отримували одну дозу цього препарату, розмір пухлин сечового міхура зменшився на 90% порівняно з тваринами, які не отримували лікування.
Цей новий підхід одного разу може зробити революцію в лікуванні раку сечового міхура. За даними Глобальної онкологічної обсерваторії Всесвітньої організації охорони здоров’я, рак сечового міхура є десятим найпоширенішим видом раку у світі: у 600,000 році було діагностовано понад 2022 220,000 нових випадків і понад XNUMX XNUMX смертей у всьому світі.
Неінвазивний рак сечового міхура, на який припадає 75% випадків, в даний час лікується резекцією пухлини з наступною внутрішньоміхуровою ін’єкцією хіміотерапевтичних або імунотерапевтичних препаратів у сечовий міхур. Однак доставка ліків є особливо складною через низьку проникність уротелію (тканини, що вистилає внутрішню частину сечовивідних шляхів), заповнення вмістом сечі та подальше вимивання ліків. Процес також незручний для пацієнтів, оскільки їм потрібно час від часу повертати тіло, лежачи на животі, щоб препарати могли досягти всіх сторін стінки сечового міхура. Після лікування ризик рецидиву становить 30–70% протягом п’яти років.
Для покращення клінічних результатів, головний дослідник Самуель Санчес і його колеги прагнуть розробити інноваційні та ефективніші методи лікування раку сечового міхура, а також зменшити частоту рецидивів. Крім того, однодозова терапія значно знизила б вартість лікування, яке наразі вимагає від шести до 14 госпіталізацій.
Команда створила наноботів із наночастинок мезопористого кремнезему з різними функціональними компонентами на їх поверхні. До них належать радіоізотопи для візуалізації ПЕТ або радіонуклідної терапії та білок уреаза, який реагує з сечовиною в сечі та забезпечує рух нанобота.
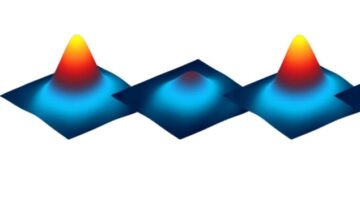
Введення в Природа нанотехнології, дослідники повідомляють, що коли вони додали краплю наноботів до розчину, що містить 300 мМ сечовини, наноботи демонстрували роїться рух, утворюючи активні та енергійні фронти та тривимірні вихори. Без сечовини наноботи просто осідали біля місця додавання.
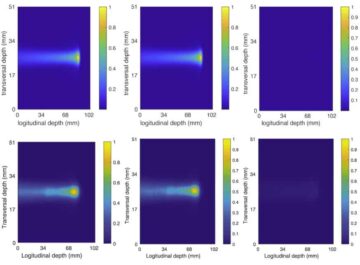
Щоб перевірити, чи можуть наноботи дістатися до пухлини в природних умовах, команда оцінила їхню поведінку у мишей із пухлиною. Зображення позитронно-емісійної томографії (ПЕТ) показали, що сигнали від мічених радіоактивним ізотопом наноботів були розташовані разом із положенням пухлини, визначеним за допомогою МРТ, причому радіоактивність в основному спостерігалася в місці цільової пухлини. Лише миші, яким вводили наноботів плюс сечовину, показали значне накопичення в масі пухлини – наноботи, доставлені у воді, і контрольні наночастинки (без уреази), доставлені у воді або сечовині, продемонстрували мінімальне поглинання пухлиною.
Дослідники припускають, що рухливість наноботів допомагає їм проникати в пухлинну масу. «Наноботам не вистачає специфічних антитіл для розпізнавання пухлини, а тканина пухлини, як правило, жорсткіша за здорову тканину, але це не так у пухлинах сечового міхура», — пояснює один із авторів. Меріксель Серра Касабланкас IBEC. «Ми помітили, що ці нанороботи можуть руйнувати позаклітинний матрикс пухлини, локально підвищуючи рН за допомогою хімічної реакції, що саморушиться. Це явище сприяло більшому проникненню пухлини». Дослідники вважають, що наноботи стикаються з уротелієм, ніби це стіна, але проникають у пухлину, яка є більш губчастою.
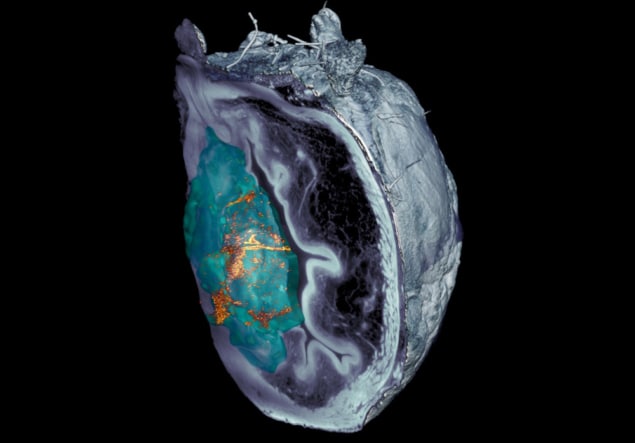
Команда зазначає, що ідентифікувати наноботів на мікроскопічних зображеннях розрізаної тканини було складно. Після того, як методи конфокальної оптичної мікроскопії зазнали невдачі, дослідники з ІРБ Барселона розробив систему мікроскопії на основі світлового аркуша, засновану на планарному лазерному освітленні, здатну сканувати різні шари сечового міхура та створювати 3D-реконструкцію всього органу.
«Система мікроскопії розсіяного еластичного світлового листа, яку ми розробили, дозволила нам усунути світло, відбите самою пухлиною, що дозволило нам ідентифікувати та локалізувати наночастинки в органі без попереднього маркування з безпрецедентною роздільною здатністю», — говорить Жульєн Коломбеллі від IRB Barcelona.

Сконструйовані бактерії приваблюють у пухлини радіоізотопи, які вбивають рак
Щоб оцінити терапевтичний ефект техніки, команда позначила наноботів йодом-131 (131I, радіоізотоп, який зазвичай використовують для радіонуклідної терапії), і вводив їх мишам із пухлиною. Лікування втраченими дозами 131I-наноботи в сечовині зупиняли ріст пухлини, при цьому високі дози 131I-nanobots, введені в сечовині, призвели до зменшення обсягу пухлини майже на 90% порівняно з тваринами, які не отримували лікування.
Розповідає Санчес Світ фізики що наступними кроками команди є інкапсуляція малих ліків, які зараз використовуються в хіміотерапії, і продовження перевірки ефективності наноботів як носіїв ліків. Зрештою вони мають намір розширити масштаби наноботів і вивчити регулятивні шляхи, щоб перейти до перших клінічних випробувань протягом наступних трьох-чотирьох років за допомогою додаткового продукту IBEC Наноботи Therapeutics.
- Розповсюдження контенту та PR на основі SEO. Отримайте посилення сьогодні.
- PlatoData.Network Vertical Generative Ai. Додайте собі сили. Доступ тут.
- PlatoAiStream. Web3 Intelligence. Розширення знань. Доступ тут.
- ПлатонЕСГ. вуглець, CleanTech, Енергія, Навколишнє середовище, Сонячна, Поводження з відходами. Доступ тут.
- PlatoHealth. Розвідка про біотехнології та клінічні випробування. Доступ тут.
- джерело: https://physicsworld.com/a/self-propelling-nanobots-shrink-bladder-tumours-in-mice-by-90/
- :є
- : ні
- $UP
- 000
- 10
- 135
- 14
- 2022
- 220
- 300
- 3d
- 600
- a
- здатність
- За
- Рахунки
- Накопичуватися
- накопичення
- активний
- доданий
- доповнення
- Додатково
- вводити
- після
- мета
- ВСІ
- Дозволити
- Також
- an
- та
- тварини
- підхід
- ЕСТЬ
- армія
- арештований
- AS
- оцінюється
- At
- приєднувати
- залучати
- автор
- Бактерії
- Барселона
- заснований
- поведінку
- Вірити
- між
- органів
- тіло
- Перерва
- але
- by
- CAN
- рак
- здатний
- носіїв
- випадок
- випадків
- складні
- хімічний
- Клінічний
- клінічні випробування
- колеги
- Зіткнення
- COM
- загальний
- зазвичай
- порівняний
- Компоненти
- проводиться
- зміст
- продовжувати
- контроль
- Коштувати
- створений
- створення
- В даний час
- день
- смерть
- поставляється
- доставка
- певний
- розвивати
- розвиненою
- різний
- розрізняти
- доза
- вниз
- наркотик
- Наркотики
- два
- Пилу
- ефект
- Ефективний
- ефективність
- усунутий
- випромінювання
- включіть
- включений
- дозволяє
- дозволяє
- Весь
- EU
- оцінювати
- врешті-решт
- досліджувати
- виставлені
- Пояснює
- не вдалося
- Художня література
- наповнення
- Перший
- п'ять
- потім
- після
- для
- чотири
- від
- функціональний
- Глобальний
- Глобально
- великий
- Зростання
- було
- Мати
- здоров'я
- здоровий
- допомагає
- Однак
- HTTPS
- ідентифікувати
- ідентифікує
- if
- зображень
- імунотерапія
- удосконалювати
- in
- включати
- зростаючий
- інформація
- інноваційний
- всередині
- мати намір
- в
- питання
- IT
- ЙОГО
- сам
- JPG
- маркування
- відсутність
- лазер
- шарів
- Led
- світло
- як
- підкладка
- локально
- низький
- Маса
- Матриця
- макс-ширина
- Може..
- Мікроскопія
- мінімальний
- мобільність
- більше
- найбільш
- рух
- рухатися
- МРТ
- природа
- Близько
- майже
- Необхідність
- Нові
- наступний
- увагу
- роман
- обсерваторії
- of
- on
- ONE
- тільки
- or
- Результати
- над
- особливо
- шляхів
- pacientes
- проникнення
- явище
- Фізика
- Світ фізики
- plato
- Інформація про дані Платона
- PlatoData
- плюс
- положення
- необхідність
- в першу чергу
- Головний
- попередній
- процес
- Пропел
- силова установка
- Білок
- ставки
- досягати
- реакція
- вступає в реакцію
- отримання
- визнати
- рецидив
- зменшити
- скорочення
- відображено
- регуляторні
- звітом
- Вимагається
- Дослідники
- дозвіл
- здійснити революцію
- Risk
- говорить
- шкала
- сканування
- розсіяний
- наука
- Наукова фантастика
- Пошук
- бачив
- показав
- Сторони
- сигнали
- істотно
- просто
- один
- сайт
- SIX
- Розмір
- невеликий
- менше
- So
- рішення
- звуки
- Іспанія
- конкретний
- заходи
- Вивчення
- наступні
- істотний
- пропонувати
- система
- Мета
- команда
- методи
- розповідає
- тест
- ніж
- Що
- Команда
- світ
- їх
- Їх
- самі
- терапія
- Ці
- вони
- це
- три
- тривимірний
- через
- по всьому
- слайдами
- times
- до
- до
- лікування
- лікування
- лікування
- випробування
- правда
- ПЕРЕГЛЯД
- типово
- безпрецедентний
- на
- поглинання
- us
- використовуваний
- різний
- через
- візуалізації
- обсяг
- Стіна
- було
- вода
- we
- були
- коли
- Чи
- який
- в той час як
- з
- в
- без
- світ
- б
- років
- зефірнет