امیونو تھراپی – کینسر سے لڑنے کے لیے جسم کے اپنے مدافعتی نظام کو استعمال کرنا – کینسر کی دیکھ بھال میں انقلاب لانے کی صلاحیت رکھتا ہے۔ لیکن جب خون کے کینسر جیسے لیوکیمیا اور لیمفوما کینسر کے امیونو تھراپی کا اچھا جواب دیتے ہیں، ٹھوس ٹیومر ایک محدود ردعمل ظاہر کرتے ہیں۔
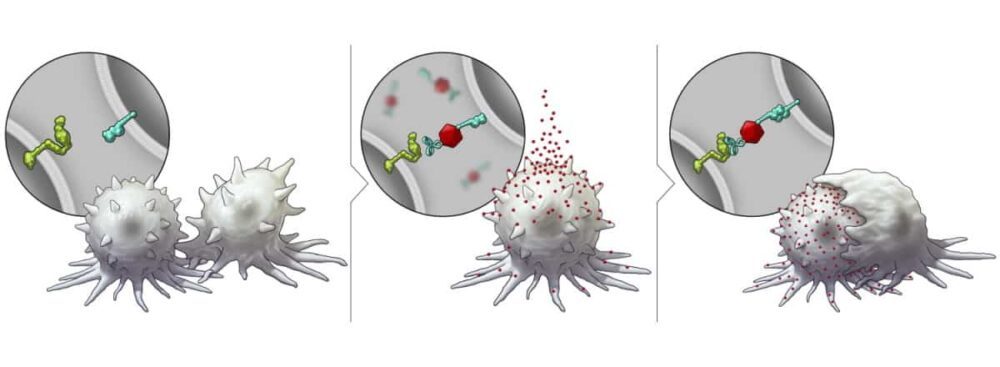
اس تفاوت کی ایک ممکنہ وجہ مختلف کینسروں میں سطحی پروٹین کا متنوع اظہار ہے۔ مثال کے طور پر، جھلی سے منسلک پروٹین SLAMF7 - جو مدافعتی نظام کو فعال کرتا ہے اور مدافعتی خلیوں کے ذریعے کینسر کے خلیات کے phagocytosis (Ingestion) کا اشارہ کرتا ہے - خون کے کینسر کے خلیوں سے ظاہر ہوتا ہے، لیکن ٹھوس ٹیومر سے نہیں۔
ٹیومر کے ٹھوس خلیوں کو امیونو تھراپی کے لیے زیادہ قابل قبول بنانے کے مقصد کے ساتھ، محققین یونیورسٹی آف ٹیکساس کے ایم ڈی اینڈرسن کینسر سینٹر۔ نے ایک نینو ٹیکنالوجی پلیٹ فارم تیار کیا ہے جو SLAMF7 کے اظہار کو متحرک کرتا ہے۔ میں بیان کیا گیا ہے۔ فطرت نانو، پلیٹ فارم بیسپیسیفک ٹیومر کو تبدیل کرنے والے نینو پارٹیکلز (BiTNs) پر مبنی ہے جس میں ایک پولیمرک کور شامل ہے جس میں ٹیومر کو نشانہ بنانے والے لیگنڈس اور SLAMF7 شامل ہیں۔
"اس نئے پلیٹ فارم کے ساتھ، اب ہمارے پاس ایک ٹھوس ٹیومر کو تبدیل کرنے کی حکمت عملی ہے، کم از کم امیونولوجیکل طور پر، ہیماتولوجیکل ٹیومر سے مشابہت رکھنے کے لیے، جس میں اکثر مدافعتی علاج کے لیے ردعمل کی شرح بہت زیادہ ہوتی ہے،" کہتے ہیں۔ وین جیانگ، جنہوں نے ساتھ ساتھ مطالعہ کی قیادت کی۔ بیٹی کم. "اگر ہم کلینک میں اس نقطہ نظر کا ترجمہ اور توثیق کرنے کے قابل ہیں، تو یہ ہمیں کینسر کے ساتھ مدافعتی ادویات سے زیادہ سے زیادہ سرگرمی کے قریب جانے کے قابل بنا سکتا ہے جنہوں نے روایتی طور پر اچھا جواب نہیں دیا ہے۔"
وٹرو میں اور vivo میں تشخیص
محققین نے پہلے پلیٹ فارم کی چھان بین کی۔ وٹرو میںHER2-مثبت چھاتی کے کینسر کے خلیات کا استعمال کرتے ہوئے. انہوں نے اس ایپلی کیشن کے لیے نینو پارٹیکلز کو اینٹی ایچ ای آر 2 اینٹی باڈیز کے ساتھ جوڑ کر ٹیومر کے خلیات سے منسلک کر کے اور SLAMF7 کو مدافعتی ردعمل کو چالو کرنے کے لیے سیل کے لیے مخصوص BiTN بنائے۔ نتیجے میں نانوکونجگیٹ - BiTNHER - منتخب طور پر HER2-مثبت چھاتی کے کینسر کے خلیوں کو نشانہ بنایا اور ان پر SLAMF7 کا لیبل لگا دیا۔
ٹیم نے تصدیق کی کہ بی ٹی اینHER- لیبل والے کینسر کے خلیوں نے غیر منسلک نینو پارٹیکلز کے مقابلے میں فاگوسائٹوسس کی اعلی سطح کو اکسایا۔ بی ٹی اینHER اس نے چھاتی کے کینسر کے خلیوں کو اینٹی CD47 اینٹی باڈی کے ساتھ علاج کے لیے بھی حساس بنایا، جو ٹیومر کے خلیات سے "مجھے مت کھاؤ" کے سگنل کو روکتا ہے، جس سے phagocytic سرگرمی میں مزید اضافہ ہوتا ہے۔
اگلا، ٹیم نے BiTN کا اندازہ کیا۔HER چھاتی کے کینسر کے ٹیومر والے چوہوں میں یا تو TUBO خلیات، جو HER2 کے چوہا ورژن کا اظہار کرتے ہیں، یا 4T1 خلیات جن میں اس رسیپٹر کی کمی ہے۔ BiTN کے ساتھ علاجHER نیز اینٹی CD47 نے ٹیومر کے بوجھ کو نمایاں طور پر کم کیا اور TUBO ٹیومر کے ساتھ چوہوں کی بقا کو طویل کیا؛ 4T1 ٹیومر میں اینٹی ٹیومر اثر نہیں دیکھا گیا۔
محققین نوٹ کرتے ہیں کہ مجموعہ علاج صرف BiTNs یا اینٹی CD47 کے مقابلے میں ٹیومر کی نمایاں روک تھام کا باعث بنا۔ ایک طویل مدتی زہریلا مطالعہ نے علاج نہ کیے جانے والے اور علاج شدہ چوہوں کے درمیان خون کی گنتی میں کوئی خاص فرق نہیں پایا۔
BiTN پلیٹ فارم کی استعداد کو ظاہر کرنے کے لیے، محققین نے نینو پارٹیکلز کو ایک اور ٹیومر ریسیپٹر کو نشانہ بنانے کے لیے اپنی مرضی کے مطابق بنایا - فولیٹ ریسیپٹر جس کا اظہار ٹرپل منفی چھاتی کے کینسر سے ہوتا ہے۔ انہوں نے BiTN بنایاFo اینٹی ایچ ای آر 2 اینٹی باڈی کو فولیٹ سے بدل کر۔ بی ٹی اینFo ٹارگٹڈ اور کینسر کے خلیوں کو SLAMF7 اظہار کرنے والے خلیوں میں تبدیل کر دیا گیا۔ جیسا کہ توقع کی گئی ہے، BiTN کے ساتھ 4T1 خلیوں کو انکیوبیٹ کرناFo اور اینٹی CD47 نے TUBO خلیوں کے مقابلے میں زیادہ فاگوسائٹوسس کا باعث بنا۔
"کیونکہ یہ انجینئرڈ تعمیرات ہیں، اس کو نینو پارٹیکل کی سطح پر مختلف ٹیومر کو نشانہ بنانے والے ایجنٹوں یا مدافعتی مالیکیولز کو شامل کرنے کے لیے پلگ اینڈ پلے اپروچ کے طور پر استعمال کیا جا سکتا ہے،" کم نے ایک پریس بیان میں کہا۔
محققین نے بی ٹی این کا بھی تجربہ کیا۔Fo ایک بے ساختہ 4T1 میٹاسٹیسیس ماؤس ماڈل میں، بنیادی ٹیومر کا بی ٹی این کے ساتھ علاجFo اور سرجیکل ریسیکشن سے پہلے اینٹی CD47۔ اس امتزاج نے مقامی بیماری کی تکرار کو روکا لیکن دور میٹاسٹیسیس کو کم نہیں کیا یا مجموعی طور پر بقا کو طول نہیں دیا۔ تاہم، علاج میں اینٹی پی ڈی 1 کو شامل کرنے سے، طویل مدتی میٹاسٹیسیس روکنا ہوا، جس میں سات میں سے دو چوہوں نے طویل مدتی ٹیومر سے پاک بقا کا مظاہرہ کیا۔
امیونو تھراپی کے علاوہ تابکاری کے پھٹنے سے چوہوں میں دماغی ٹیومر کا علاج ہوتا ہے۔
آخر میں، اس ماڈل کی ترجمہی مطابقت کو مزید بڑھانے کے لیے، ٹیم نے سرجری کے بعد کے علاج کے نظام کی چھان بین کی۔ یہاں، چوہوں میں ٹیومر کو بغیر کسی پیشگی علاج کے 12 ویں دن ریسیکٹ کیا گیا، اور پھر 15 ویں دن سے، جانوروں کا علاج BiTN کے ٹرپل مرکب سے کیا گیا۔Fo، اینٹی سی ڈی 47 اور اینٹی پی ڈی 1۔ آپریٹو کے بعد کے اس علاج نے میٹاسٹیسیس اور طویل بقا کو روکا - یہ ظاہر کرتا ہے کہ انٹراٹومورل علاج کے بغیر بھی، BiTNs ٹیومر کے بقایا خلیوں کو ختم کرنے اور نظامی بیماری کو کم کرنے میں مدد کر سکتے ہیں۔
اگلا، محققین کلینک میں اس نئی ٹیکنالوجی کا ترجمہ کرنے پر توجہ مرکوز کر رہے ہیں۔ "طبی ترجمہ کو آسان بنانے کے لیے، ہم ایک پروٹین پر مبنی حکمت عملی کی تلاش کر رہے ہیں جس میں ہم ایک مخصوص پروٹین تیار کریں گے جو BiTN کی طرح کام کر سکے،" جیانگ بتاتے ہیں۔ طبیعیات کی دنیا. "اس کے لیے کچھ پروٹین/اینٹی باڈی انجینئرنگ کی ضرورت ہوگی لیکن ممکنہ طور پر ریگولیٹری منظوریوں کو پورا کرنا آسان ہوگا۔"