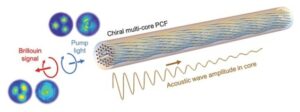
Các dịch bệnh lớn, bao gồm SARS, Zika và Ebola, và các đại dịch như H1N1 và COVID-19 đã bao trùm thế giới trong hai thập kỷ qua. Khi các đợt bùng phát bệnh truyền nhiễm xuất hiện với tần suất ngày càng tăng, nhu cầu mở rộng năng lực xét nghiệm chẩn đoán và giám sát vi rút để ngăn chặn dịch bệnh và ngăn chặn đại dịch ngày càng trở nên rõ ràng. Các nhà nghiên cứu dẫn đầu bởi khủng long di caro và Sam Emaminejad từ Đại học California, Los Angeles (UCLA) hiện đã phát triển một xét nghiệm chẩn đoán vi-rút cầm tay dựa trên một nhóm nam châm có kích thước milimet (được gọi là “ferrobots”). Công nghệ này có thể tăng đáng kể quy mô xét nghiệm bệnh, đồng thời giảm thiểu chi phí và sử dụng các nguồn cung cấp khan hiếm.
Mô tả bộ dụng cụ phòng thí nghiệm chẩn đoán trong Thiên nhiên, các nhà nghiên cứu phác thảo nguyên tắc hoạt động và khả năng thích ứng của nền tảng để xét nghiệm vi-rút tổng hợp và ghép kênh. Họ cũng báo cáo kết quả từ một nghiên cứu lâm sàng sử dụng các mẫu từ những người có triệu chứng COVID-19. So sánh kết quả xét nghiệm bằng cách sử dụng bộ dụng cụ phòng thí nghiệm với cùng các mẫu được xét nghiệm COVID-19 bằng xét nghiệm phản ứng chuỗi polymerase sao chép ngược (RT-PCR) tiêu chuẩn vàng cho thấy độ nhạy của xét nghiệm là 98% và độ đặc hiệu là 100%.
Khắc phục tình trạng thiếu nguồn cung và giảm chi phí
Trong số các lựa chọn xét nghiệm giám sát và chẩn đoán vi-rút, xét nghiệm khuếch đại axit nucleic (NAAT) cho thấy những ưu điểm rõ ràng so với xét nghiệm dựa trên kháng nguyên và kháng thể, về độ nhạy, độ đặc hiệu và khả năng cung cấp nhanh chóng mà không cần tạo kháng thể chẩn đoán cụ thể trước đó. Tuy nhiên, các nền tảng thử nghiệm dựa trên NAAT trước đây không thể thực hiện các quy trình xử lý, phân tích và phản hồi tự động tích hợp cần thiết để đạt được quy trình làm việc linh hoạt và tối đa hóa hiệu quả sàng lọc bệnh.
Để khắc phục sự thiếu hụt này, các nhà nghiên cứu của UCLA đã tạo ra một nền tảng lập trình dựa trên bảng mạch in có kích thước bằng lòng bàn tay, thực hiện các hoạt động xử lý chất lỏng và phân tích sinh học theo cách song song. Trái ngược với các phương pháp trước đây, vốn yêu cầu các công cụ cồng kềnh, sử dụng nhiều tài nguyên, nền tảng thu nhỏ giúp tiết kiệm chi phí đáng kể đối với nhiều mức độ phổ biến của virus, đồng thời mang lại độ chính xác cao, độ bền, khả năng thích ứng và khả năng mở rộng.
Emaminejad cho biết: “Công nghệ phòng thí nghiệm cầm tay của chúng tôi có thể giúp vượt qua một số rào cản về sự khan hiếm và khả năng tiếp cận các xét nghiệm, đặc biệt là giai đoạn đầu của đại dịch, khi điều quan trọng nhất là kiểm soát sự lây lan của dịch bệnh”. “Và ngoài khả năng giải quyết các vấn đề thiếu nguồn cung và nhu cầu cao, nó có thể được điều chỉnh rộng rãi để thử nghiệm nhiều loại bệnh trên thực địa và với chất lượng ở cấp độ phòng thí nghiệm.”
Chuyển sang thử nghiệm ghép kênh và gộp
Các nhà nghiên cứu đã phát triển một bộ hoạt động để phát hiện sự hiện diện của vật liệu di truyền từ vi-rút – trong trường hợp này là SARS-CoV-2 gây ra COVID-19. Bảng mạch điều khiển một bầy rô bốt sắt để vận chuyển các mẫu được từ hóa thông qua quy trình NAAT chẩn đoán, bao gồm vận chuyển tự động, chia mẫu, hợp nhất, trộn và làm nóng các giọt mẫu để khuếch đại sản phẩm phản ứng (ADN). Cuối cùng, các kết quả được xác định dựa trên sự thay đổi màu sắc của chất chỉ thị pH, cho phép diễn giải nhị phân kết quả xét nghiệm, trên hoặc dưới ngưỡng, tương ứng là dương tính hoặc âm tính.
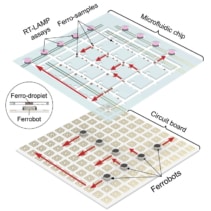
Các nhà nghiên cứu của UCLA cũng đã chứng minh khả năng song song hóa – di chuyển nhiều ferrobot cùng lúc bằng cách sử dụng các ô điện từ trong mạch – cũng như các hoạt động nhiệm vụ tuần tự theo cách hợp tác của từng ferrobot (phối hợp với các ferrobot khác).
Di Carlo cho biết: “Thiết kế nhỏ gọn và xử lý mẫu tự động của nền tảng này cho phép triển khai dễ dàng xét nghiệm gộp, nơi bạn có thể xét nghiệm hàng chục mẫu bệnh phẩm cùng lúc và tất cả đều sử dụng cùng một vật liệu mà hiện tại cần để xét nghiệm cho chỉ một bệnh nhân. “Ví dụ, bạn có thể kiểm tra sinh viên trong toàn bộ ký túc xá của trường đại học chỉ với vài chục bộ dụng cụ kiểm tra.”

Cảm biến sinh học có thể thích ứng nhanh chóng phát hiện vi rút và kháng thể COVID-19
Bằng cách triển khai thuật toán xét nghiệm gộp, có thể xét nghiệm tối đa 16 mẫu trong một xét nghiệm, hệ thống yêu cầu chi phí thuốc thử thấp hơn nhiều so với mức cần thiết để xét nghiệm từng mẫu riêng lẻ. Nếu xét nghiệm gộp cho kết quả dương tính, thì một loạt hoạt động được sắp xếp hợp lý tiếp theo sẽ diễn ra trong nền tảng cho đến khi các mẫu dương tính thực tế được xác định. Cuối cùng, các nhà nghiên cứu lưu ý, chi phí thuốc thử hóa học có thể giảm từ 10 đến 300 lần tùy thuộc vào mức độ phổ biến của virus.
Ngoài việc xét nghiệm đồng thời một số bệnh, nền tảng có thể phân tích một số lượng lớn các mẫu đầu vào song song và không đồng bộ khi chúng đến, tránh thời gian chờ đợi liên quan đến xử lý hàng loạt. Do đó, nhóm nghiên cứu kết luận rằng công nghệ này đóng vai trò là một giải pháp đầy hứa hẹn để tăng khả năng xét nghiệm trên toàn cầu nhằm chuẩn bị cho dịch bệnh và đại dịch.