Các khối u có thể bị tiêu diệt bằng nhiều cách. Xạ trị sử dụng chùm tia bức xạ ion hóa để làm tổn thương DNA và tiêu diệt các tế bào khối u. Một cách tiếp cận ít phổ biến hơn là liệu pháp quang động, sử dụng thuốc kích hoạt bằng ánh sáng để tiêu diệt tế bào ung thư thông qua tổn thương ty thể. Sau đó là kỹ thuật trị liệu phóng xạ (RDT) mới nổi.
“Liệu pháp xạ trị là sự kết hợp giữa xạ trị và liệu pháp quang động,” giải thích. Charlie Ma từ Trung tâm Ung thư Fox Chase, phát biểu tại cuộc họp gần đây Hội nghị thường niên AAPM.
Liệu pháp quang động thường sử dụng ánh sáng laser nhìn thấy được để kích hoạt một loại thuốc cảm quang được ưu tiên định vị trong các tế bào khối u. Thuốc được kích hoạt tạo ra oxy nhóm đơn có tính độc tế bào cao gây chết tế bào. Tuy nhiên, sự thâm nhập hạn chế của ánh sáng laser vào mô có nghĩa là kỹ thuật này chủ yếu được sử dụng để điều trị các khối u bề mặt hoặc các vị trí có thể tiếp cận bằng nội soi. Để điều trị các khối u nằm sâu mà liệu pháp quang động không thể chạm tới, RDT sử dụng chùm photon năng lượng cao để kích hoạt chất cảm quang.
Ma giải thích: “Trong RDT, chúng tôi sử dụng 20 đến 30% liều xạ trị. “Và sau đó chúng tôi cũng sử dụng đèn Cherenkov.” Ông lưu ý rằng bức xạ Cherenkov này, được tạo ra trong quá trình xạ trị khi chùm tia điều trị tương tác với mô của bệnh nhân, sẽ có sự phân bố ánh sáng gần như giống hệt với sự phân bố liều bức xạ trị liệu và do đó có thể dễ dàng lên kế hoạch.
Ngoài việc tích tụ trong khối u nguyên phát, thuốc cũng sẽ được hấp thụ bởi các tế bào di căn phân tán, chúng có thể bị tiêu diệt bằng cách sử dụng liều lượng ánh sáng Cherenkov rất thấp. Ma cho biết: “Lần đầu tiên, RDT biến liệu pháp xạ trị không chỉ ở địa phương và khu vực mà còn trở thành một kỹ thuật điều trị toàn thân.
Nhóm tại Fox Chase đang sử dụng một loại thuốc gọi là axit 5-aminolevulinic (5-ALA) cho RDT. 5-ALA được ty thể trong tế bào ung thư hấp thụ, với sự hấp thu ở khối u cao gấp 10 đến 20 lần so với các mô bình thường. Khi ở trong tế bào ung thư, 5-ALA được chuyển hóa thành protoporphyrin IX (PpIX), một chất cảm quang có đỉnh phổ hấp thụ ở khoảng 380–430nm. Điều này không lý tưởng đối với ánh sáng laser đỏ thường được sử dụng trong liệu pháp quang động. Tuy nhiên, nó rất phù hợp với đỉnh hấp thụ Cherenkov ở bước sóng 370–430 nm.
Bằng chứng tiền lâm sàng
Trong vài năm qua, Ma và nhóm của ông đã thực hiện nhiều nghiên cứu tiền lâm sàng sử dụng các dòng tế bào khối u khác nhau và các năng lượng bức xạ khác nhau. Ông đã chia sẻ một số kết quả từ một nghiên cứu lớn (vài trăm động vật) đánh giá RDT trên chuột mang khối u bằng cách sử dụng 100 mg/kg 5-ALA và chiếu xạ photon 6, 15 hoặc 45 MV.
Ma lưu ý rằng khối u rất hung hãn, chỉ riêng xạ trị 4 Gy chỉ tiêu diệt được khoảng 10% tế bào khối u. Ngoài ra, RDT ở mức 6 MV không làm tăng đáng kể hiệu quả điều trị. “Đó là lý do tại sao mọi người lo lắng rằng ánh sáng Cherenkov không đủ,” ông lưu ý. “Nhưng với MV 15 và 45, bạn thấy khối u chậm phát triển hơn nhiều. Chúng tôi vẫn đang nghiên cứu tại sao có sự thay đổi mạnh mẽ này do năng lượng, chúng tôi cần tìm ra cơ chế chính xác đằng sau nó.”
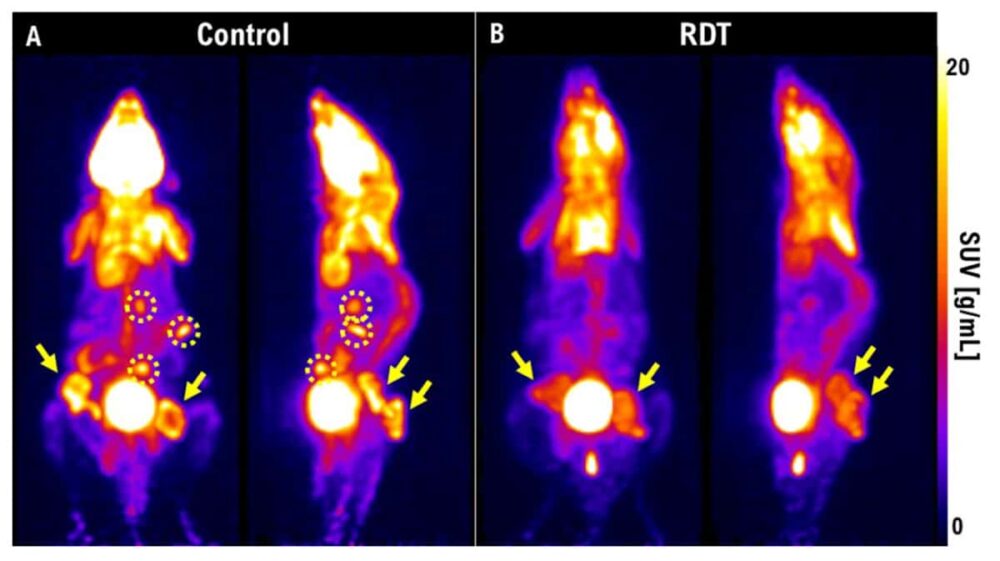
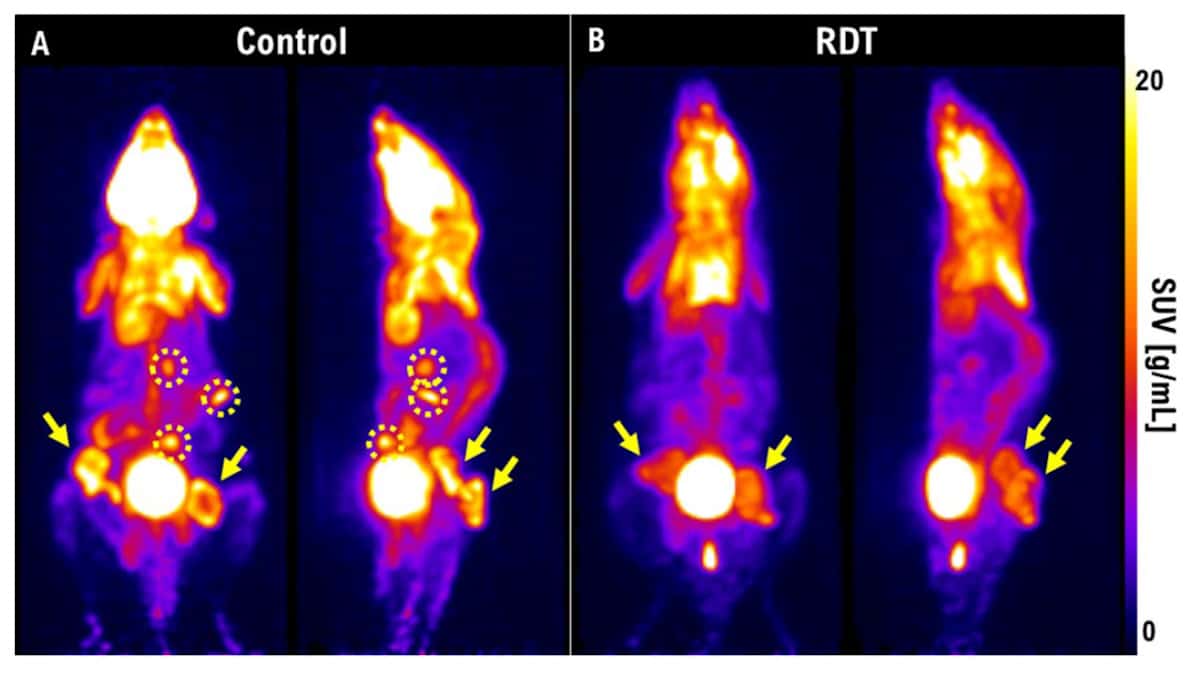
Nhóm nghiên cứu đã sử dụng PET để hình dung sự co rút của khối u sau RDT. Một tuần sau điều trị, khối u ở chuột đối chứng đã phát triển và di căn, trong khi những con được điều trị bằng RDT có tổn thương nhỏ hơn nhiều và không có di căn. Ma cũng mô tả một nghiên cứu về bệnh ung thư tuyến giáp rất nguy hiểm ở thỏ. Một tuần sau 3 Gy xạ trị, khối u vẫn đang phát triển. “Nhưng nếu chúng tôi sử dụng RDT ở mức 3 Gy với 5-ALA, khối u sẽ không được nhìn thấy trên hình ảnh PET.” Ông nhấn mạnh rằng PET cung cấp một phương pháp tuyệt vời để thực hiện đánh giá điều trị sớm và có thể giúp xác định liệu RDT có hiệu quả ở bệnh nhân hay không.
Fox Chase hiện đang thực hiện thử nghiệm lâm sàng về RDT, với giai đoạn đầu tiên của nghiên cứu là kiểm tra sự tăng liều (cả liều bức xạ và liều thuốc) trong các khối u giai đoạn cuối. Giai đoạn này hiện đã đạt đến mức liều cuối cùng khi chỉ còn lại ba bệnh nhân, Ma cho biết và chỉ ra rằng cho đến nay không có trường hợp độc tính nào xảy ra. Ở những nơi khác, một thử nghiệm RDT thứ hai tại Bệnh viện Đại học Muenster đang kiểm tra những bệnh nhân bị u nguyên bào thần kinh đệm tái phát lần đầu.
Trường hợp thực tế
Cuối cùng, Ma trình bày kết quả từ một số trường hợp thực tế. “Bạn sẽ rất hào hứng khi xem những thứ này,” anh ấy nói với khán giả, đồng thời lưu ý rằng “thông thường, mọi người không tin rằng nó hoạt động trừ khi bạn chụp ảnh CT, MR hoặc PET trong một tháng”.
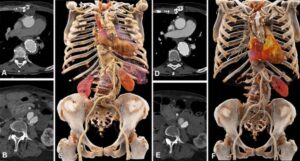
Trong ví dụ đầu tiên, về điều trị di căn gan, ông cho thấy rằng một tháng sau RDT, hình ảnh PET cho thấy không còn khối u nào. Tiếp theo, ông trình bày một trường hợp ung thư phổi di căn: “bạn có thể thấy kết quả rất ấn tượng với các khối u ngừng hoạt động sau RDT,” ông nói.
Thiết bị cấy ghép mang lại liệu pháp quang động được cá nhân hóa
Các phương pháp điều trị RDT thành công khác bao gồm ung thư thực quản, khối u phổi có nhiều di căn xương và một bệnh nhân đã thất bại trong hóa trị nhưng có phản ứng tốt ba ngày sau RDT. Ma lưu ý rằng hầu hết bệnh nhân đều mắc bệnh ung thư giai đoạn cuối và đã thất bại trong các phương pháp điều trị khác. Ông nói thêm: “Chúng tôi thấy có hiệu quả nên hy vọng chúng tôi có thể cải thiện khả năng sống sót của họ”.
Ma kết luận: “RDT có thể là phương pháp điều trị cục bộ, khu vực và toàn thân kết hợp giữa xạ trị và liệu pháp quang động. "Chúng tôi có rất nhiều ống nghiệm và trong cơ thể các thử nghiệm để chứng minh tiềm năng điều trị của nó và mặc dù các thử nghiệm lâm sàng còn ít nhưng tôi hy vọng chúng ta sẽ có nhiều kết quả hơn trong tương lai và biến điều này thành một điều gì đó thực sự hữu ích.”
- Phân phối nội dung và PR được hỗ trợ bởi SEO. Được khuếch đại ngay hôm nay.
- PlatoData.Network Vertical Generative Ai. Trao quyền cho chính mình. Truy cập Tại đây.
- PlatoAiStream. Thông minh Web3. Kiến thức khuếch đại. Truy cập Tại đây.
- Trung tâmESG. Ô tô / Xe điện, Than đá, công nghệ sạch, Năng lượng, Môi trường Hệ mặt trời, Quản lý chất thải. Truy cập Tại đây.
- BlockOffsets. Hiện đại hóa quyền sở hữu bù đắp môi trường. Truy cập Tại đây.
- nguồn: https://physicsworld.com/a/radiodynamic-therapy-harnessing-light-to-improve-cancer-treatments/
- : có
- :là
- :không phải
- $ LÊN
- 10
- 100
- 15%
- 20
- 30
- a
- Giới thiệu
- truy cập
- thêm
- Ngoài ra
- Sau
- tích cực
- AL
- cô đơn
- Ngoài ra
- Mặc dù
- an
- và
- động vật
- hàng năm
- bất kì
- phương pháp tiếp cận
- LÀ
- xung quanh
- AS
- Đánh giá
- At
- khán giả
- BE
- Chùm tia
- sau
- Tin
- XƯƠNG
- cả hai
- nhưng
- by
- gọi là
- CAN
- Ung thư
- Các tế bào ung thư
- không thể
- trường hợp
- trường hợp
- nguyên nhân
- Tế bào
- Trung tâm
- thay đổi
- đuổi theo
- vòng tròn
- Nhấp chuột
- Lâm sàng
- các thử nghiệm lâm sàng
- kết hợp
- kết hợp
- Chung
- kết luận
- điều khiển
- có thể
- Ngày
- Tử vong
- chậm trễ
- cung cấp
- chứng minh
- mô tả
- phá hủy
- bị phá hủy
- Xác định
- thiết bị
- ĐÃ LÀM
- khác nhau
- phân phối
- phân phối
- dna
- do
- dont
- đáng kể
- thuốc
- hai
- suốt trong
- Đầu
- dễ dàng
- hiệu lực
- Hiệu quả
- nơi khác
- mới nổi
- nhấn mạnh
- năng lượng
- leo thang
- đánh giá
- Kiểm tra
- ví dụ
- tuyệt vời
- kích thích
- thí nghiệm
- Giải thích
- thất bại
- xa
- vài
- cuối cùng
- Tìm kiếm
- Tên
- lần đầu tiên
- tiếp theo
- Trong
- fox
- từ
- tương lai
- tạo ra
- tạo
- tốt
- tuyệt vời
- lớn hơn
- Phát triển
- mới lớn
- Tăng trưởng
- có
- Khai thác
- Có
- he
- giúp đỡ
- cao
- của mình
- mong
- Hy vọng
- Tuy nhiên
- HTTPS
- một trăm
- i
- lý tưởng
- giống hệt nhau
- if
- hình ảnh
- hình ảnh
- Hình ảnh
- nâng cao
- in
- bao gồm
- Tăng lên
- chỉ
- thông tin
- trong
- tương tác
- trong
- vấn đề
- IT
- ITS
- jpg
- chỉ
- Giết chết
- lớn
- tia laser
- Họ
- trái
- ít
- Cấp
- ánh sáng
- Hạn chế
- dòng
- Gan
- địa phương
- Rất nhiều
- Thấp
- phần lớn
- làm cho
- LÀM CHO
- nhiều
- Trận đấu
- max-width
- có nghĩa
- cơ chế
- Ti thể
- tháng
- chi tiết
- hầu hết
- mr
- nhiều
- nhiều
- Cần
- tiếp theo
- Không
- bình thường
- lưu ý
- Lưu ý
- tại
- con số
- xảy ra
- of
- thường
- on
- hàng loạt
- ONE
- có thể
- mở
- or
- Nền tảng khác
- ra
- Ôxy
- bệnh nhân
- bệnh nhân
- Đỉnh
- thâm nhập
- người
- mỗi
- Thực hiện
- thực hiện
- biểu diễn
- Cá nhân
- giai đoạn
- Vật lý
- Thế giới vật lý
- kế hoạch
- plato
- Thông tin dữ liệu Plato
- PlatoDữ liệu
- thêm
- tiềm năng
- trình bày
- chính
- cung cấp
- Xạ trị
- đạt
- đạt
- có thật không
- gần đây
- sự tái xuất
- đỏ
- khu vực
- vẫn
- phản ứng
- Kết quả
- Tiết lộ
- Nói
- Thứ hai
- xem
- đã xem
- một số
- chia sẻ
- cho thấy
- đáng kể
- Các trang web
- nhỏ hơn
- So
- cho đến nay
- một số
- một cái gì đó
- nói
- quang phổ
- Vẫn còn
- nghiên cứu
- Học tập
- Học tập
- thành công
- đủ
- sống còn
- hệ thống
- Lấy
- nhóm
- hơn
- việc này
- Sản phẩm
- Tương lai
- cung cấp their dịch
- sau đó
- Đó
- Kia là
- điều này
- những
- số ba
- thumbnail
- Như vậy
- thời gian
- thời gian
- đến
- điều trị
- điều trị
- thử nghiệm
- thử nghiệm
- đúng
- thường
- trường đại học
- sử dụng
- đã sử dụng
- sử dụng
- sử dụng
- khác nhau
- rất
- thông qua
- có thể nhìn thấy
- là
- Đường..
- cách
- we
- tuần
- liệu
- cái nào
- trong khi
- tại sao
- sẽ
- với
- ở trong
- công trinh
- thế giới
- lo lắng
- sẽ
- năm
- Bạn
- zephyrnet