生物环境中化学反应的远程控制可以实现多种医疗应用。 例如,在体内靶标释放化疗药物的能力可以帮助绕过与这些有毒化合物相关的破坏性副作用。 为了实现这一目标,加州理工学院的研究人员(加州理工学院)创建了一种全新的药物输送系统,该系统使用超声波在需要的时间和地点精确地释放诊断或治疗化合物。
该平台是在实验室开发的 麦克斯韦·罗伯 和 米哈伊尔·夏皮罗,基于被称为机械载体的力敏感分子,这些分子在受到物理力时会发生化学变化并释放较小的货物分子。 机械刺激可以通过聚焦超声波 (FUS) 提供,该超声波可深入生物组织,并能以亚毫米精度施加。 然而,早期对该方法的研究需要高声强度,这会导致发热并可能损坏附近的组织。
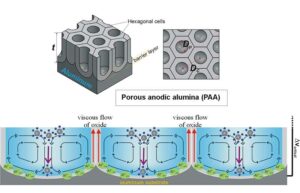
为了能够使用较低且更安全的超声强度,研究人员转向了气体囊泡(GV),即可用作超声造影剂的充满空气的蛋白质纳米结构。 他们假设 GV 可以充当声机械换能器来聚焦超声能量:当暴露于 FUS 时,GV 会发生空化,产生的能量会激活机械团。
“通过超声波施加力通常依赖于非常强烈的条件,从而引发微小溶解气泡的内爆,”共同第一作者解释道 莫莉麦克法登 在一份新闻声明中。 “它们的崩溃是激活机械载体的机械力的来源。 囊泡对超声波的敏感性更高。 使用它们,我们发现在更弱的超声波下也可以实现相同的机械力激活。”
在报告中报告他们的发现 诉讼中的国家科学院院士研究人员证明,这种方法可以使用生物相容性 FUS 远程触发机械载体功能化聚合物中货物分子的释放。
药物输送开发
McFadden 和同事首先确定了生理应用的安全超声参数。 330 kHz FUS 实验显示,占空比为 1.47%(每个脉冲 4.5 个周期)的生物相容性上限为 3000 MPa 峰值负压,声强度为 3.6 W/cm2。 在模拟组织的凝胶体模中,这些参数导致最大温度仅升高 3.6 °C。
研究人员随后研究了 FUS 是否可以利用这些生物相容性参数激活含有机械力团的聚合物。 他们研究了聚合物 PMSEA,该聚合物含有以链为中心的机械载体,负载有荧光小分子。 在 GV 存在的情况下将该聚合物的稀溶液暴露于生物相容性 FUS 中会导致荧光强烈增加,表明有效负载成功释放 - FUS 暴露 15 分钟后释放约 10%。 重要的是,没有 GV 的 FUS 暴露不会触发荧光反应,这证实了 GV 作为声机械换能器发挥着重要作用。
接下来,研究人员检查了该系统是否适合机械触发药物释放。 他们将化疗药物喜树碱与机械载体结合,然后聚合生成 PMSEA-CPT,并使用 FUS 提供控释。 接触生物相容性 FUS 加 GV 10 分钟后,约 8% 的喜树碱被释放。 正如荧光分子所发现的那样,在没有 GV 的情况下没有检测到药物释放。
据共同第一作者称 姚玉兴,这是 FUS 首次被证明可以控制生物环境中的特定化学反应。 “以前超声波被用来破坏物体或移动物体,”姚说。 “但现在它利用机械化学为我们开辟了这条新道路。”
为了评估该平台未来对患者进行靶向化疗的潜力,研究人员调查了其细胞毒性 细胞/组织 作用于类淋巴母细胞 Raji 细胞。 与之前暴露于 FUS 和 GV 的 PMSEA-CPT 一起孵育两天的细胞表现出活力显着下降。 相反,在与未暴露于FUS的PMSEA-CPT一起孵育的细胞或暴露于FUS但没有GV的PMSEA-CPT的细胞中没有观察到显着的细胞毒性。

光触发植入装置提供可编程药物输送
研究人员写道:“水介质中聚合物的分子有效负载的机械触发释放说明了这种方法在聚合物机械化学的非侵入性生物成像和治疗应用中的力量。” “更广泛地说,这项研究展示了一种在生物医学相关条件下利用 FUS 提供的时空精度和组织穿透力实现特定化学反应远程控制的方法。”
在受控实验室条件下进行这些初步测试后,研究人员现在计划在活生物体中测试他们的平台。 “我们正在努力将这一基本发现转化为 体内 药物输送和其他生物医学技术的应用,”罗布说 物理世界.
- :具有
- :是
- :不是
- :在哪里
- 1
- 10
- 15%
- 3000
- a
- 对,能力--
- 学院
- 实现
- 实现
- 激活
- 活化
- 有能力
- 后
- 经纪人
- 中介代理
- 瞄准
- an
- 和
- 应用领域
- 应用的
- 的途径
- 约
- 保健
- 围绕
- AS
- 评估
- 相关
- At
- 作者
- 基于
- BE
- 很
- 生物医学
- 身体
- 界
- 宽广地
- 但是
- by
- 加州
- CAN
- 癌症预防
- 原因
- 细胞
- 更改
- 化学
- 崩溃
- 同事
- 条件
- 包含
- 对比
- 控制
- 受控
- 可以
- 创建信息图
- 创建
- 周期
- 周期
- 损坏
- 一年中的
- 减少
- 深
- 提供
- 交货
- 演示
- 证明
- 演示
- 检测
- 发达
- 设备
- 诊断
- DID
- 发现
- 破坏
- 不同
- 药物
- 毒品
- 此前
- 影响
- enable
- 能源
- 完全
- 环境中
- 必要
- 例子
- 实验
- 介绍
- 裸露
- 曝光
- 发现
- (名字)
- 第一次
- 专注焦点
- 重点
- 其次
- 针对
- 力
- 发现
- 止
- 功能
- 根本
- 未来
- 天然气
- 民政事务总署
- 有
- 提高
- 帮助
- 高
- 但是
- HTTPS
- 确定
- 说明
- 图片
- 爆
- 重要的
- in
- 增加
- 孵化
- 信息
- 初始
- 研究所
- 成
- 问题
- 它的
- JPG
- 已知
- 实验室
- 实验室
- 导致
- 左
- 极限
- 活的
- 降低
- 最大宽度
- 最多
- 机械
- 媒体
- 医生
- 医疗应用
- 方法
- 分钟
- 分子
- 分子
- 移动
- 许多
- National
- 打印车票
- 负
- 全新
- 没有
- 现在
- of
- on
- 仅由
- 开放
- or
- 其他名称
- 参数
- 径
- 患者
- 高峰
- 渗透
- 为
- 模体
- 的
- 物理
- 物理世界
- 计划
- 平台
- 平台
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 播放
- 加
- 聚合物
- 潜力
- 功率
- 恰恰
- 平台精度
- 存在
- express
- 压力
- 先前
- 可编程
- 蛋白质
- 提供
- 提供
- 提供
- 脉冲
- 范围
- 反应
- 反应
- 释放
- 发布
- 相应
- 远程
- 必须
- 研究人员
- 响应
- 导致
- 揭密
- 右
- 角色
- 安全
- 更安全
- 同
- 说
- 看到
- 灵敏度
- 设置
- 侧
- 显著
- 小
- 小
- 方案,
- 来源
- 具体的
- 个人陈述
- 刺激物
- 强烈
- 研究
- 研究
- 学习
- 成功
- 合适的
- 系统
- 目标
- 针对
- 技术
- 专业技术
- 告诉
- test
- 测试
- 这
- 其
- 他们
- 然后
- 博曼
- 他们
- 事
- Free Introduction
- 通过
- 缩略图
- 次
- 至
- 翻译
- 触发
- 引发
- true
- 转身
- 二
- 下
- 经历
- us
- 使用
- 用过的
- 使用
- 运用
- 平时
- 非常
- 通过
- 可行性
- 是
- we
- ,尤其是
- 是否
- 这
- 中
- 也完全不需要
- 加工
- 世界
- 写
- 和风网