研究人员在 杜克大学医学中心 开发了一种基于深度学习的计算机辅助检测 (CAD) 系统,以识别 MR 图像上难以检测的脑转移。 该算法表现出出色的灵敏度和特异性,优于其他开发中的 CAD 系统。 该工具显示出能够更早识别新出现的脑转移瘤的潜力,使它们能够在首次出现时通过立体定向放射外科 (SRS) 进行靶向治疗,并且对于某些患者而言,还可以减少所需治疗的次数。
SRS 使用精确聚焦的光子束在单次放射治疗中向大脑中的目标输送高剂量辐射,正在发展成为针对脑转移瘤数量有限的患者的标准治疗。 然而,要靶向转移灶,必须首先在 MR 图像上识别它。 不幸的是,大约 10% 不是,30% 的尺寸小于 3 毫米,即使经过专家神经放射学家的审查也是如此。
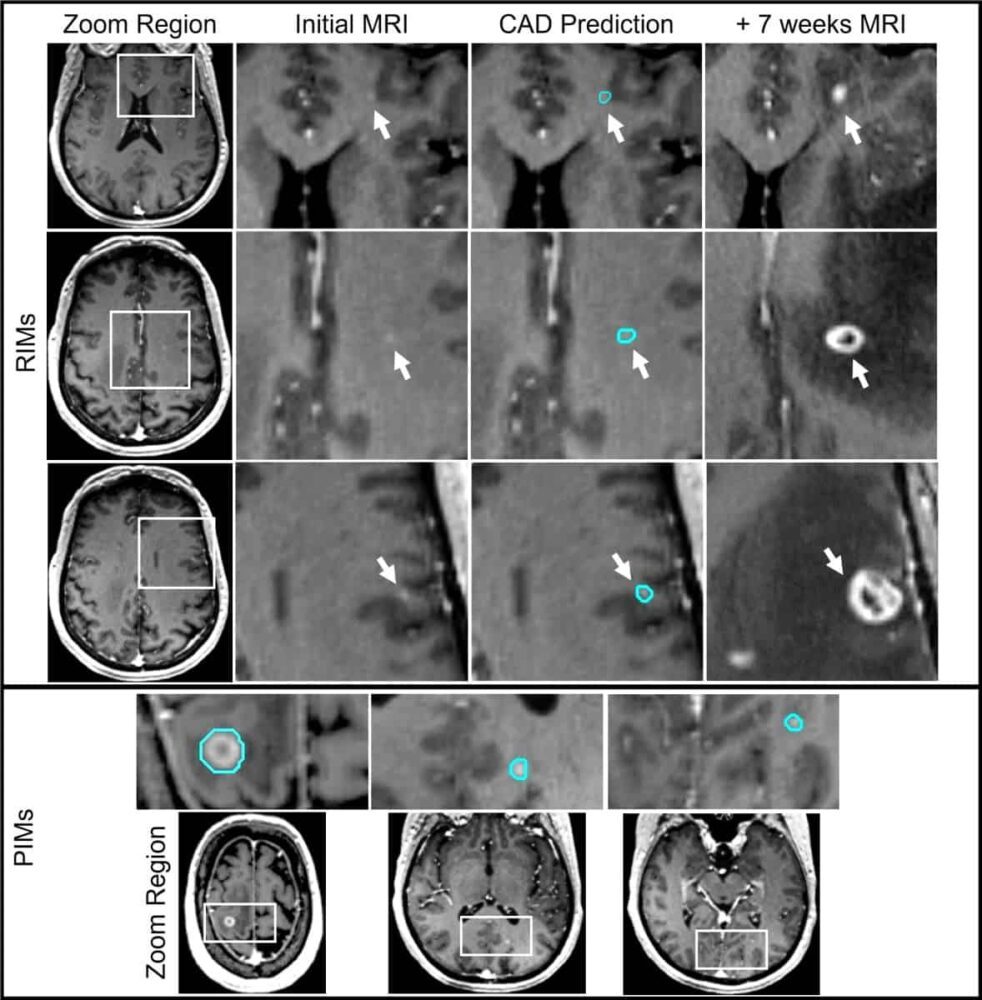
当这些未被发现的脑转移——研究人员称之为回顾性确定的转移 (RIM)——在随后的 MRI 扫描中被识别时,通常需要进行第二次 SRS 治疗。 这种治疗很昂贵,而且可能不舒服且具有侵入性,有时需要用用别针固定在头骨上的框架来固定头部。
在最近的 ASTRO 年会上, 德文戈弗雷 解释说,研究人员设计了基于卷积神经网络 (CNN) 的 CAD 系统,专门用于改进难以检测的 RIM 和非常小的前瞻性识别转移 (PIM) 的检测和分割。 Godfrey 及其同事在 国际放射肿瘤学生物学物理学杂志.
该团队使用来自 135 名患有 563 处脑转移瘤的患者的 MRI 数据(对比增强的破坏梯度回波序列)对 CAD 工具进行了训练。 这些图像是使用来自 Duke Health 多个地点的不同供应商的 1.5 T 和 3.0 T MRI 扫描仪获取的。 数据集总共包括 491 个 PIM,中位直径为 6.7 mm,以及来自 72 名患者的 32 个 RIM,中位直径为 2.7 mm。
为了识别 RIM,研究人员检查了每位患者的原始 MR 图像,以在后来检测到转移的确切位置寻找对比度增强的迹象。 经过审查,他们将每个 RIM 分类为满足基于影像学的诊断标准 (+DC) 或视觉信息不足 (-DC),无法确定为转移。
研究人员将 RIM 和 PIM 的数据集随机分为五组,其中四组用于模型和算法开发,另一组作为测试组。 “同时包含 +DC 和 -DC RIM 导致每个脑转移类别和大小的灵敏度最高,同时还返回最低的假阳性率和最高的阳性预测值,”他们报告说。 “这表明将具有挑战性的小脑转移超加权采样纳入 CAD 训练数据具有明显的好处。”
对于在 MRI 上具有明显转移特征的 PIM 和 +DC RIM,该模型的总体灵敏度达到 93%,范围从直径大于 100 毫米的病灶的 6% 到小于 79 毫米的病灶的 3%。 假阳性率也低得令人印象深刻,平均每人 2.7 个,而其他 CAD 系统的假阳性率在 35 到 XNUMX 个之间,对小病变的检测灵敏度相当。
CAD 系统还能够检测开发和测试集中的一些 -DC RIM。 在这个最早阶段识别脑转移将是一个很大的临床优势,因为这样的病变可以通过成像进行更彻底的监测,如果需要的话可以促进治疗。
Duke 团队现在正致力于通过利用多个 MR 序列来提高 CAD 工具的准确性。 Godfrey 解释说,大脑 MRI 研究几乎总是包括多个 MR 序列,这些序列产生关于大脑中每个体素的独特信息。 “我们认为,结合从这些其他序列中获得的额外信息应该会提高其准确性,”他说。
Godfrey 指出,研究人员距离启动现有 CAD 系统的模拟前瞻性临床使用研究仅几周时间,以调查该工具如何影响放射科医生和放射肿瘤科医生的临床决策。
深度学习帮助放射科医生通过胸部 X 光检测肺癌
“执行 SRS 的多位专家神经放射学家和神经放射肿瘤学家将接受脑部 MR 扫描。 他们将被要求找到任何可能是脑转移的病灶,评估他们对此的置信度,并根据其在图像中的出现说明他们是否会用 SRS 治疗该病灶,”他说 物理世界. “然后我们将向他们展示 CAD 预测并评估 CAD 对每位医生临床决策的影响。”
如果这项模拟研究产生可喜的结果,Godfrey 预计将部署 CAD 工具,以帮助前瞻性地识别在杜克放射肿瘤诊所根据研究方案接受治疗的新患者中具有挑战性的脑转移,最早可能在 2023 年年中。