创伤性脑损伤 (TBI) 是由头部突然摇晃或撞击引起的,需要尽快诊断。 为了防止不可逆转的损害,必须在创伤后的“黄金小时”内做出至关重要的治疗决定。 然而,在护理点诊断 TBI 很困难,需要依赖救护人员的观察,以及到达医院后进行 MRI 或 CT 扫描等放射学检查。
为了能够更及时地进行干预,来自 伯明翰大学 正在开发一种手持式诊断设备,通过向眼睛照射安全激光来检测 TBI。 该设备,描述于 科学进展的目标是在受伤发生后立即使用 - 无论是在路边、战场还是运动场上 - 评估患者的 TBI,确定创伤的严重程度并相应地指导治疗。
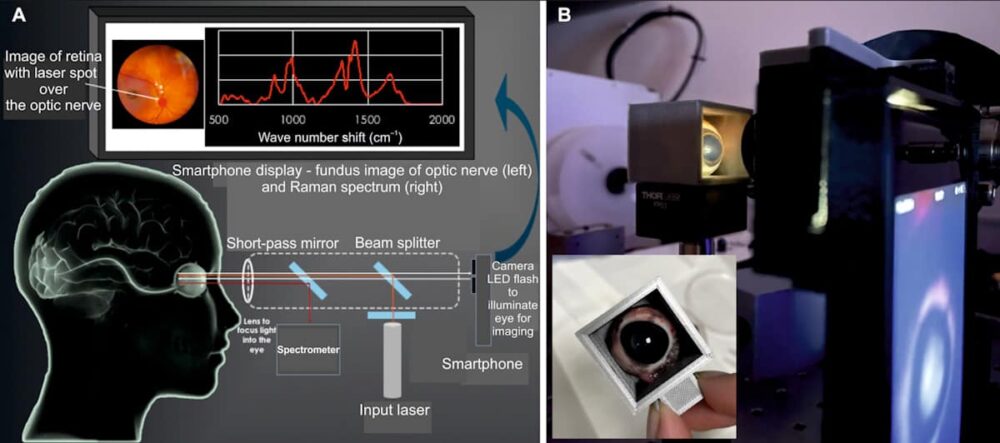
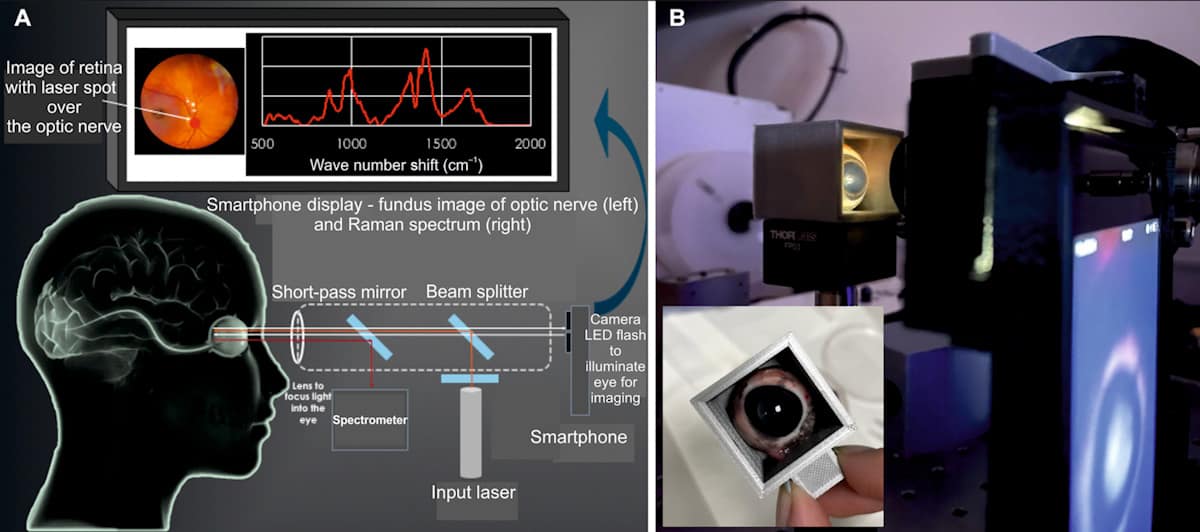
这款人眼安全设备 (EyeD) 基于拉曼光谱——一种利用激光非弹性散射来探测分子成分的光学技术。 它的工作原理是将 635 nm 1 级激光照射到角膜上。 然后,准直光束通过眼睛自身的光学器件聚焦到视网膜上。 为了将激光瞄准感兴趣的区域,EyeD 系统使用智能手机摄像头同时进行眼底成像和光谱分析,以可视化眼睛后部。
使用人工神经网络算法 SKiNET 作为决策支持工具,分析从视网膜和视神经收集的拉曼光谱是否存在 TBI 特异性生化变化。 由于视网膜和视神经与大脑的联系如此紧密,损伤后生物标志物的变化将反映大脑微环境的生化变化。
“我们的设备将通过直接实时评估活体神经视网膜/视神经组织的急性应激变化来实现 TBI 的早期诊断。 它使我们能够直接、非侵入性地询问中枢神经系统组织,”团队负责人解释道 波拉·戈德堡·奥本海默。 “将神经视网膜作为中枢神经系统的投影进行分析,为了解大脑生物化学提供了一个窗口。”
光谱研究
为了测试成像设备的性能,奥本海默和同事构建了一个组织模型,模仿眼睛的物理尺寸和光学特征,同时提供真实的视网膜拉曼特征。 该体模包括一个透镜、一个代表未散瞳的直径 4 毫米的针孔和用于视网膜组织的样品架。
研究小组证明,EyeD 设备可以有效地将激光束聚焦在视网膜上的所需位置。 从组织模型测量的光谱解析了高波数区域的主要拉曼谱带,可用于区分多种组织类型。
研究人员接下来使用原型设备分析了猪眼的视网膜样本,猪眼的大小、结构、发育和成分与人眼相似。 他们从 510 个 TBI 视网膜样本和 39 个对照样本中收集了 12 个测量值,记录了靠近视神经盘的光谱。 总体而言,拉曼光谱在 1200–1700 cm 范围内显示出几个特征谱带。 - 1 指纹区域,加上 2800–3200 cm 内高波数带的增强 - 1 地区。
使用 SKiNET 创建自优化图 (SOM),显示视网膜拉曼光谱的聚类,揭示了 TBI 视网膜和对照样本之间的明显分离。 出现这种情况是因为拉曼光谱反映了 TBI 后眼睛的生化变化。 例如,TBI 会增加眼睛中的脂质和蛋白质含量,导致源自这些的峰在拉曼光谱中变得更加明显。
TBI 反应中最显着的光谱变化是由于脑脂质心磷脂和细胞色素 C 的贡献,表现为 2930 cm 与 2850 cm 的比率增加。 - 1 拉曼光谱中出现峰值。 研究人员使用 TBI 光谱中 2850/2930 峰比和六个特征峰强度的选定特征来形成 SKiNET 分类,从而生成用于 TBI 检测的光谱条形码。
为了评估 EyeD 系统通过视网膜变化区分 TBI 的能力,他们计算了每个峰值的曲线下面积 (AUC) 和 2930/2850 峰值比率,并绘制了真阳性率与假阴性率的图。 使用 SKiNET 优化对训练数据进行 10 倍交叉验证,分类准确率达到 90.7±0.9%。 该结果表明,TBI 后 2930/2850 峰值比的变化可以提供区分 TBI 与健康对照的有价值的指标。
“使用同步拉曼光谱和眼底成像,封装为低成本手持设备,为 TBI 的非侵入性护理点诊断提供了第一个切实可行的途径,”Oppenheimer 说道。 物理世界.

对于脑震荡,眼睛是大脑的窗户
下一步将是优化临床验证原型。 为了简化临床转化,研究人员计划用紧凑型设备上光谱仪和智能手机读数器取代独立光谱仪,通过单个智能手机屏幕实现眼底摄影和拉曼光谱。
“我们目前正在设计一种用户友好的可部署设备,与我们的人工神经网络算法集成,无需专家支持即可自动解释输出,快速对光谱数据进行分类,”奥本海默说。 “[我们还]在健康志愿者和患者中临床评估设备的可用性,以证明其实时诊断的潜力。 在确定设备的耐受性和可用性后,我们正在进行首次人体评估和小规模临床试验。”
- :是
- 1
- 10
- 12
- 39
- a
- 对,能力--
- AC
- 因此
- 获得
- 增加
- 后
- 驳
- 算法
- 让
- 允许
- 还
- 美国人
- an
- 分析
- 分析
- 和
- 应用领域
- 保健
- 国家 / 地区
- 围绕
- 到来
- 人造的
- AS
- 评估
- 评估
- At
- 澳柯
- 自动化
- 背部
- 基于
- 战场
- BE
- 光束
- 因为
- 成为
- 之间
- 大脑
- by
- 计算
- 相机
- CAN
- 造成
- 造成
- 中央
- 更改
- 特点
- 特点
- 程
- 分类
- 清除
- 点击
- 临床资料
- 关闭
- 密切
- 集群
- 同事
- 紧凑
- 写作
- 概念
- 条件
- 内容
- 捐款
- 控制
- 控制
- 可以
- 创建信息图
- 目前
- 曲线
- 损伤
- data
- 决定
- 决定
- 演示
- 证明
- 描述
- 设计
- 期望
- 检测
- 确定
- 发展
- 研发支持
- 设备
- 诊断
- 诊断
- 诊断
- 诊断
- 区分
- 难
- 尺寸
- 直接
- 直接
- 区分
- 遇险
- 两
- 每
- 缓解
- 只
- enable
- 使
- 使
- 工程师
- 建立
- 评估
- 评估
- 例子
- 介绍
- 眼
- 眼部彩妆
- 特征
- 指纹
- (名字)
- 专注焦点
- 重点
- 其次
- 以下
- 足球
- 针对
- 申请
- 止
- 头
- 健康
- 持有人
- 医院
- 但是
- HTTPS
- 人
- 图片
- 同步成像
- 影响力故事
- in
- 包括
- 增加
- 增加
- 表示
- 指示符
- 信息
- 伤
- 集成
- 解释
- 介入
- 成
- 调查
- 问题
- IT
- 它的
- JPG
- 激光器是如何工作的
- 领导者
- 光
- 链接
- 活的
- 廉价
- 制成
- 主要
- 地图
- 最大宽度
- 测量
- 分子
- 更多
- 最先进的
- MRI
- 多数
- 必须
- 网络
- 神经
- 神经网络
- 下页
- 数
- of
- 优惠精选
- on
- 到
- 打开
- 光学
- 优化
- 优化
- or
- 始发
- 我们的
- 输出
- 最划算
- 己
- συσκευάζονται
- 径
- 患者
- 高峰
- 性能
- 施行
- 模体
- 摄影
- 的
- 物理
- 物理世界
- 沥青
- 计划
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 加
- 手提
- 位置
- 可能
- 潜力
- 存在
- 防止
- 探测器
- 投影
- 宣判
- 蛋白质
- 原型
- 提供
- 提供
- 优
- 很快
- 急速
- 价格表
- 比
- 真实
- 实时的
- 现实
- 了解
- 反映
- 地区
- 依托
- 更换
- 代表
- 需要
- 研究人员
- 解决
- 响应
- 导致
- 视网膜
- 揭密
- 安全
- 说
- 科学
- 屏风
- 选
- 几个
- 显示
- 签名
- 显著
- 类似
- 同时
- 单
- SIX
- 尺寸
- 智能手机
- So
- 或很快需要,
- 专家
- 光谱
- 光谱
- 运动
- 独立
- 步
- 结构体
- 这样
- 突
- SUPPORT
- 系统
- 有形
- 目标
- 针对
- 团队
- 技术
- 专业技术
- test
- 这
- 区域
- 其
- 然后
- 博曼
- 他们
- Free Introduction
- 通过
- 缩略图
- 次
- 及时
- 至
- 工具
- 向
- 产品培训
- 翻译
- 治疗
- 试用
- true
- 类型
- 下
- 上
- us
- 可用性
- 使用
- 用过的
- 用户友好
- 使用
- 运用
- 验证
- 有价值
- 通过
- 想像
- 志愿者
- we
- 为
- 是否
- 这
- 而
- 将
- 窗口
- 窗户
- 中
- 也完全不需要
- 合作
- 世界
- 生产
- 和风网