香港, 17年2022月3681日 – (亚太商讯) – 中国抗体生物科技有限公司(「中国抗体」或「公司」,连同其附属公司统称「集团」,股份代号:11.HK),一家总部位于香港的生物制药公司公司致力于免疫性疾病治疗药物的研究、开发、制造和商业化,很高兴地宣布,于 2022 年 17 月 17 日(美国东部时间),该公司的新药研究申请(“IND”) First-in-Class(FIC)哮喘治疗产品SM2022(注射用人源化抗ILXNUMXRB单克隆抗体)已提交美国食品药品监督管理局(“FDA”)并获得受理。一旦 IND 获得 FDA 批准,该公司计划于 XNUMX 年第一季度在美国启动首次人体研究。
 |
SM17是由汉诺生物和LifeArc(一家总部位于英国的医学研究慈善机构)共同开发的全球首个靶向IL17BR的单克隆抗体。 SM17适应症范围广泛,包括市场容量较大的适应症,如哮喘和特发性肺纤维化等高死亡率疾病。 与市面上其他产品相比,SM17具有差异化优势。 凭借 SM17 的临床前数据和独特的作用机制,公司认为 SM17 对哮喘治疗的潜在影响比其他批准的生物制剂更广泛和更有益。
在全球市场上,哮喘患者人数逐渐增加,预计到 247.5 年将达到 2023 亿,到 267.7 年将进一步增加到 2030 亿。预计到 25.6 年将达到 2023 万,到 27.8 年将进一步增加到 2030 万。就市场规模而言,全球哮喘市场预计到 25.1 年将达到 2023 亿美元,到 34.6 年将达到 2030 亿美元。中国预计到 36.4 年将达到 2023 亿元人民币,到 65.0 年达到 2030 亿元人民币。在治疗选择方面,传统的哮喘治疗以吸入皮质类固醇为基础,但它们容易出现严重的不良反应,尤其是在青少年中。 长期使用也会产生耐药性。 SM17的引入有望在疗效和安全性的平衡方面提供更好的治疗选择。
华诺生物董事长、执行董事兼首席执行官梁瑞安博士表示:“继国家药监局受理SN1011治疗多发性硬化的IND申请后,FDA全面受理SM17 IND申请。表明公司新药研发计划的有效执行。对于额外的有效疗法,尤其是对当前治疗无反应的患者,仍有未满足的医疗需求。因此,我们对 SM17临床开发的巨大前景充满信心。我们的核心SM03、SN1011、SM17等产品的临床研发进展顺利,推动公司稳步迈向商业化。未来,我们将加快项目落地,以创新造福患者,为股东创造价值。”
关于 SM17
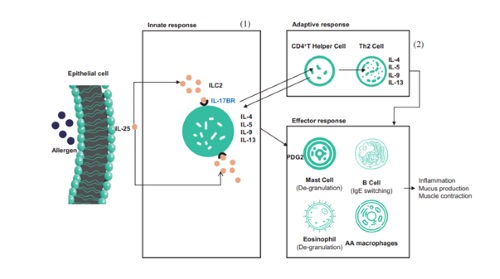
众所周知,SM17 是世界上第一个针对 IL-4RB 的用于新药开发的人源化 IgG17-k 单克隆抗体。 而IL-17RB是属于IL-17受体家族的I型单跨膜糖蛋白。 SM17 与 IL-17RB 的结合可以抑制由一类称为“alarmin”的细胞因子诱导的 Th2 免疫反应,这已被证明与过敏性疾病的发病机制和气道病毒反应有关。 针对 Th2 炎症级联反应的上游介质的替代方法,例如“alarmins”,预计对气道炎症有更广泛的影响,并提供比目前可用的治疗更有效的哮喘控制,并且与 SM17 具有相似作用机制的产品已经经美国食品药品监督管理局批准。
关于SinoMab BioScience Limited
SinoMab BioScience Limited(股票代码:3681.HK)致力于免疫疾病治疗药物的研究、开发、制造和商业化。 公司的旗舰产品SM03是治疗类风湿性关节炎(RA)的潜在全球首个靶向CD22单克隆抗体,目前正在中国进行类风湿性关节炎的III期临床试验,被公认为重要的特殊药物之一。 “十二五”和“十三五”重大新药开发项目。 此外,公司还拥有其他潜在的首创和首创候选药物,其中部分已进入临床阶段,适应症包括类风湿关节炎(RA)、系统性红斑狼疮(SLE)、寻常型天疱疮(PV)、非霍奇金淋巴瘤 (NHL)、哮喘和其他主要未满足临床需求的疾病。
版权所有 2022 ACN 新闻专线。 版权所有。 www.acnnewswire.comSinoMab BioScience Limited(“SinoMab”或“公司”,连同其附属公司统称“集团”,股票代码:3681.HK),一家致力于研究、开发、制造的香港生物制药公司治疗免疫疾病的疗法和商业化