华盛顿特区 - 胰腺癌是最致命的癌症类型之一——在美国,据估计 超过88% 的人将在诊断后五年内死于这种疾病。 这种黯淡预后的原因之一是,大多数胰腺癌是在疾病已经扩散或转移到身体其他部位后才被诊断出来的。 另一个原因是胰腺癌的治疗特别具有挑战性,因为这些肿瘤通常对标准抗癌药物具有耐药性。
国立生物医学影像与生物工程研究所(尼比布) 受资助的研究人员正在开发一种治疗这种致命疾病的新方法。 他们的 根据一项研究,,最近发表于 自然生物医学工程,在多种胰腺癌小鼠模型中将可注射放射性凝胶与全身化疗相结合。 该治疗导致所有评估模型中的肿瘤消退,这对于这种遗传多样性和侵袭性癌症类型来说是前所未有的结果。
NIBIB 发现科学与技术部门主任 David Rampulla 博士表示:“放射治疗通常是在外部进行的,这会使健康组织暴露在辐射下,并限制肿瘤接受的剂量,最终限制其有效性。” “这项临床前研究中研究的放射性生物材料可以直接注射到肿瘤中,从而实现局部治疗。 更重要的是,这种可生物降解的生物材料允许比其他植入式放射治疗更高的累积辐射剂量。”
近距离放射治疗(将放射源放置在体内)可用于治疗几种不同类型的癌症。 例如,早期前列腺癌可以通过“种子”近距离放射治疗进行治疗,即将许多含有放射性物质的微小金属种子植入前列腺。 虽然这些种子可以限制健康组织暴露在辐射下,但它们的金属外壳可以防止使用强效辐射粒子(称为α和β发射体),这些粒子可以更有效地杀死癌细胞。 此外,由于种子体积小,前列腺癌治疗通常需要大约 100 颗种子(每个种子都需要注射)。 迄今为止,近距离放射治疗方法尚未改善胰腺癌患者的临床结果。
目前的研究正在研究一种新型的近距离放射治疗。 研究作者正在研究使用直接注射到肿瘤中的放射性生物聚合物,而不是使用金属种子或导管来提供辐射。 除了可生物降解之外,生物聚合物还具有独特的特性——它经过精心设计,可在室温下从液体转变为加热至体温时的凝胶状状态。 当生物聚合物凝固时,它会留在肿瘤内,并且不容易扩散到周围的健康组织中。
“我们的生物聚合物源自弹性蛋白,这是一种在我们全身的结缔组织中发现的丰富蛋白质,”在杜克大学进行这项工作的第一作者 Jeff Schaal 博士解释道。 “通过修改这种生物聚合物的成分,我们可以控制它从液体转变为凝胶的精确温度。 而且由于我们没有将放射性聚合物包裹在保护性金属种子中,因此我们可以使用不同且更有效的同位素,从而使我们能够提供比传统种子近距离放射治疗更高的辐射剂量。”
这种概念验证治疗中使用的放射性同位素是碘 131(或 I-131),它会释放被称为 β 粒子的高能粒子。 β 粒子会造成 DNA 损伤并杀死受辐射的细胞,但它们不能传播很远,只能传播几毫米(因此脱靶毒性有限)。 Schaal 说,I-131 已用于治疗甲状腺癌数十年,并且具有完善的安全性。
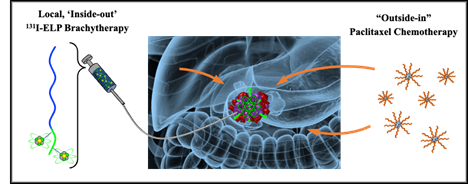
本研究评估了临床前治疗方案。 将放射性生物聚合物(131I-ELP,其中ELP代表弹性蛋白样多肽)注射到胰腺肿瘤中,并全身递送放射增敏化疗药物紫杉醇。 图片来源:Chilkoti 实验室。
胰腺癌有时会结合放疗和特定化疗药物进行治疗,以使放疗更有效。 Schaal 解释说,这些“放射增敏”药物通过延长细胞的复制过程发挥作用,特别是当其 DNA 暴露时。 暴露的DNA对辐射更敏感,更有可能受到辐射造成不可挽回的损害,最终导致细胞死亡。
与放射增敏化疗药物紫杉醇相结合,研究作者在几种不同的胰腺癌模型中评估了其放射性生物聚合物,这些模型经过精心选择,以反映胰腺癌的不同方面(例如常见突变、肿瘤特征、肿瘤密度或治疗耐药性)。 在所有测试的模型中,几乎每只小鼠都有反应,这意味着肿瘤缩小或完全消失。 “我们在模型中看到的响应率是前所未有的,”沙尔说。 “在对文献进行彻底审查后,我们尚未找到另一种治疗方案,能够在多种遗传多样性的胰腺癌模型中表现出如此强劲的反应。” 此外,在一些小鼠中,肿瘤在研究过程中从未复发。
当研究作者评估当前的临床治疗方案(紫杉醇加外照射)时,反应率并不那么令人印象深刻:肿瘤生长速度仅被抑制,而不是肿瘤缩小或消失。 “与短时间进行的外部束辐射不同,我们的近距离放射治疗方法持续提供辐射,”Schaal 解释道。 “我们发现这种连续的β粒子辐射改变了肿瘤的微环境,使紫杉醇能够更好地渗透到肿瘤核心,从而产生协同治疗效果。”
重要的是,研究人员在研究过程中没有观察到任何急性毒性问题,小鼠关键器官中积累的放射性量可以忽略不计。 他们有 先前报道 他们的放射性生物聚合物可以安全地生物降解——凝胶的半衰期(大约 95 天)远远超过 I-131 的半衰期(大约 XNUMX 天)。
作者没有评估他们对转移性疾病的治疗,但他们的方法的性质将允许在多个位置注射生物聚合物,例如其他器官的肿瘤块。 虽然这项研究仍处于临床前阶段,但研究作者正在努力推动这种治疗方法的发展。 “我们的团队一直在与临床研究人员合作,开发和优化我们的系统,以便在更大的动物模型中进行内窥镜引导递送,”杜克大学生物医学工程系教授、资深作者 Ashutosh Chilkoti 博士说。 “然而,将这种疗法或任何新疗法带给患者的挑战是找到支持以使其通过临床试验。”
这项研究得到了 NIBIB (R01EB000188) 和美国国家癌症研究所 (NCI;R35CA197616) 的资助。
(三)美国国立卫生研究院