肿瘤可以通过多种方式被消灭。 放射治疗使用电离辐射束来损伤 DNA 并破坏肿瘤细胞。 一种不太常见的方法是光动力疗法,它使用光激活药物通过线粒体损伤来杀死癌细胞。 然后是新兴的放射动力疗法(RDT)技术。
“放射动力疗法是放射疗法与光动力疗法的结合,”解释道 马查理 福克斯蔡斯癌症中心在最近的会议上发言 AAPM年会.
光动力疗法通常使用可见激光来激活优先定位于肿瘤细胞内的光敏药物。 活化的药物产生高细胞毒性的单线态氧,导致细胞死亡。 然而,激光对组织的穿透力有限,这意味着该技术主要用于治疗浅表肿瘤或内窥镜进入的部位。 为了治疗光动力疗法无法到达的深部肿瘤,RDT 使用高能光子束来激活光敏剂。
“在 RDT 中,我们使用了放射治疗剂量的 20% 到 30%,”Ma 解释道。 “然后我们还使用切伦科夫灯。” 他指出,这种切伦科夫辐射是在放射治疗期间治疗光束与患者组织相互作用时产生的,其光分布与治疗辐射剂量分布几乎相同,因此可以轻松规划。
除了在原发肿瘤中积聚外,药物还会被分布的转移细胞吸收,使用极低剂量的切伦科夫光即可杀死这些细胞。 “现在,RDT 第一次使放射治疗不再是局部和区域性的,而是一种全身治疗技术,”马说。
Fox Chase 的团队正在使用一种名为 5-氨基乙酰丙酸 (5-ALA) 的药物进行 RDT。 5-ALA 被癌细胞中的线粒体吸收,肿瘤中的吸收量是正常组织的 10 至 20 倍。 一旦进入癌细胞,5-ALA 就会代谢成原卟啉 IX (PpIX),这是一种吸收光谱峰值在 380-430 nm 左右的光敏剂。 这对于常用于光动力治疗的红色激光来说并不理想。 然而,它与 370-430 nm 处的切伦科夫吸收峰非常匹配。
临床前证明
在过去的几年中,马和他的团队使用不同的肿瘤细胞系和各种辐射能量进行了许多临床前研究。 他分享了一项大型研究(数百只动物)的一些结果,该研究使用 100 mg/kg 5-ALA 和 6、15 或 45 MV 光子照射来评估荷瘤小鼠的 RDT。
马指出,该肿瘤具有高度侵袭性,仅 4 Gy 的放疗只能杀死约 10% 的肿瘤细胞。 此外,6MV的RDT并没有显着增加治疗效果。 “这就是为什么人们担心切伦科夫光不够,”他指出。 “但是对于 15 和 45 MV,您会看到更多的肿瘤生长延迟。 我们仍在研究为什么能量会产生这种巨大的变化,我们需要找到其背后的确切机制。”
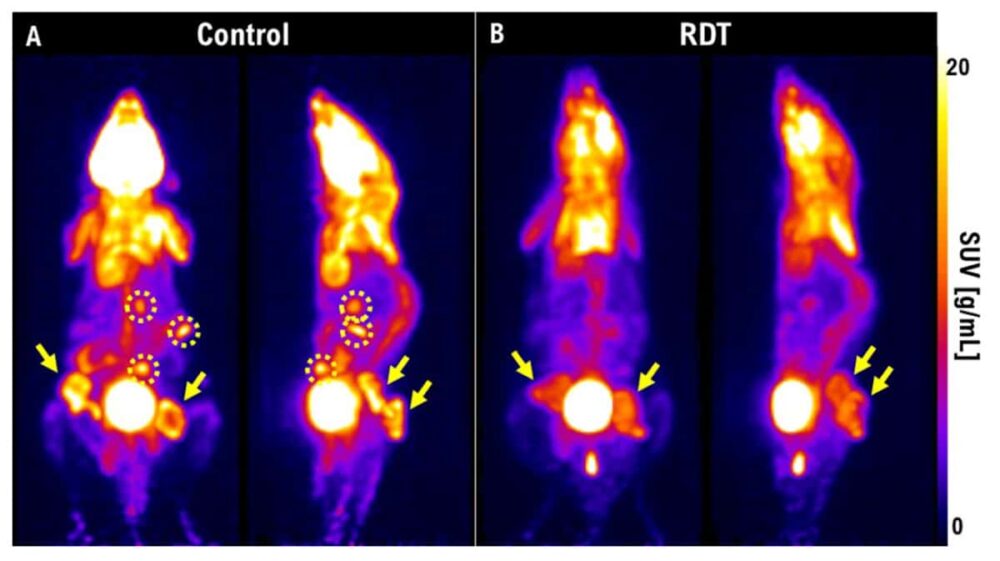
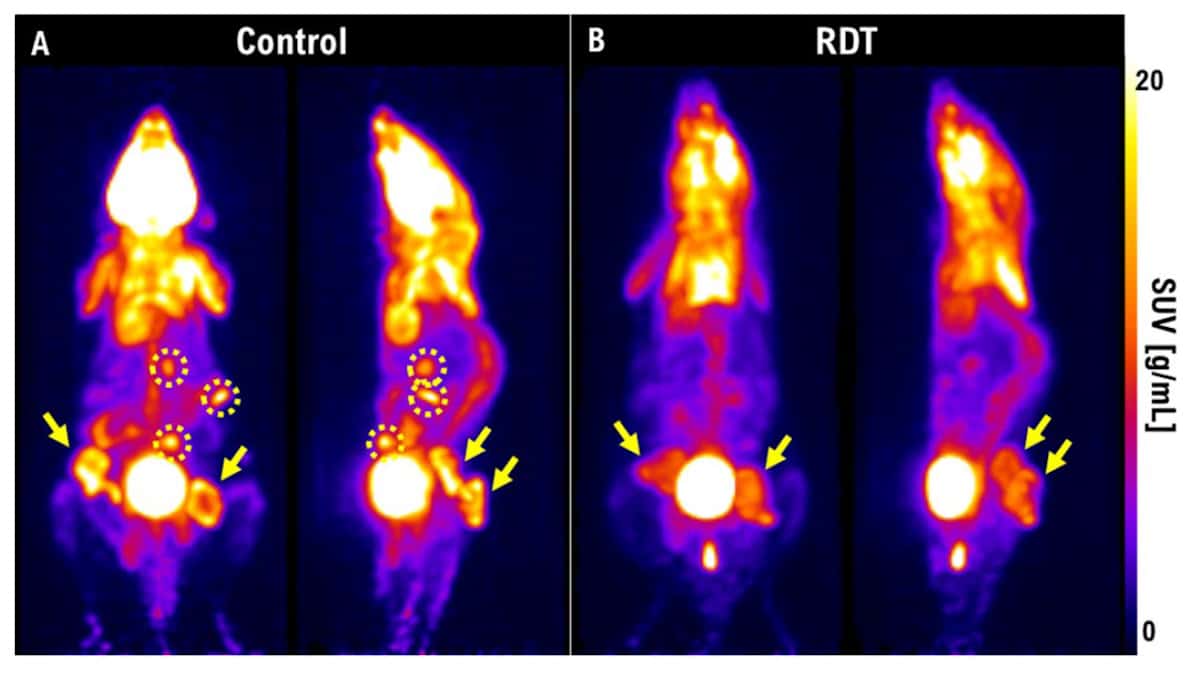
研究小组使用 PET 来观察 RDT 后肿瘤缩小的情况。 治疗一周后,对照小鼠的肿瘤已经生长并转移,而接受 RDT 治疗的小鼠的病灶要小得多,并且没有转移。 马还描述了一项针对兔子的高度侵袭性甲状腺癌的研究。 3Gy放疗一周后,肿瘤仍在生长。 “但如果我们使用 3 Gy 的 RDT 和 5-ALA,PET 图像上就看不到肿瘤。” 他强调,PET 提供了一种进行早期治疗评估的极好方法,可以帮助确定 RDT 对患者是否有效。
Fox Chase 目前正在进行 RDT 临床试验,该研究的第一阶段研究晚期肿瘤的剂量递增(辐射剂量和药物剂量)。 马说,这一阶段现已达到最终剂量水平,只剩下三名患者。他指出,到目前为止,在任何情况下都没有发生任何毒性反应。 在其他地方,明斯特大学医院的第二项 RDT 试验正在检查胶质母细胞瘤首次复发的患者。
现实生活中的案例
最后,马云展示了一些现实案例的结果。 “看到这些你会很兴奋,”他告诉观众,并指出“通常,除非你用 CT、MR 或 PET 进行一个月的成像,否则人们不会相信它有效”。
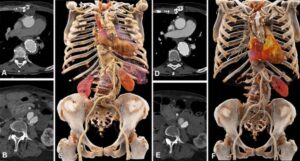
在第一个例子中,肝转移的治疗,他表明 RDT 一个月后,PET 成像显示没有肿瘤残留。 接下来,他介绍了一个患有转移性肺癌的病例:“您可以看到 RDT 后肿瘤失活的非常显着的结果,”他说。
植入式设备提供个性化的光动力治疗
其他成功的 RDT 治疗包括食道癌、多发骨转移的肺部肿瘤,以及化疗失败但 RDT 三天后反应良好的患者。 马指出,大多数患者患有晚期癌症,并且其他治疗均失败。 “我们确实看到了效果,所以希望我们能够提高他们的生存率,”他补充道。
“RDT 可以是结合放射疗法和光动力疗法的局部、区域和全身治疗,”马总结道。 “我们有很多 细胞/组织 和 体内 实验来证明它的治疗潜力,虽然临床试验很少,但我希望我们将来能有更多的结果,并将其变成真正有用的东西。”
- :具有
- :是
- :不是
- $UP
- 10
- 100
- 15%
- 20
- 30
- a
- 关于
- ACCESS
- 添加
- 增加
- 后
- 侵略性
- AL
- 单
- 还
- 尽管
- an
- 和
- 动物
- 全年
- 任何
- 的途径
- 保健
- 围绕
- AS
- 评估
- At
- 听众
- BE
- 光束
- 背后
- 相信
- 骨
- 都
- 但是
- by
- 被称为
- CAN
- 癌症预防
- 癌细胞
- 不能
- 案件
- 例
- 原因
- 细胞
- Center
- 更改
- 追逐
- 界
- 点击
- 临床资料
- 临床试验
- 组合
- 结合
- 相当常见
- 总结
- 控制
- 可以
- 一年中的
- 死亡
- 延迟
- 提供
- 演示
- 描述
- 摧毁
- 销毁
- 确定
- 设备
- DID
- 不同
- 分布
- 分配
- 的DNA
- do
- 别
- 显着
- 药物
- 两
- ,我们将参加
- 早
- 容易
- 效果
- 有效
- 别处
- 新兴经济体的新市场。
- 强调
- 能源
- 升级
- 评估
- 检查
- 例子
- 优秀
- 兴奋
- 实验
- 解释
- 失败
- 远
- 少数
- 最后
- 找到最适合您的地方
- 姓氏:
- 第一次
- 以下
- 针对
- 狐狸
- 止
- 未来
- 产生
- 产生
- 非常好
- 大
- 更大的
- 成长
- 长大的
- 事业发展
- 民政事务总署
- 治理
- 有
- he
- 帮助
- 高度
- 他的
- 抱有希望
- 希望
- 但是
- HTTPS
- 百
- i
- 理想
- 相同
- if
- 图片
- 图片
- 同步成像
- 改善
- in
- 包括
- 增加
- 表明
- 信息
- 内
- 交互
- 成
- 问题
- IT
- 它的
- JPG
- 只是
- 杀
- 大
- 激光器是如何工作的
- 名:
- 左
- 减
- Level
- 光
- 有限
- 线
- 肝
- 本地
- 占地
- 低
- 主要
- 使
- 制作
- 许多
- 匹配
- 最大宽度
- 手段
- 机制
- 线粒体
- 月
- 更多
- 最先进的
- mr
- 许多
- 多
- 需求
- 下页
- 没有
- 正常
- 注意到
- 注意
- 现在
- 数
- 发生
- of
- 经常
- on
- 一旦
- 一
- 仅由
- 打开
- or
- 其他名称
- 输出
- 氧
- 病人
- 患者
- 高峰
- 渗透
- 员工
- 为
- 演出
- 执行
- 执行
- 个性化你的
- 相
- 物理
- 物理世界
- 计划
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 加
- 潜力
- 呈现
- 小学
- 提供
- 放射治疗
- 达到
- 达到
- 真
- 最近
- 复发
- 红色
- 区域性
- 保持
- 响应
- 成果
- 揭密
- 说
- 其次
- 看到
- 看到
- 几个
- 共用的,
- 显示
- 显著
- 网站
- 小
- So
- 至今
- 一些
- 东西
- 发言
- 光谱
- 仍
- 研究
- 学习
- 留学
- 成功
- 足够
- 生存
- 系统的
- 拍摄
- 团队
- 比
- 这
- 未来
- 其
- 然后
- 那里。
- 博曼
- Free Introduction
- 那些
- 三
- 缩略图
- 从而
- 次
- 时
- 至
- 治疗
- 治疗
- 试用
- 试验
- true
- 一般
- 大学
- 使用
- 用过的
- 使用
- 运用
- 各个
- 非常
- 通过
- 可见
- 是
- 方法..
- 方法
- we
- 周
- 是否
- 这
- 而
- 为什么
- 将
- 中
- 合作
- 世界
- 担心
- 将
- 年
- 完全
- 和风网