光学散射是生物成像的一个现实问题。通过防止光线深入聚焦到生物组织中,散射效应将成像深度限制在 100 微米左右,超出后仅产生模糊图像。一种称为超声诱导光学透明显微镜的新技术可以将这个距离增加六倍以上,这要归功于在成像区域插入一层气泡的有点违反直觉的步骤。添加该气泡层可确保光子在穿过样品传播时不会偏离。
当光与小于其波长的结构相互作用时,就会发生光学散射。入射光扰动结构中的电子,形成振荡偶极矩,从而在许多不同方向重新发射光。
“共焦显微镜等技术广泛应用于生命科学研究,例如癌症和脑组织成像,但由于这个问题,它们受到限制,”解释道 张振浩 在 地理信息系统 (大邱庆北科学技术学院)在韩国。 “成像深度的限制主要是由于光学散射导致入射光子严重偏离其原始传播方向。事实上,非散射光子的数量随着光子行进的距离呈指数减少,因此光在大约 100 微米的深度后就无法紧密聚焦。”
虽然研究人员已经开发出各种类型的光波前整形技术来解决这一限制,但它们都不能用于拍摄三维图像。这些其他技术也需要高性能光学模块和复杂的光学系统。
气泡云中没有光学散射
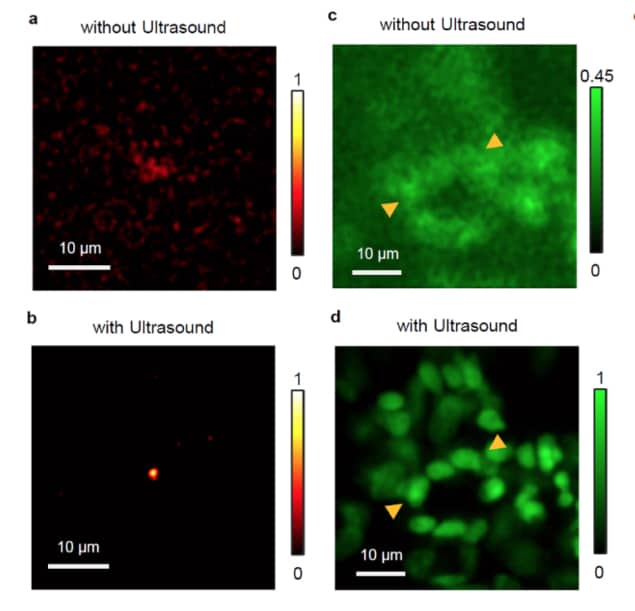
在最新的工作中,Chang 和同事开发了一种新方法,他们使用高强度超声波在位于成像平面前面的组织体积中产生气泡。为了防止气泡破裂并可能损坏组织,研究人员在激光扫描显微镜成像过程中连续发射低强度超声波,始终保持气泡的连续通量。他们发现,当体积中气泡的浓度高于 90% 时,来自成像激光器的光子在气泡区域(称为“气泡云”)内几乎不会经历任何光学散射。这是因为临时产生的气泡减少了与入射光传播方向相同的光学散射,从而增加了其穿透深度。
“因此,激光可以紧密聚焦在成像平面上,超出该成像平面,传统激光扫描显微镜就无法获取清晰的图像,”Chang 说道 物理世界。 “这种现象类似于基于化学试剂的光学透明,因此我们将我们的方法命名为超声诱导光学透明显微镜(US-OCM)。”
与传统的光学清除方法不同,UC-OCM 可以将光学清除定位在感兴趣的区域,并在气泡通量关闭后恢复该区域的原始光学特性。这意味着该技术应该对活组织无害。
据研究人员称,他们详细介绍了他们的工作 自然 光电子US-OCM的主要优点是:成像深度增加六倍以上,分辨率与传统激光显微镜相似;快速的图像数据采集和图像重建(125 x 403像素的一帧图像仅需403毫秒);以及易于获取的 3D 图像。
这还不是全部:该团队指出,实施新方法只需要在传统的激光扫描显微镜设置中添加一个相对简单的声学模块(单个超声换能器和换能器驱动系统)即可。该技术还可以扩展到其他激光扫描显微镜技术,例如多光子和光声显微镜。
超声波和光易于结合
“我个人认为,混合技术的发展是新的研究方向之一,超声波和光相对容易结合起来,以最大限度地发挥各自的优势,同时互补彼此的劣势,”张说。 “从事超声波领域工作的研究人员很早就知道,强超声波可以在生物组织中产生气泡,并且气泡可以完全消失而不损坏组织。”

Kerker 散射以亚原子精度定位粒子
这个实验的想法是在与团队成员、DGIST 光学专家 Jae Youn Hwang 讨论时提出的。人们的想法是,如果超声波诱导的气泡能够以某种方式在感兴趣的区域产生密集的气泡,那么它们就可以用作光学清除剂。 “传统的光学透明技术依赖于这样一个事实:当组织中的光散射体的折射率彼此相似时,光学散射最小,”Chang 解释道。 “采用化学试剂来降低散射体的高折射率,使其接近组织本身的折射率。”
DGIST团队表示,该技术与内窥镜技术相结合,可能用于高分辨率脑组织成像、阿尔茨海默病的早期诊断以及癌组织的精确诊断。 “我还相信这项研究的基本概念可以应用于光学疗法,例如光热疗法和光动力疗法,以提高其疗效,因为它们也受到光穿透有限的影响,”张说。