في غضون أشهر قليلة، تجربة سريرية جريئة قد يقلل بشكل أساسي من خطر الإصابة بالنوبات القلبية لدى الأشخاص الأكثر ضعفًا. إذا سارت الأمور على ما يرام ، فستأخذ لقطة واحدة فقط.
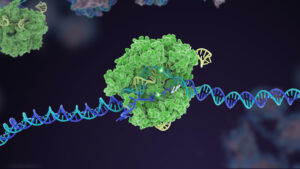
إنها ليست لقطة عادية. المحاكمة بقيادة علاجات الفيرف، وهي شركة للتكنولوجيا الحيوية مقرها ماساتشوستس ، ستكون واحدة من أوائل الشركات التي تختبر محررات القواعد الجينية مباشرة داخل جسم الإنسان. أحد أشكال أداة تحرير الجينات CRISPR-Cas9 ، المحررات الأساسية ارتفعت إلى النجومية عندما قدم لأول مرة لكفاءتها في استبدال الحروف الجينية الفردية دون كسر خيوط الحمض النووي الحساسة. لأنه أكثر أمانًا من الإصدار الكلاسيكي من كريسبر، أثارت الأداة الجديدة الأمل في إمكانية استخدامها في علاج الأمراض الوراثية.
لاحظ الرئيس التنفيذي لشركة Verve ، الدكتور Sekar Kathiresan. تساءل طبيب القلب في جامعة هارفارد ، كاثيريسان عما إذا كان تعديل القاعدة يمكن أن يساعد في حل أحد الأسباب الرئيسية للفتاة في عصرنا: النوبات القلبية. بدت حالة الاختبار المثالية. نحن نعلم أحد الأسباب الرئيسية للنوبات القلبية - ارتفاع مستويات الكوليسترول ، خاصةً نوع يسمى LDL-C (كوليسترول البروتين الدهني منخفض الكثافة). نحن نعرف أيضًا العديد من الجينات الرئيسية التي تتحكم في مستواه. والأهم من ذلك ، نحن نعرف أن تبادل حروف الحمض النووي يمكنه ، من الناحية النظرية ، خفض LDL-C بشكل كبير وبالتالي تقليل مخاطر الإصابة بالنوبات القلبية.
هناك مشكلة واحدة فقط: نحن لا نعرف كيف سيتصرف المحررون الأساسيون داخل جسم بشري حي.
رقصة الكوليسترول
يشبه LDL-C قطعة دهنية من العلكة مع قليل من البروتين الممزوج بها. وعادة ما تدور في الدم ، ويتم سحبها في النهاية داخل الخلايا في "سفن" تشبه الفقاعات وتؤكل في حجرة مليئة بالحمض (نعم ، بيولوجيا الخلية غريبة بشكل مذهل). فويلا - يحتوي مجرى الدم على كمية أقل من المادة الدهنية.
ولكي يحدث هذا ، يحتاج LDL-C إلى الالتحام بالخلية. نقطة الالتحام تسمى بشكل مناسب LDLR ، مع "R" للمستقبل. مثل ساحة الشحن الفعالة ، تتحكم الخلية في عدد الأحواض المتوفرة اعتمادًا على مستوى LDL-C. إذا لم يكن هناك ما يكفي من الكوليسترول ، فإن الخلية توجه "المعالج" ، PCSK9 ، لتدمير الأحواض.
لكن يمكن أن يصبح PCSK9 مفرط الحماس في بعض الأحيان. بدون وجود عدد كافٍ من الأحواض ، لن يكون لدى LDL-C ما يمسك به ويتراكم داخل مجرى الدم. في نهاية المطاف ، تتشبث بجدران الأوعية الدموية وتكوِّن قشرة سيئة ، مما يضيق البنية التحتية لإمداد الدم ويزيد من خطر الإصابة بنوبة قلبية أو سكتة دماغية. يتم طرح العملية برمتها في حالة فرط كوليسترول الدم العائلي (HeFH) ، حيث يتغير حرف الحمض النووي في PCSK9 ، مما يؤدي بدوره إلى ارتفاع الكوليسترول - غالبًا إلى مستوى يهدد الحياة.
كان PCSK9 في مرمى العلماء منذ عقود. تعتبر العقاقير المخفضة للكوليسترول خيارًا شائعًا ، لكنها تستهدف فقط الأعراض - ارتفاع الكوليسترول - دون معالجة المشكلة الجينية الأساسية. تمت الموافقة على العديد من الأدوية ، مثل الأجسام المضادة التي تمنع عملها ، من قبل إدارة الغذاء والدواء في عام 2015. وهناك خيار آخر لإيقاف التعبير الجيني وهو الحمض النووي الريبي الصغير المتداخل ، والذي تم طرحه في الأسواق في عام 2021. ومع ذلك ، يتطلب كلا العلاجين الحقن المتكرر—بعضهم في عيادة الطبيب — مما يجعلهم يعانون مدى الحياة. كما أنها ليست مصممة لأكبر عدد من الأشخاص المعرضين لخطر الإصابة بالنوبات القلبية.
بدلاً من الاستثمار مدى الحياة ، هل هناك طريقة للذهاب لجرعة واحدة وفعلها لأمراض القلب؟
نجاح رئيسيات
في عام 2021 ، كاثيريسان قام بخطوة جذرية: ننسى العلاجات العابرة - دعونا نستهدف المصدر.
من خلال الاستفادة من محرري قاعدة CRISPR ، اعتمد فريقه على عمل سابق في الفئران وأظهرت أن حقنة واحدة من المحرر الأساسي ، المسمى ABE8.8 ، يمكن أن تقلل مستويات كوليسترول PCSK9 و LDL في قرود المكاك الصحية.
العلاج عمل فني. يحتوي على مكونين تم تصنيعهما بسهولة وبتكلفة زهيدة: mRNA الذي يجعل محرر القاعدة داخل الجسم ، ودليل RNA (gRNA) لتوجيه محرر القاعدة إلى بقعة الحمض النووي الصحيحة. ثم غُلّفت المكونات داخل جسيم نانوي شحمي - في الأساس عبارة عن فقاعة دهنية - وحُقنت في مجرى الدم لدى القرود.
على عكس علاجات كريسبر الكلاسيكية ، التي تتطلب عادةً فيروسًا لتتأرجح ، تعتبر الجسيمات النانوية الدهنية أكثر أمانًا من حيث أنها لا تحمل خطر الاندماج في الجينوم. كما يتم تناولها بسهولة عن طريق الكبد. كمصدر رئيسي لعملية التمثيل الغذائي للكوليسترول ، فإن الكبد هو المرشح المثالي لاختبار محرر الجينات وآلية التوصيل.
باستخدام حقنة واحدة فقط ، كان للعلاج تكرار 63 بالمائة في تعديل جين PCSK9. بعد أسبوعين ، انخفضت مستويات الكوليسترول في القردة بأكثر من النصف. إنها ليست مجرد صورة عابرة ، ولكنها تفادي: بعد ثمانية أشهر ، كان لدى القرود 10 في المائة فقط من مستويات PCSK9 السابقة ومستوى منخفض من الكوليسترول. كما أظهرت الخزعات واختبارات الدم أن القردة تعاني من آثار جانبية قليلة.
كان محرر الجينات أيضًا محددًا بشكل صادم. في شاشة واحدة ، ظهر موقع DNA واحد فقط للتحرير خارج الهدف. ومع ذلك ، قد يكون الموقع خاصًا بالقردة ، ولم يتم الإبلاغ عنه مطلقًا كمشكلة في الاختبارات التي أجريت على خلايا الكبد البشرية.
إنه مثال مثير على "الإمكانات العلاجية الهائلة لتعديل قاعدة CRISPR ،" محمد الدكتورة إيفا فان رويج من معهد هوبريشت بهولندا ، والتي لم تشارك في الدراسة ، في ذلك الوقت. بالطبع ، يجب معالجة المخاوف المتعلقة بالطفرات غير المستهدفة ، والاستمناع ، واستهداف الأعضاء. ومع ذلك ، مع التقدم السريع في الأنظمة القائمة على كريسبر ، يبدو الأمر مجرد مسألة وقت قبل أن تفوق مزايا التحرير الجينومي الدقيق عيوب الانتقال إلى الترجمة السريرية ".
نقلة نوعية
قد يبدو تحرير الجينات مباشرة داخل جسم الإنسان لمنع النوبات القلبية أمرًا شديدًا. لكن الفريق لديه سبب لمتابعة استراتيجية واحدة وفعلت.
النوع الرئيسي من خلايا الكبد له عمر طويل نسبيًا. وهذا يعني أن "الإدارة لمرة واحدة لمكونات تحرير الجينات لتثبيط وظيفة PCSK9 بشكل دائم في الكبد يمكن أن تكون فعالة لعقود ، وتحسين نوعية الحياة وتقليل تكاليف الرعاية الصحية ،" محمد من الأحمر.
ليست Verve الشركة الوحيدة التي تتطلع إلى تحول نموذجي لأمراض القلب. دراسة أخرى في الوقت نفسه ، بقيادة الدكتور جيرالد شوانك من جامعة زيورخ ، اتخذ نهجًا مشابهًا لتحرير قاعدة CRISPR ووجد انخفاضًا بنسبة 26 بالمائة في مستويات PCSK9 بعد شهر ، مما زاد فعاليته بعد جرعة ثانية. دراسة أخرى أخذ استهداف PCSK9 مسارًا مختلفًا باستخدام أليغنوكليوتيدات مضادة المعنى (ASO) ، وهي سلسلة من أحرف الحمض النووي التي تحجب الجين. هنا ، تم تناول العلاج عن طريق الفم بدلاً من الحقن ، مع معدلات اغلاق PCSK9.
بالنسبة لـ Verve ، هناك الكثير من الركوب على التجربة السريرية ، المقرر إجراؤها في نيوزيلندا منتصف عام 2022. إذا نجحت ، فستكون أول تجربة لاستخدام المحررين الأساسيين مباشرة داخل الجسم ، وحلاً دائمًا لإدارة النوبات القلبية. للبدء ، ستجند التجربة فقط الأشخاص المصابين بـ HeFH ، وهو الاضطراب الوراثي الذي يسبب مستويات عالية للغاية من الكوليسترول. تركز المرحلة الأولى بشكل أساسي على السلامة ، على الرغم من أن التحسينات - إن وجدت - قد تظهر أيضًا بعد التحليل. تتوقع Verve النتائج الأولية حوالي عام 2023. وفي الوقت نفسه ، تطلب الشركة أيضًا من المملكة المتحدة والولايات المتحدة الحصول على الضوء الأخضر للتجارب السريرية.
الشركة لديها صراع في المستقبل. على الرغم من أنه تم اعتباره آمنًا في التجارب قبل السريرية على الفئران والقرود ، إلا أن الجهاز المناعي البشري قد لا يزال يهاجم سيارة التوصيل. قد يواجه العلاج أيضًا إحجامًا عن المرضى لأنه يحرر الجينوم مباشرة. يبقى العلاج طويل الأمد والآثار الجانبية غير معروفة. وأخيرًا ، تكلفة العلاج—تقدر بمبلغ 50,000 إلى 200,000 دولار- ستجعله بعيد المنال بالنسبة للبعض. العقاقير المخفضة للكوليسترول ، على سبيل المثال ، يمكن أن تكون منخفضة مثل 29 دولار شهريا، ولكنها تتطلب علاجًا طويل الأمد.
تتطلع Verve بالفعل إلى المستقبل. "سنركز أولاً على البالغين المصابين بمرض تصلب الشرايين القلبي الوعائي الذي يهدد حياتهم (ASCVD) ، ثم سنتوسع ليشمل شريحة أوسع من المرضى المصابين بالمرض ،" محمد.
وفي الوقت نفسه ، يجب أن تدخل التروس القانونية والسداد حيز التنفيذ. إلى الدكاترة. كوين بولوسما وبيتر بوسما في جامعة أمستردام ، الذين علق سابقا في دراسات القرود ، "إن جعل هذه العلاجات المتغيرة للحياة متاحة للمرضى في المستقبل القريب هي مهمة للمنظمين ، وشركات التأمين الصحي ، والحكومات. في ضوء وتيرة هذه التطورات التقنية المثيرة ، سيكون من الصعب عليهم جميعًا مواكبة ذلك ".
الصورة الائتمان: جوليجون / Shutterstock.com
- "
- 000
- 10
- 2021
- اكشن
- الإجراءات
- إدارة
- الكبار
- مزايا
- قدما
- الكل
- سابقا
- أمستردام
- تحليل
- آخر
- نهج
- حول
- فنـون
- متاح
- قبل
- علم الاحياء
- التكنولوجيا الحيوية
- حظر
- دم
- بلومبرغ
- الجسدي
- يبني
- يستطيع الحصول على
- مرشح
- حمل
- سبب
- الأسباب
- الرئيس التنفيذي
- تحدي
- كلاسيكي
- الشركات
- حول الشركة
- يحتوي
- مراقبة
- التكاليف
- استطاع
- ائتمان
- التوصيل
- اعتمادا
- تصميم
- هدم
- التطورات
- مختلف
- مباشرة
- مباشرة
- مرض
- الأمراض
- الحمض النووي
- إلى أسفل
- المخدرات
- بسهولة
- رئيس التحرير
- الطُرق الفعّالة
- الآثار
- كفاءة
- فعال
- مثال
- وسع
- تتوقع
- تمكنت
- أقصى
- الوجه
- ادارة الاغذية والعقاقير
- أخيرا
- الاسم الأول
- تركز
- ركز
- وجدت
- وظيفة
- في الأساس
- مستقبل
- معدّات الأطفال
- الحكومات
- انتزاع
- أكبر
- أخضر
- توجيه
- يحدث
- هارفارد
- صحة الإنسان
- التأمين الصحي
- الرعاية الصحية
- مساعدة
- هنا
- مرتفع
- كيفية
- لكن
- HTTPS
- الانسان
- تحسين
- زيادة
- في ازدياد
- البنية التحتية
- التأمين
- استثمار
- المشاركة
- قضية
- IT
- واحد فقط
- ليد
- شروط وأحكام
- مستوى
- أوقات الحياة
- ضوء
- الذين يعيشون
- طويل
- طويل الأجل
- رائد
- يصنع
- إدارة
- تجارة
- ماساتشوستس
- أمر
- يعني
- مختلط
- شهر
- المقبلة.
- الأكثر من ذلك
- أكثر
- يتحرك
- الطبيعة
- قرب
- إحتياجات
- هولندا
- نيوزيلاندا
- المعاهد الوطنية للصحة
- عدد
- خيار
- نموذج
- خاصة
- مجتمع
- فى المائة
- دائم
- مرحلة جديدة
- قطعة
- البوينت
- أكثر الاستفسارات
- سكان
- محتمل
- المشكلة
- عملية المعالجة
- جودة
- المنحدر
- الأجور
- تخفيض
- تقليص
- بخصوص
- الجهات التنظيمية
- لا تزال
- تطلب
- النتائج
- المخاطرة
- طريق
- خزنة
- السلامة
- علوم
- شاشة
- طقم
- نقل
- الشحن
- شترستوك
- مماثل
- الموقع
- صغير
- So
- حل
- حل
- بعض
- بقعة
- بداية
- الإستراتيجيات
- دراسات
- دراسة
- ناجح
- تزويد
- نظام
- أنظمة
- الهدف
- استهداف
- فريق
- تقني
- تجربه بالعربي
- الاختبار
- اختبارات
- هولندا
- المصدر
- وبالتالي
- الوقت
- مرات
- أداة
- خدمات ترجمة
- معالجة
- علاج
- هائل
- محاكمة
- Uk
- جامعة
- us
- عادة
- المثالية
- المزيد
- فيروس
- الضعيفة
- من الذى
- بدون
- للعمل