En ny type computermodel, der kan afsløre strålingsskader på cellulært niveau, kan forbedre strålebehandlingsresultater for lungekræftpatienter.
Roman Bauer, en computational neuroscientist ved University of Surrey i Storbritannien, i samarbejde med Marker Under , Nicolò Cogno fra GSI Helmholtzzentrum für Schwerionenforschung i Tyskland, skabt modellen, som simulerer, hvordan stråling interagerer med lungerne på celle-for-celle basis.
Over halvdelen af alle patienter med lungekræft behandles med strålebehandling. Selvom denne tilgang er effektiv, efterlader den op til 30 % af modtagerne med strålingsinducerede skader. Disse kan udløse alvorlige tilstande, der påvirker vejrtrækningen, såsom fibrose - hvor slimhinden i alveolerne (luftsækkene) i lungerne bliver fortykket og stivnet - og lungebetændelse - når alveolernes vægge bliver betændt.
For at begrænse strålingsskader på sundt væv, mens de stadig dræber kræftceller, afgives strålebehandling i flere separate "fraktioner". Dette gør det muligt at indgive en højere – og derfor mere effektiv – dosis samlet, fordi nogle af de beskadigede raske celler kan reparere sig selv mellem hver fraktion.
I øjeblikket er strålebehandlingsfraktioneringsskemaer valgt baseret på tidligere erfaringer og generaliserede statistiske modeller, så de er ikke optimeret til individuelle patienter. I modsætning hertil kunne personlig medicin opnås takket være denne nye model, som, som Durante, direktør for Biofysisk afdeling ved GSI forklarer, ser på "toksicitet i væv startende fra de basale cellulære reaktioner og [er] derfor i stand til at forudsige, hvad der sker med enhver patient", når forskellige fraktioneringsskemaer er valgt.
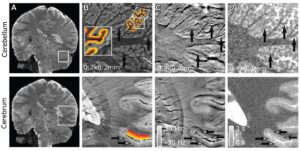
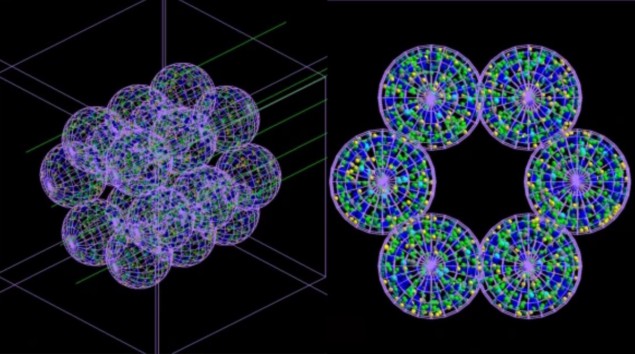
Holdet udviklede en "agent-baseret" model (ABM) bestående af separate interagerende enheder eller midler - som i dette tilfælde efterligner lungeceller - koblet med en Monte Carlo-simulator. ABM, beskrevet i Kommunikationsmedicin, bygger en repræsentation af et alveolært segment bestående af 18 alveoler hver 260 µm i diameter. Dernæst udføres Monte Carlo-simuleringer af bestråling af disse alveoler i mikroskopisk og nanoskopisk skala, og information om strålingsdosis leveret til hver celle og dens fordeling føres tilbage til ABM.
ABM'en bruger denne information til at finde ud af, om hver celle ville leve eller dø, og udsender de endelige resultater i form af et 3D-billede. Det er afgørende, at den koblede model kan simulere tidens gang og dermed vise sværhedsgraden af strålingsskader - og progressionen af de medicinske tilstande, den kan forårsage - timer, dage, måneder eller endda år efter behandlingen.
"Det, jeg fandt meget spændende, er, at disse beregningssimuleringer faktisk leverede resultater, der matchede med forskellige eksperimentelle observationer fra forskellige grupper, laboratorier og hospitaler. Så vores beregningsmæssige tilgang kunne i princippet bruges inden for en klinisk ramme,” siger Bauer, talsmand for det internationale BioDynaMo samarbejde, som har til formål at bringe nye beregningsmetoder ind i sundhedsvæsenet via softwarepakken, der blev brugt til at bygge denne model.
Bauer begyndte at arbejde på beregningsmæssige kræftmodeller, efter at en nær ven døde af sygdommen kun 34 år gammel. "Hver kræft er forskellig, og hver person er forskellig, med forskellige formede organer, genetiske dispositioner og livsstil," forklarer han. Hans håb er, at informationer fra scanninger, biopsier og andre tests kan føres ind i den nye model for at give et billede af hver enkelt person. En AI-assisteret terapiprotokol kunne derefter oprettes, som ville producere en nøje skræddersyet behandlingsplan, der forbedrer patientens chancer for overlevelse.
Patientspecifik planlægning kunne forbedre resultaterne af strålebehandling
Bauer søger i øjeblikket samarbejdspartnere fra andre discipliner, herunder fysik, for at hjælpe med at bevæge sig hen imod et klinisk forsøg efter lungekræftpatienter over flere år. I mellemtiden har holdet til hensigt at udvide modellens anvendelse til andre områder af medicin.
Durante håber for eksempel at studere viral infektion med denne lungemodel, da den "kan forudsige lungebetændelse induceret af COVID-19-infektionen". I mellemtiden er Bauer begyndt at simulere udviklingen af kredsløb i for tidligt fødte børns hjerner med det mål at forstå bedre "på hvilket tidspunkt man skal gribe ind og hvordan".
- SEO Powered Content & PR Distribution. Bliv forstærket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk dig selv. Adgang her.
- PlatoAiStream. Web3 intelligens. Viden forstærket. Adgang her.
- PlatoESG. Kulstof, CleanTech, Energi, Miljø, Solenergi, Affaldshåndtering. Adgang her.
- PlatoHealth. Bioteknologiske og kliniske forsøgs intelligens. Adgang her.
- Kilde: https://physicsworld.com/a/modelling-lung-cells-could-help-personalize-radiotherapy/
- :har
- :er
- :ikke
- $OP
- 135
- 3d
- a
- I stand
- Om
- AC
- opnået
- faktisk
- administreret
- påvirke
- Efter
- alderen
- midler
- målsætninger
- LUFT
- Alle
- tillader
- Skønt
- an
- ,
- enhver
- tilgang
- ER
- områder
- AS
- At
- tilbage
- baseret
- grundlæggende
- grundlag
- BE
- fordi
- bliver
- begyndte
- begyndt
- Bedre
- mellem
- vejrtrækning
- bringe
- bygge
- bygger
- by
- CAN
- Kræft
- Kræftceller
- gennemføres
- tilfælde
- Årsag
- celle
- Celler
- odds
- valgt
- Klinisk
- Luk
- nøje
- samarbejde
- samarbejdspartnere
- beregningsmæssige
- computer
- betingelser
- Bestående
- kontrast
- kunne
- koblede
- Covid-19
- oprettet
- afgørende
- For øjeblikket
- skader
- Dage
- leveret
- Afdeling
- beskrevet
- udviklet
- Udvikling
- Die
- døde
- forskellige
- Direktør
- discipliner
- Sygdom
- fordeling
- dosis
- hver
- Effektiv
- Endog
- Hver
- spændende
- Udvid
- erfaring
- eksperimenterende
- Forklarer
- Fed
- endelige
- efter
- Til
- formular
- fundet
- fraktion
- ven
- fra
- generaliseret
- genetiske
- Tyskland
- mål
- Gruppens
- Halvdelen
- sker
- he
- sundhedspleje
- sund
- hjælpe
- højere
- hans
- håber
- håber
- sygehuse
- HOURS
- Hvordan
- HTTPS
- i
- Forbedre
- forbedrer
- in
- Herunder
- individuel
- oplysninger
- skader
- instans
- hensigt
- interaktion
- interagerer
- internationalt
- intervenere
- ind
- spørgsmål
- IT
- ITS
- jpg
- lige
- drab
- Labs
- Niveau
- livsstil
- GRÆNSE
- foring
- leve
- UDSEENDE
- matchede
- max-bredde
- Kan..
- I mellemtiden
- medicinsk
- medicin
- metoder
- mikroskopisk
- model
- modellering
- modeller
- måned
- mere
- bevæge sig
- Natur
- Ny
- næste
- of
- on
- optimeret
- or
- ordrer
- Andet
- vores
- ud
- udfald
- output
- udgange
- i løbet af
- samlet
- passage
- forbi
- patient
- patienter
- person,
- Tilpas
- Personlig
- Fysik
- Fysik verden
- billede
- fly
- planlægning
- plato
- Platon Data Intelligence
- PlatoData
- Punkt
- forudsige
- For tidlig
- princippet
- progression
- protokol
- give
- Strålebehandling
- reaktioner
- modtagere
- reparere
- repræsentation
- Resultater
- afsløre
- siger
- Scale
- scanninger
- ordninger
- søger
- segment
- adskille
- alvorlig
- indstilling
- flere
- formet
- Vis
- simulere
- simuleringer
- simulator
- So
- Software
- nogle
- talsmand
- Starter
- statistiske
- Stadig
- Studere
- sådan
- suite
- Surrey
- overlevelse
- skræddersyet
- hold
- tests
- Tak
- at
- UK
- selv
- derefter
- terapi
- derfor
- Disse
- denne
- thumbnail
- Dermed
- tid
- til
- mod
- behandlet
- behandling
- retssag
- udløse
- sand
- typen
- Uk
- forståelse
- enheder
- brug
- anvendte
- bruger
- ved brug af
- forskellige
- meget
- via
- viral
- Hvad
- hvornår
- hvorvidt
- som
- mens
- med
- inden for
- Arbejde
- træning
- arbejder
- world
- ville
- år
- zephyrnet