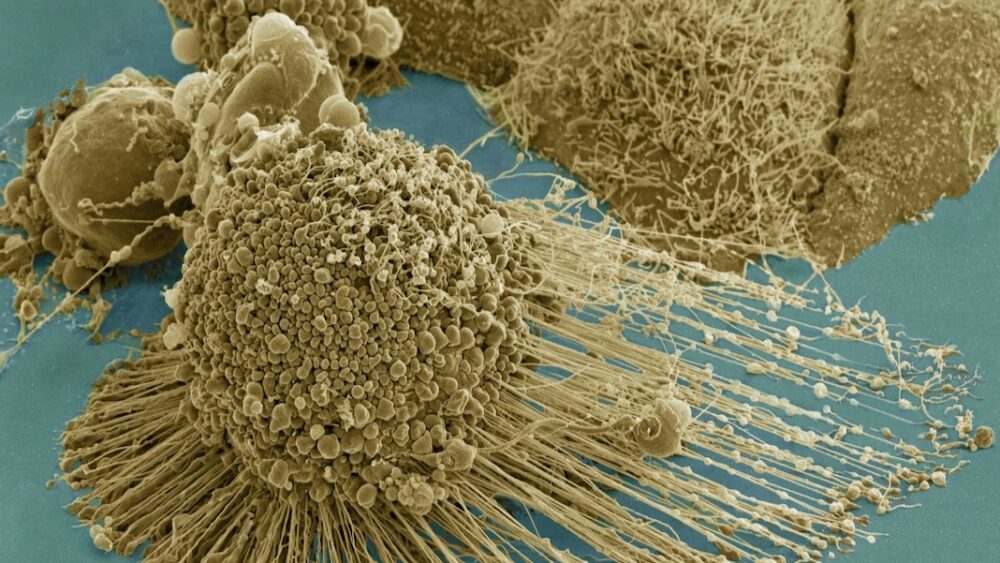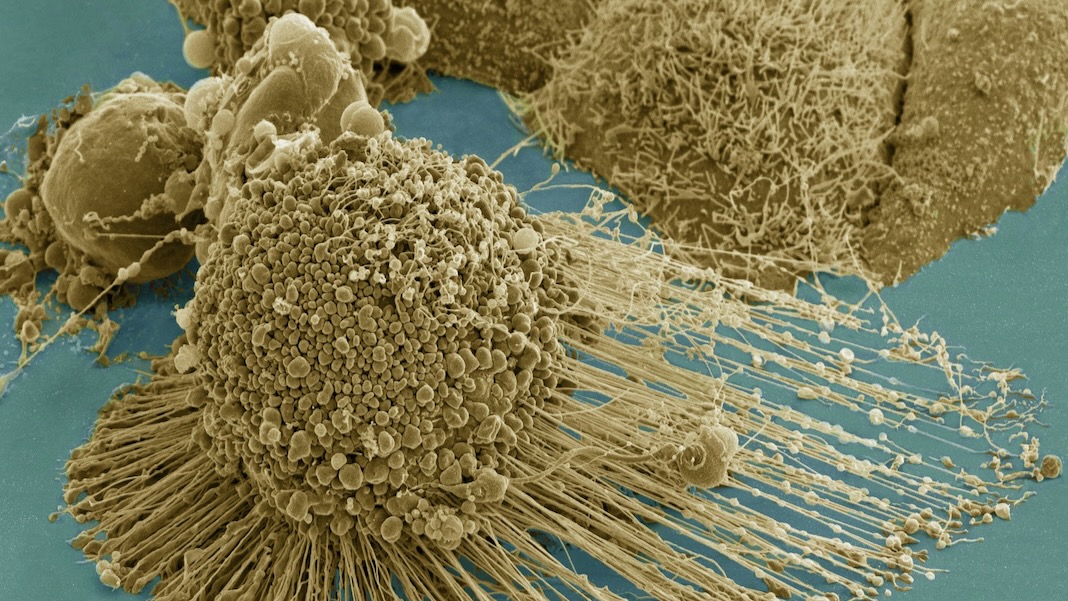
Ældrende celler er biokemiske affaldsfabrikker.
En ny undersøgelse antyder, at en måde at udslette dem på er en medicin, der allerede er godkendt til øjenproblemer.
Kaldt "zombieceller", ældende celler akkumuleres langsomt med alderen eller med kræftbehandlinger. Cellerne mister deres evne til at udføre normale funktioner. I stedet lækker de en giftig kemisk suppe ind i deres lokale miljø, hvilket øger inflammation og beskadiger sunde celler.
Over et årti med forskning har vist at eliminere disse celler med genteknologi eller medicin bremse aldring symptomer hos mus. Det er ikke underligt, at investorer har det skænket milliarder af dollars ind i disse "senolytiske" lægemidler.
Der er allerede antydninger af tidlige succeser. I et tidligt klinisk forsøg blev udrensning af zombieceller med en kombination af lægemidler hos mennesker med aldersrelaterede lungeproblemer fundet at være sikker. En anden undersøgelse hjalp midaldrende og ældre mennesker opretholde blodtrykket mens du løber op ad trapper. Men at kæmpe mod ældningsceller handler ikke kun om at forbedre atletiske evner. Mange mere kliniske forsøg er undervejs, herunder styrkelse af knogleintegritet og bekæmpelse Alzheimers.
Men for Carlos Anerillas, Myriam Gorospe og deres team ved National Institutes of Health (NIH) i Baltimore, har terapier endnu ikke ramt zombieceller, hvor det virkelig gør ondt.
In et studie in Natur aldring, fandt holdet en svaghed i disse celler: De frigiver konstant giftige kemikalier, som en utæt næse under en forkølelse. Kaldet SASP, for senescens-associeret sekretorisk fænotype, bidrager denne gryderet af inflammatoriske molekyler til aldring.
Heldigvis for os har denne konstante frigivelse af kemikalier en pris. Zombieceller bruger en "fabrik" inde i cellen til at pakke og sende deres giftige nyttelast til naboceller og nærliggende væv. Alle celler har disse fabrikker. Men dem i zombieceller går i overdrive.
Den nye undersøgelse fastslog et proteinpar, der er afgørende for zombiecellernes giftige udsug og fandt et FDA-godkendt lægemiddel, der hæmmer processen. Når de blev givet til 22 måneder gamle mus - omtrent det menneskelige ækvivalent til 70 år gamle - havde de bedre nyre-, lever- og lungefunktion inden for kun to måneders behandling.
Værket "skiller sig ud", sagde Yahyah Aman, redaktør på Natur aldring. Det er et "spændende mål for udvikling af nye senolytiske lægemidler," tilføjede Ming Xu ved UConn Health, som ikke var involveret i undersøgelsen.
En molekylær storby
Hver celle er en travl by med flere kvarterer.
Nogle huser vores genetiske arkiver. Andre oversætter disse DNA-koder til proteiner. Der er også syrefyldte containere og molekylær genbrugspapirer for at holde hver celle fri for affald.
Så er der skadestuen. Nej, ikke skadestuen, men en fluffy croissant-lignende struktur. Kaldet det endoplasmatiske reticulum, det er Grand Central for nye proteiner. ER pakker proteiner og leverer dem til interne strukturer, cellens overflade eller destinationer uden for cellen.
Disse "sekretoriske" pakker er kraftfulde regulatorer, der kontrollerer lokale cellulære funktioner. Normalt hjælper ER celler med at koordinere deres reaktioner med tilstødende væv - f.eks. lader blodet størkne efter en skrabe eller stimulerer immunresponser for at helbrede skaden.
Ældrende celler kaprer denne proces. I stedet for produktiv signalering frigiver de i stedet en giftig suppe af kemikalier. Disse celler er ikke født skadelige. Tværtimod bliver de forvandlet af et helt liv med skade - beskadigelse af deres DNA, for eksempel. Stillet over for så megen skade ville normale celler visne væk, hvilket tillod sunde nye celler at erstatte dem i nogle væv som huden.
Zombieceller derimod nægter at dø. Så længe skaden forbliver under et dødeligt niveau, lever cellerne videre, udstøder deres dødbringende bryg og skader andre i nærheden.
Disse egenskaber gør zombieceller til et værdifuldt mål for anti-aldringsterapier. Og der har været lovende behandlinger. De fleste har stolet på eksisterende viden eller ideer om, hvordan zombieceller fungerer. Forskere opsøger derefter kemikalier i massive lægemiddelbiblioteker, der kan forstyrre deres funktion. Selvom denne strategi er nyttig, kan den gå glip af behandlingsmuligheder.
Den nye undersøgelse blev slyngelagtig. I stedet for at starte med hypoteser, screenede de hele det menneskelige genom for at finde nye sårbarheder.
Et vilde vesten
I deres jagt henvendte holdet sig til CRISPR. Berømt kendt som en geneditor, bruges CRISPR nu ofte til at lokalisere gener og proteiner, der bidrager til cellulære funktioner. Her forstyrrede holdet hvert gen i det menneskelige genom for at udpege dem, der eliminerede zombieceller.
Deres arbejde gav pote. Skærmen fandt et proteinpar, der var kritiske for ældende cellers overlevelse. Holdet ledte derefter efter et FDA-godkendt lægemiddel til at forstyrre parret. De fandt, hvad de ledte efter, i verteporfin, et lægemiddel, der er godkendt til behandling af øjenblodkarsygdom.
I adskillige zombiecellekulturer med proteinparret drev stoffet senescerende celler ind i apoptose - det vil sige "blide fald af blade", en slags celledød gør ingen skade på omgivende celler.
Graver man dybere, så stoffet ud til at være direkte målrettet mod zombiecellernes endoplasmatiske retikulum - deres forsendelsescenter. Celler behandlet med lægemidlet kunne ikke opretholde den sarte flerlagsstruktur, og det skrumlede efterfølgende ind i en form som et vådt, krøllet papirhåndklæde.
"En krympet ER udløste en metabolisk krise" i zombieceller, forklarede Anerillas og Gorospe. Det "kulminerede med deres død."
Tidsløse mus
Som et bevis på konceptet injicerede holdet ældre mus - omkring en alder af et 70-årigt menneske - med verteporfin en gang om måneden i to måneder.
På bare en uge viste mus behandlet med verteporfin færre molekylære tegn på alderdom i deres nyre, lever og lunger. Deres pels var mere luksuriøs sammenlignet med kontrolmus uden stoffet.
Når vi bliver ældre, kommer immunceller ofte ind i lungerne og forårsager skade. Verteporfin fjernede denne infiltration og reducerede lungeardannelse hos mus - hvilket ofte er forbundet med nedsat åndedrætskapacitet. På samme måde hjalp stoffet ifølge blodprøver også med at genoprette funktionen i musenes nyrer og lever.
Et fald i antallet af senescerende celler dæmpede inflammatoriske signaler, hvilket kunne forklare de foryngende virkninger, forklarede holdet. Verteporfin stoppede også et "værge"-protein, der beskytter ældende celler mod død, hvilket yderligere udløste deres død.
At udnytte en zombiecelles unikke sårbarheder er en ny strategi i udviklingen af senolytika. Der er meget mere at udforske. Det endoplasmatiske retikulum er ikke den eneste cellekomponent i den biologiske affaldsfabrik. Andre cellulære komponenter, der genererer ældende cellegifte, kunne også blokeres og hjælpe med at fjerne selve cellerne.
Det er et lovende alternativ til eksisterende metoder til at udslette ældre celler. Strategien kunne "i høj grad udvide kataloget af senolytiske terapier," skrev holdet.
Billedkredit: En HeLA-celle, der gennemgår apoptose. Tom Deerinck / NIH / FLICKR
- SEO Powered Content & PR Distribution. Bliv forstærket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk dig selv. Adgang her.
- PlatoAiStream. Web3 intelligens. Viden forstærket. Adgang her.
- PlatoESG. Kulstof, CleanTech, Energi, Miljø, Solenergi, Affaldshåndtering. Adgang her.
- PlatoHealth. Bioteknologiske og kliniske forsøgs intelligens. Adgang her.
- Kilde: https://singularityhub.com/2023/11/07/zombie-cells-have-a-weakness-a-new-anti-aging-therapy-exploits-it/
- :har
- :er
- :ikke
- :hvor
- $OP
- 70
- a
- evner
- evne
- Om
- Ifølge
- Ophobe
- tilføjet
- Efter
- alder
- Aging
- Alle
- tillade
- allerede
- også
- alternativ
- Aman
- an
- ,
- En anden
- godkendt
- arkiv
- ER
- AS
- At
- væk
- Baltimore
- kæmper
- BE
- været
- jf. nedenstående
- Bedre
- milliarder
- blokeret
- blod
- KNOGLE
- født
- vejrtrækning
- travle
- men
- by
- kaldet
- CAN
- Kræft
- Kapacitet
- carlos
- katalog
- Årsag
- Celler
- center
- central
- kemikalie
- By
- Rengøring
- klar
- Klinisk
- kliniske forsøg
- koder
- forkølelse
- bekæmpelse
- kombination
- kommer
- sammenlignet
- komponent
- komponenter
- Konceptet
- konstant
- konstant
- kontrast
- bidrage
- bidrager
- kontrol
- koordinere
- kunne
- kredit
- CRISPR
- kritisk
- skader
- beskadige
- Død
- årti
- er faldet
- dybere
- leverer
- destinationer
- Udvikling
- Die
- direkte
- Sygdom
- Afbryde
- forstyrret
- dna
- gør
- ned
- medicin
- Narkotika
- i løbet af
- hver
- Tidligt
- editor
- effekter
- Ældre
- elimineret
- eliminere
- nødsituation
- Engineering
- Indtast
- Miljø
- Ækvivalent
- væsentlig
- Hver
- eksempel
- eksisterende
- Udvid
- eksperimenterende
- Forklar
- forklarede
- exploits
- udforske
- øje
- konfronteret
- fabrikker
- fabrik
- Faldende
- berømt
- langt
- færre
- Finde
- Til
- fundet
- fra
- funktion
- funktioner
- yderligere
- generere
- genetiske
- genteknologi
- given
- Go
- grand
- havde
- skade
- skadelig
- SKADES
- Have
- Helse
- sund
- hjælpe
- hjulpet
- hjælper
- link.
- hijack
- hints
- Hit
- hus
- Hvordan
- HTTPS
- menneskelig
- Mennesker
- jagt
- gør ondt
- ideer
- forbedring
- in
- Herunder
- stigende
- indvendig
- i stedet
- integritet
- interne
- ind
- Investorer
- involverede
- IT
- lige
- Holde
- nyre
- nyrer
- viden
- kendt
- lække
- Niveau
- biblioteker
- levetid
- ligesom
- forbundet
- leve
- Lever
- lokale
- Lang
- kiggede
- leder
- taber
- luksuriøs
- lave
- mange
- massive
- medicin
- metoder
- måske
- glip af
- molekylær
- Måned
- måned
- mere
- mest
- meget
- flerlagede
- flere
- national
- nationale sundhedsinstitutter
- Natur
- tilstødende
- Ny
- næste
- NIH
- ingen
- normal
- Normalt
- næse
- nu
- numre
- of
- off
- tit
- ældre
- on
- engang
- ONE
- dem
- kun
- Indstillinger
- or
- Andet
- Andre
- vores
- ud
- uden for
- pakke
- pakker
- betalt
- par
- Papir
- Mennesker
- Udfør
- plato
- Platon Data Intelligence
- PlatoData
- vigtigste
- pris
- problemer
- behandle
- produktiv
- lovende
- bevis
- Bevis for koncept
- Protein
- Proteiner
- hellere
- virkelig
- Reduceret
- Regulators
- frigive
- Fjern
- erstatte
- forskning
- forskere
- reaktioner
- genoprette
- Værelse
- kører
- Skærm
- Søg
- syntes
- flere
- Shape
- SKIB
- Levering
- viste
- vist
- signaler
- Skilte
- Tilsvarende
- hud
- langsomt
- So
- nogle
- Starter
- stoppet
- Strategi
- styrkelse
- struktur
- strukturer
- Studere
- Efterfølgende
- foreslår
- overflade
- Omkringliggende
- overlevelse
- Symptomer
- mål
- hold
- tests
- end
- at
- deres
- Them
- selv
- derefter
- Der.
- Disse
- de
- denne
- dem
- til
- omdannet
- Oversætte
- behandle
- behandling
- behandlinger
- retssag
- forsøg
- udløst
- udløsning
- Drejede
- to
- undergår
- enestående
- us
- brug
- anvendte
- Værdifuld
- Beholder
- Sårbarheder
- var
- Affald
- Vej..
- we
- Svaghed
- uge
- gik
- var
- våd
- Hvad
- hvornår
- som
- mens
- WHO
- Hele
- Wikipedia
- Wild
- tørre
- aftørring
- med
- inden for
- uden
- spekulerer
- Arbejde
- virker
- ville
- skrev
- år
- endnu
- zephyrnet
- Zombie