Eine Nierenerkrankung im Endstadium, bei der die Nieren den Bedarf des Körpers nicht mehr decken können, wird am besten durch eine Nierentransplantation behandelt. Allerdings ist das Angebot an Spenderorganen begrenzt und viele Patienten sind stattdessen auf die Dialyse angewiesen. Und obwohl eine Nierentransplantation hervorragende Ergebnisse liefert, erfordert sie vom Patienten die lebenslange Einnahme von Immunsuppressionsmedikamenten, die zu gesundheitlichen Komplikationen führen. Um diese Probleme anzugehen, hoffen Forscher, eine implantierbare bioartifizielle Niere zur Behandlung von Nierenversagen zu entwickeln.
Forscher der UC San Francisco (UCSF) arbeiten an der Entwicklung eines solchen Geräts. In ihrer neuesten Studie, berichtet in Nature Communications veröffentlicht , Sie zeigen, dass Nierenzellen, die in einem implantierbaren Bioreaktor untergebracht sind, im Inneren eines Schweins überleben und mehrere wichtige Nierenfunktionen nachahmen können. Entscheidend ist, dass das implantierte Gerät keine Immunreaktion hervorrief. Die Forschung ist Teil von Das Nierenprojekt, gemeinsam geleitet von UCSFs Shuvo Roy und William Fissell des Vanderbilt University Medical Center.
Als ersten Schritt hin zu einer implantierbaren bioartifiziellen Niere haben Roy, Fissel und Kollegen einen zellhaltigen Bioreaktor entwickelt, der Schlüsselfunktionen des Nierentubulus nachbildet, einschließlich der Zufuhr von Sauerstoff und Nährstoffen zu Nierenzellen und gleichzeitigem Schutz vor Empfängerimmunzellen, die eine Abstoßung verursachen könnten . Um diesen Immunschutz zu erreichen, konstruierte das Team eine dünne (weniger als 1 μm) Silizium-Nanoporenmembran (SNM) aus Siliziumwafern, die nanoskalige Schlitzporen enthalten.
Die Forscher bauten einen Prototyp eines Bioreaktors, der ein SNM mit 10 nm breiten Poren beherbergte, wobei menschliche Nierenepithelzellen (HRECs) auf Acryleinsätzen auf beiden Seiten des SNM kultiviert wurden. Um zu testen, ob das SNM eine immunprotektive Barriere darstellt in vitro, setzten sie eine Seite des SNM dem proinflammatorischen Zytokin TNF-α aus.
Sechs Stunden nach der Exposition waren die TNF-α-Spiegel in dem durch das SNM geschützten Kompartiment vernachlässigbar, was zeigt, dass die 10 nm breiten Poren den Durchgang großer Zytokine (und damit auch größerer Komponenten des Immunsystems wie T-Zellen und Antikörper) verhindern. . Zellen auf der Seite, die direkt TNF-α ausgesetzt war, hatten eine Lebensfähigkeit von weniger als 50 %, während die durch das SNM versiegelten Zellen eine hohe Lebensfähigkeit von fast 90 % beibehielten.
Es ist auch wichtig, dass ein Implantat keine Blutgerinnsel verursacht, die sich auf Oberflächen bilden können, die mit Blut in Kontakt kommen, und zum Ausfall des Geräts und zu schwerwiegenden Komplikationen für den Patienten führen können. Um dies zu vermeiden, verwendeten die Forscher numerische Strömungsdynamik, um die Geometrie des U-förmigen Blutflusspfades durch den Bioreaktor zu optimieren.
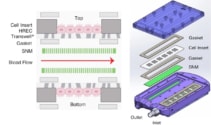
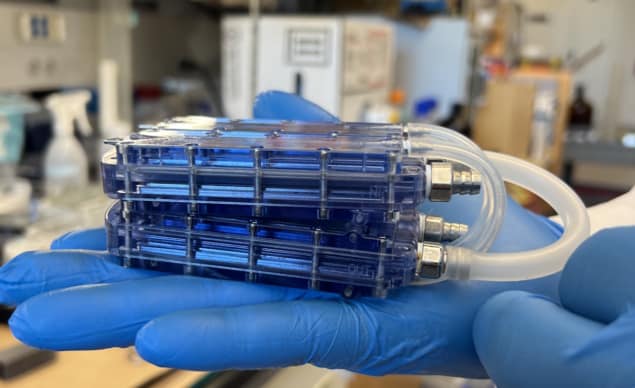
Sie nutzten dieses Design, um einen implantierbaren Bioreaktor zu entwickeln, der vier SNMs in einem Polycarbonatgehäuse enthält und an der Ober- und Unterseite der Blutkanäle ausgerichtet ist. Sie platzierten mit konfluenten HRECs bestückte Acryleinsätze auf den gegenüberliegenden Seiten jedes SNM und verwendeten Verbindungsstücke aus rostfreiem Stahl, um das Blut zwischen den SNMs und den PTFE-Gefäßtransplantaten zu übertragen.
Um die Biokompatibilität dieser Bioreaktor-Prototypen zu testen, baute das Team Geräte zusammen und implantierte sie chirurgisch in fünf gesunde Schweine unter dualer Thrombozytenaggregationshemmung (ohne Immunsuppression). Die Bioreaktoren waren über die PTFE-Transplantate mit dem Gefäßsystem der Tiere verbunden. Es traten keine Komplikationen im Zusammenhang mit den Geräten oder der Operation auf und die Tiere blieben während der gesamten drei- oder siebentägigen Experimente (der Zeit, in der typischerweise eine hyperakute Abstoßung auftritt) gesund, ohne Anzeichen einer Abstoßung.
Die Forscher untersuchten, ob die Implantation von Bioreaktoren mit xenogenen menschlichen Zellen eine Immunreaktion bei den Schweinen hervorrief. Die Untersuchung von 13 häufigen Entzündungsbiomarkern ergab einen Anstieg einiger Zytokine zwei Tage nach der Implantation, wie aufgrund einer postoperativen Entzündung zu erwarten war. Aber sieben Tage nach der Implantation waren alle Zytokinspiegel auf einen Zustand minimaler Entzündung gesunken. Dieser Befund steht im Gegensatz zu der heftigen Reaktion, die in einem typischen Xenotransplantatmodell mit einem immunkompetenten Empfänger erwartet wird.
OCT könnte dabei helfen, den Pool an Nierenspendern zu erweitern
Nach drei oder sieben Tagen entfernten die Forscher die Bioreaktoren zur Auswertung von den Tieren. Sie fanden heraus, dass das explantierte SNM intakt war, nur eine minimale Zell- und Proteinanhaftung aufwies und sich im Gerät keine Blutgerinnsel bildeten – ein wichtiger Schritt zum Nachweis seiner Sicherheit. Darüber hinaus blieben die eingekapselten HREC-Zellen zu mehr als 90 % lebensfähig, ohne Anzeichen einer Zellablösung und der Aufrechterhaltung enger interzellulärer Verbindungen.
„Wir mussten beweisen, dass ein funktionsfähiger Bioreaktor keine immunsuppressiven Medikamente benötigt, und das haben wir getan“, sagt Roy in einer Pressemitteilung. „Wir hatten keine Komplikationen und können jetzt iterieren und die gesamte Palette der Nierenfunktionen auf menschlicher Ebene abdecken.“
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- PlatoData.Network Vertikale generative KI. Motiviere dich selbst. Hier zugreifen.
- PlatoAiStream. Web3-Intelligenz. Wissen verstärkt. Hier zugreifen.
- PlatoESG. Automobil / Elektrofahrzeuge, Kohlenstoff, CleanTech, Energie, Umwelt, Solar, Abfallwirtschaft. Hier zugreifen.
- PlatoHealth. Informationen zu Biotechnologie und klinischen Studien. Hier zugreifen.
- ChartPrime. Verbessern Sie Ihr Handelsspiel mit ChartPrime. Hier zugreifen.
- BlockOffsets. Modernisierung des Eigentums an Umweltkompensationen. Hier zugreifen.
- Quelle: https://physicsworld.com/a/implantable-bioartificial-kidney-aims-to-free-patients-from-dialysis/
- :Ist
- :nicht
- $UP
- 1
- 10
- 125
- 13
- a
- Erreichen
- Zusatz
- Adresse
- Nach der
- Ziel
- ausgerichtet
- Alle
- ebenfalls
- an
- und
- Tiere
- SIND
- AS
- montiert
- At
- vermeiden
- Barriere
- BESTE
- zwischen
- Blut
- Boden
- erbaut
- aber
- by
- CAN
- Verursachen
- Die Zellen
- Center
- Kanäle
- klicken Sie auf
- Kopien
- gemeinsam
- abschließen
- Komponenten
- inbegriffen
- Confluent
- Sie
- Kontakt
- enthält
- Kontrast
- könnte
- erstellen
- erstellt
- entscheidend
- Tage
- verringert
- liefern
- zeigen
- demonstrieren
- Design
- entwickeln
- Gerät
- Geräte
- Dialyse
- DID
- Direkt
- Direkt
- Krankheit
- Arzt
- die
- Drogen
- zwei
- im
- Dynamik
- jeder
- entweder
- beschäftigt
- gekapselt
- Bewerten
- Auswertung
- Beweis
- Untersuchen
- Ausgezeichnet
- Erweitern Sie die Funktionalität der
- erwartet
- Experimente
- ausgesetzt
- Belichtung
- Scheitern
- Suche nach
- fünf
- Fluss
- Flüssigkeit
- Fluiddynamik
- Aussichten für
- unten stehende Formular
- gebildet
- gefunden
- vier
- Francisco cisco~~POS=HEADCOMP
- Frei
- für
- funktional
- Funktionen
- hätten
- Leitung
- Gesundheit
- gesund
- Hilfe
- GUTE
- Halten
- Hoffnung
- STUNDEN
- Gehäuse
- aber
- HTTPS
- human
- Image
- Immunsystem
- wichtig
- in
- Dazu gehören
- Erhöhung
- Information
- Anfangs-
- Einsätze
- innerhalb
- beantragen müssen
- in
- Problem
- Probleme
- IT
- SEINE
- jpg
- Wesentliche
- Niere
- Nieren
- grosse
- größer
- neueste
- führen
- links
- weniger
- Cholesterinspiegel
- Limitiert
- länger
- Wartung
- viele
- max-width
- sowie medizinische
- minimal
- Modell
- mehr
- sollen
- Nanoporen
- Natur
- fast
- erforderlich
- Bedürfnisse
- Neu
- nicht
- jetzt an
- aufgetreten
- of
- on
- EINEM
- XNUMXh geöffnet
- gegenüber
- Optimieren
- or
- Ergebnisse
- besitzen
- Sauerstoff
- Tafel
- Teil
- Durchgang
- Weg
- Vertrauen bei Patienten
- Patienten
- Physik
- Physik-Welt
- Plato
- Datenintelligenz von Plato
- PlatoData
- Presse
- verhindern
- Projekt
- geschützt
- Schutz
- Proteine
- Prototyp
- Prototypen
- Belegen
- bietet
- Erreichen
- Reaktion
- bezogene
- verlassen
- blieb
- Entfernt
- renal
- repliziert
- Berichtet
- erfordern
- erfordert
- Forschungsprojekte
- Forscher
- Antwort
- Revealed
- Recht
- roy
- Sicherheit
- San
- San Francisco
- sagt
- Skalieren
- Abschnitt
- Abschnitte
- ernst
- sieben
- mehrere
- Seite
- Seiten
- Schild
- Silizium
- einige
- Bundesstaat
- Erklärung
- Schritt
- Studie
- Erfolgreich
- so
- liefern
- Support
- Chirurgie
- überleben
- System
- T-Zellen
- Nehmen
- Team
- Test
- getestet
- als
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- ihr
- Sie
- Diese
- vom Nutzer definierten
- fehlen uns die Worte.
- diejenigen
- obwohl?
- nach drei
- während
- Daumennagel
- So
- Zeit
- zu
- Top
- gegenüber
- Übergang
- Transplantation
- behandeln
- Bearbeitung
- Behandlungen
- was immer dies auch sein sollte.
- XNUMX
- typisch
- typisch
- Universität
- benutzt
- Durchführbarkeit
- lebensfähig
- wurde
- we
- waren
- wann
- ob
- welche
- während
- ganze
- werden wir
- mit
- ohne
- arbeiten,
- weltweit wie ausgehandelt und gekauft ausgeführt wird.
- würde
- Zephyrnet