Die Strahlentherapie beweglicher Läsionen ist eine Herausforderung. Die Abgabe der therapeutischen Strahlung an ein geplantes Zielvolumen kann durch Organbewegungen beeinträchtigt werden, während anatomische Verformungen und Unsicherheiten bei der Einrichtung zu Zielfehlern führen können. Wenn Radioonkologen über eine genaue 3D-Karte der Strahlungsdosisverteilung in Echtzeit verfügten, könnten sie die Höhe oder Flugbahn der Strahlung online ändern, um wirksamere und sicherere Behandlungen zu erzielen.
Akustische Bildgebung mit ionisierender Strahlung (iRAI) ist eine nicht-invasive Technologie, die diese Fähigkeit bieten könnte. Durch die Rekonstruktion der Strahlungsdosis mithilfe akustischer Wellen kann iRAI die Dosisablagerung in Tumoren und angrenzenden gesunden Geweben abbilden und die Dosisakkumulation während der Strahlentherapie in Echtzeit überwachen, ohne dass zusätzliche Strahlungsquellen verwendet werden müssen.
Ein multidisziplinäres Forschungsteam am University of Michigan und Moffitt-Krebszentrum hat nun ein volumetrisches Bildgebungssystem iRAI für klinische Zwecke entwickelt. Das System, beschrieben in Nature Biotechnologygelang eine semiquantitative dreidimensionale Kartierung der Röntgenstrahlabgabe tief in den Körper während der Strahlentherapie eines Patienten mit Lebermetastasen.
Die iRAI-Technik funktioniert über den thermoakustischen Effekt. Wenn ein hochenergetischer gepulster Photonenstrahl, der von einem Linearbeschleuniger erzeugt wird, auf Körpergewebe trifft, wird er absorbiert. Diese absorbierte Energie wird in Wärme umgewandelt, die eine lokale Wärmeausdehnung verursacht und akustische Wellen erzeugt. Diese Wellen sind jedoch schwach und mit der klinischen Ultraschalltechnologie normalerweise nicht erkennbar.
Das neue iRAI-System erkennt die akustischen Signale mit einem speziell entwickelten 2D-Matrix-Array-Wandler und einer passenden Mehrkanal-Vorverstärkerplatine, die von einem kommerziellen Forschungsultraschallsystem angetrieben wird. Das verstärkte Signal wird dann in ein Ultraschallgerät übertragen, um in Echtzeit dosisbezogene Bilder zu erstellen.
Die Forscher erklären, dass ihr duales Modalitätssystem, das iRAI mit Ultraschallbildgebung kombiniert, „eine vielversprechende Lösung bietet, um den Bedarf an Echtzeitüberwachung der Strahlposition und Online-Bewertung der abgegebenen Dosis während der Strahlentherapie zu decken“. Das Ultraschallbild stellt die morphologischen Gewebestrukturen und Bewegungen im Körper sowie funktionelle Informationen wie Blutfluss und Gefäßdichte dar, während das iRAI-Bild die räumlich verteilte Dosisdeposition in verschiedenen biologischen Geweben abbilden und quantifizieren kann.
„Bei dieser klinischen Studie handelte es sich um eine Pilotstudie zur Beurteilung der Machbarkeit des Einsatzes von iRAI bei Patienten, die eine abdominale stereotaktische Körperbestrahlungstherapie (SBRT) erhielten“, erklärt der klinische Studienleiter Kyle Cuneo vom Rogel Cancer Center in Michigan. „Seine Erkenntnisse ermöglichen es uns, das iRAI-System zu optimieren.“
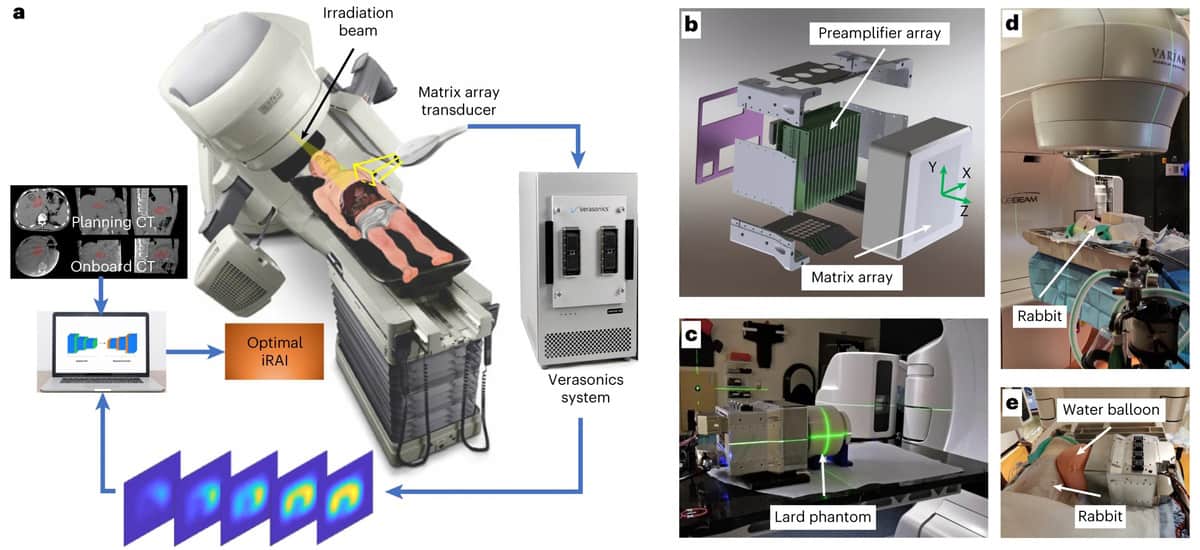
Für ihre Proof-of-Concept-Studie validierten die Forscher das System an einem zylindrischen Schweinefettphantom, einem Kaninchen und dann an einem Patienten, der sich einer abdominalen SBRT unterzog. Um das Signal-Rausch-Verhältnis (SNR) bei der Erkennung akustischer Strahlungssignale zu verbessern, wählten sie eine Zentralfrequenz von 0.35 MHz, um dem Leistungsspektrum der akustischen Signale zu entsprechen, die durch den 4-µs-Röntgenimpuls erzeugt werden. Das SNR wurde durch den 1024-Kanal-Vorverstärker mit 46 dB Verstärkung, der in das 2D-Matrix-Array integriert ist, und durch die Anzeige der iRAI-Bilder mit 25-facher Mittelung weiter verbessert.
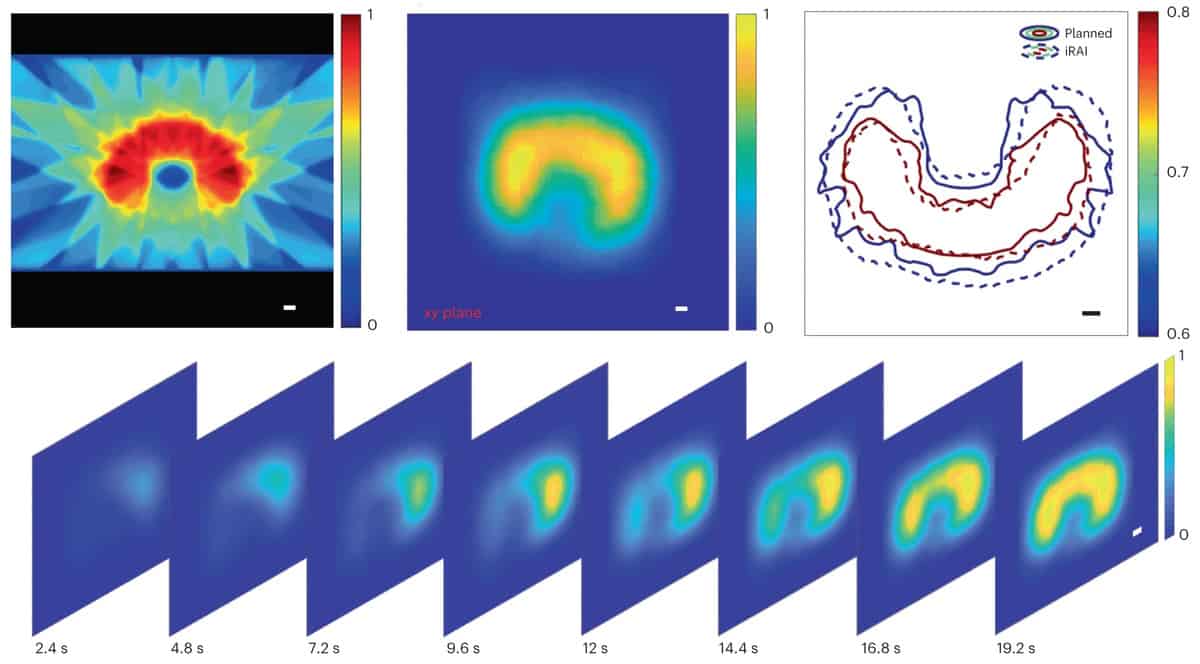
Nach der Überprüfung der Systemleistung mithilfe des Phantoms erstellte und testete das Team einen klinischen Behandlungsplan zur Bestrahlung der Leber eines Kaninchens. Die iRAI-Messungen zeigten eine hohe Übereinstimmung zwischen der gemessenen Dosisverteilung und der vom Behandlungsplanungssystem generierten.
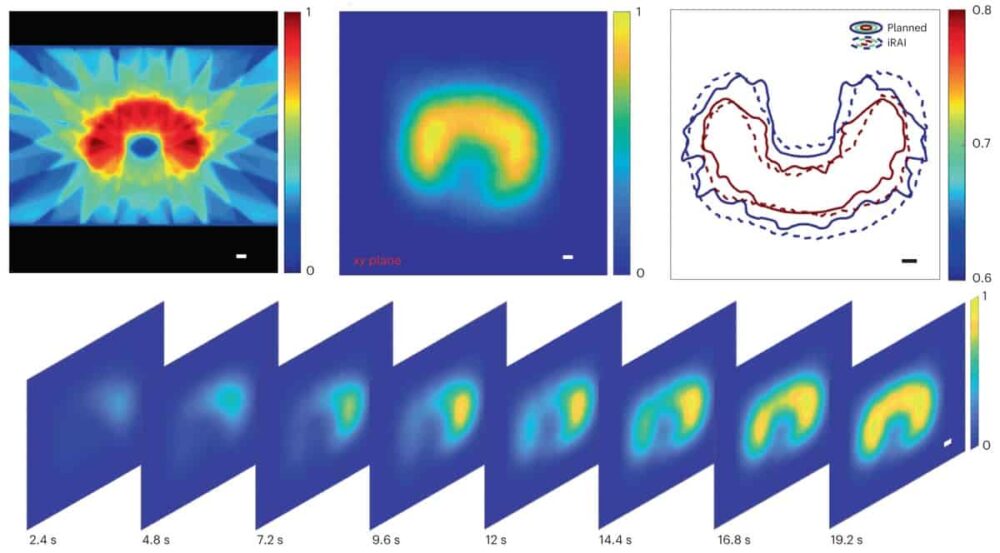
Anschließend erstellte das Team Strahlentherapiepläne für den Studienteilnehmer, wobei der Behandlungsplan für jede Fraktion in zwei Teile unterteilt war. Der erste Teil war für die iRAI-Bildgebung bestimmt und umfasste Strahlen mit 2.087 bzw. 0.877 Gy, die in die obere bzw. untere vordere Richtung abgegeben wurden. Darauf folgte ein volumetrisch modulierter Arc-Therapieplan (ohne iRAI-Bildgebung), um sicherzustellen, dass die gesamte abgegebene Strahlendosis den klinischen Anforderungen entsprach.
Sowohl die Dosisorte als auch die Gesamtverteilungen der iRAI-Messungen stimmten gut mit dem Behandlungsplan überein. Mit der volumetrischen iRAI-Bildgebung konnte der hochdosierte Bereich mit hoher Genauigkeit kartiert werden. Die Forscher weisen darauf hin, dass sie die Kartierungsgenauigkeit für Bereiche mit geringerer Dosisintensität optimieren, die räumliche Auflösung verbessern und ein umfassendes Kalibrierungsprotokoll entwickeln müssen, um eine absolute Dosismessung zu ermöglichen, indem sie fortschrittliche Rekonstruktionstechniken nutzen, die künstliche Intelligenz nutzen.
Grant, Hauptermittler Issam El Naqa vom Moffitt Cancer Center weist darauf hin, dass das aktuelle System durch Echtzeit-Ultraschallbildgebung erweitert und auch im Zusammenhang mit Hochrisiko-Abgabeszenarien wie der FLASH-Strahlentherapie evaluiert wird.
Akustische Bildgebung verspricht Echtzeit-Dosismessung für die FLASH-Strahlentherapie
„Eine mögliche zukünftige Anwendung dieser Technologie ist die adaptive Behandlungsbereitstellung in Echtzeit. Aktuelle adaptive Behandlungstechniken basieren hauptsächlich auf anatomischen Veränderungen im Tumor und gefährdeten Organen (OARs)“, erklärt Cuneo. „Mit iRAI können wir sowohl anatomische als auch, was noch wichtiger ist, dosimetrische Informationen nutzen, um den Bestrahlungsplan anzupassen. Dies könnte eine Dosiserhöhung im Ziel ermöglichen, insbesondere in Situationen, in denen ein benachbarter OAR vorhanden ist, und sicherere Behandlungen ermöglichen, indem die tatsächliche Dosis, die während jeder Fraktion an das Ziel und die OARs abgegeben wird, genau quantifiziert wird.“
„Das System verfügt über die einzigartige Fähigkeit, die Strahlungsdeposition zu visualisieren und gleichzeitig die Organbewegung zu überwachen. Dies ermöglicht eine bessere Lokalisierung der Strahlung auf gezielte Tumoren und schont gleichzeitig unbeteiligtes Gewebe auf kostensparende Weise“, fügt El Naqa hinzu. „Dies kann sowohl in Industrie- als auch in Entwicklungsländern angewendet werden, in denen die finanziellen Ressourcen knapp sind, was zu einer verbesserten Patientenversorgung und besseren Ergebnissen an diesen Orten führt.“
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- Platoblockkette. Web3-Metaverse-Intelligenz. Wissen verstärkt. Hier zugreifen.
- Quelle: https://physicsworld.com/a/dose-tracking-during-radiotherapy-could-enable-safer-cancer-treatments/
- 10
- 2D
- 3d
- a
- Fähig
- Absolute
- Beschleuniger
- Anhäufung
- Genauigkeit
- genau
- genau
- Erreichen
- erreicht
- automatisch
- Zusätzliche
- Fügt
- advanced
- Zustimmung
- Zulassen
- und
- Anwendung
- angewandt
- Arc
- Bereich
- Bereiche
- Feld
- künstlich
- künstliche Intelligenz
- Bewertung
- Augmented
- Mittelung
- basierend
- Strahl
- Besser
- zwischen
- Blut
- Blau
- Tafel
- Körper
- Boden
- CAD
- Krebs
- österreichische Unternehmen
- Verursachen
- Ursachen
- Center
- Hauptgeschäftsstelle
- herausfordernd
- Änderungen
- Klinische
- vereint
- kommerziell
- umfassend
- Bestehend
- konstruieren
- Kontext
- Kosten
- könnte
- Ländern
- erstellt
- Strom
- tief
- geliefert
- liefern
- Lieferanten
- beschrieben
- entwickeln
- entwickelt
- Entwicklung
- Entwicklungsländer
- Gerät
- anders
- verteilt
- Verteilung
- Ausschüttungen
- geteilt
- angetrieben
- im
- jeder
- bewirken
- Effektiv
- ermöglichen
- ermöglichen
- Energie
- verbesserte
- gewährleisten
- gleichermaßen
- Fehler
- Eskalation
- insbesondere
- Bewerten
- Expansion
- Erklären
- Erklärt
- Revolution
- Vorname
- Blinken (Flash)
- Fluss
- gefolgt
- Fraktion
- Frequenz
- für
- funktional
- weiter
- Zukunft
- Gewinnen
- erzeugt
- erzeugt
- gut
- Klasse
- gesund
- GUTE
- hohes Risiko
- aber
- HTTPS
- Image
- Bilder
- Imaging
- wirkt
- zu unterstützen,
- verbessert
- in
- Information
- integriert
- Intelligenz
- Problem
- IT
- führenden
- Niveau
- Linien
- Leber
- Standorte
- Weise
- Karte
- Mapping
- Spiel
- abgestimmt
- Abstimmung
- Matrix
- max-width
- Messungen
- Überwachen
- Überwachung
- mehr
- Bewegung
- ziehen um
- Natur
- Need
- Neu
- Angebote
- Online
- XNUMXh geöffnet
- Optimieren
- Gesamt-
- Teil
- Teile
- Vertrauen bei Patienten
- Patienten
- Leistung
- Phantom
- Pilot
- Länder/Regionen
- Plan
- geplant
- Planung
- Pläne
- Plato
- Datenintelligenz von Plato
- PlatoData
- Position
- Potenzial
- Werkzeuge
- bereit
- Geschenke
- Principal
- Promises
- aussichtsreich
- Protokoll
- die
- Puls
- Hase
- Strahlentherapie
- Verhältnis
- echt
- Echtzeit
- Empfang
- Voraussetzungen:
- Forschungsprojekte
- Forscher
- Auflösung
- Downloads
- REIHE
- Sicherheit
- Einsparung
- Knapp
- Szenarien
- ausgewählt
- Signal
- Signale
- Umstände
- Lösung
- LÖSEN
- Quellen
- räumlich
- Spektrum
- Strikes
- Es wurden Studien
- Studie
- so
- Oberteil
- System
- Target
- gezielt
- Targeting
- Team
- Techniken
- Technologie
- Das
- ihr
- Thermal-
- Daumennagel
- Zeit
- mal
- zu
- Top
- Gesamt
- Tracking
- Flugbahn
- übertragen
- Transfers
- Behandlungen
- Versuch
- was immer dies auch sein sollte.
- Unsicherheiten
- einzigartiges
- us
- -
- gewöhnlich
- validiert
- verifizieren
- Anzeigen
- Volumen
- Wellen
- welche
- während
- werden wir
- ohne
- Werk
- würde
- Röntgenstrahl
- Zephyrnet