Große Epidemien, darunter SARS, Zika und Ebola, und Pandemien wie H1N1 und COVID-19 haben die Welt in den letzten zwei Jahrzehnten erfasst. Da immer häufiger Ausbrüche von Infektionskrankheiten auftreten, wird die Notwendigkeit, die Kapazitäten für virale Diagnose- und Überwachungstests zu erweitern, um Epidemien einzudämmen und Pandemien zu verhindern, immer deutlicher. Forscher unter der Leitung von Dino diCarlo und Sam Emaminejad von der University of California, Los Angeles (UCLA) haben nun einen handgehaltenen viralen Diagnosetest entwickelt, der auf einem Schwarm millimetergroßer Magnete (sogenannte „Ferrobots“) basiert. Die Technologie könnte den Durchsatz von Krankheitstests erheblich steigern und gleichzeitig die Kosten und den Verbrauch knapper Vorräte minimieren.
Beschreibung des diagnostischen Laborkits in Naturskizzieren die Forscher das Arbeitsprinzip und die Anpassungsfähigkeit der Plattform für Multiplex- und Pool-Virustests. Sie berichten auch über Ergebnisse einer klinischen Studie mit Proben von Personen mit COVID-19-Symptomen. Der Vergleich der Testergebnisse unter Verwendung des Laborkits mit denselben Proben, die unter Verwendung des Goldstandard-Assays für die reverse Transkriptions-Polymerase-Kettenreaktion (RT-PCR) auf COVID-19 getestet wurden, ergab eine Testempfindlichkeit von 98 % und eine Spezifität von 100 %.
Überwindung von Lieferengpässen und Reduzierung der Kosten
Unter den Optionen für Virusdiagnostik und Überwachungstests zeigen Nukleinsäureamplifikationstests (NAATs) klare Vorteile gegenüber Antigen- und Antikörper-basierten Tests in Bezug auf Sensitivität, Spezifität und die Fähigkeit zur schnellen Bereitstellung ohne vorherige Generierung spezifischer diagnostischer Antikörper. Frühere NAAT-basierte Testplattformen waren jedoch nicht in der Lage, die integrierten Liquid-Handling-, Analyse- und automatischen Feedback-Prozesse durchzuführen, die erforderlich sind, um flexible Arbeitsabläufe zu erreichen und die Effizienz des Krankheitsscreenings zu maximieren.
Um diesen Mangel zu überwinden, haben die UCLA-Forscher eine handflächengroße, auf Leiterplatten basierende programmierbare Plattform entwickelt, die Liquid-Handling- und bioanalytische Operationen parallel durchführt. Im Gegensatz zu früheren Methoden, die sperrige, ressourcenintensive Instrumente erforderten, bietet die miniaturisierte Plattform erhebliche Kosteneinsparungen über einen weiten Bereich der Virusprävalenz hinweg und bietet gleichzeitig eine hohe Präzision, Robustheit, Anpassungsfähigkeit und Skalierbarkeit.
„Unsere Handheld-Labortechnologie könnte dazu beitragen, einige der Barrieren der Knappheit und des Zugangs zu Tests zu überwinden, insbesondere zu Beginn einer Pandemie, wenn es am wichtigsten ist, die Ausbreitung von Krankheiten einzudämmen“, sagt Emaminejad. „Und über sein Potenzial hinaus, Probleme mit knappen Vorräten und hoher Nachfrage anzugehen, könnte es umfassend angepasst werden, um viele Arten von Krankheiten im Feld und in Laborqualität zu testen.“
Umstellung auf Multiplex- und Pooled-Tests
Die Forscher entwickelten eine Reihe von Operationen, um das Vorhandensein von genetischem Material eines Virus nachzuweisen – in diesem Fall SARS-CoV-2, das COVID-19 verursacht. Die Platine steuert einen Schwarm von Ferrobots, um magnetisierte Proben durch den diagnostischen NAAT-Workflow zu transportieren, einschließlich automatisiertem Transport, Aliquotieren, Zusammenführen, Mischen und Erhitzen von Probentröpfchen zur Amplifikation des Reaktionsprodukts (DNA). Schließlich werden die Ergebnisse anhand einer Farbänderung eines pH-Indikators bestimmt, was eine binäre Interpretation des Tests über oder unter einem Schwellenwert als positiv bzw. negativ ermöglicht.
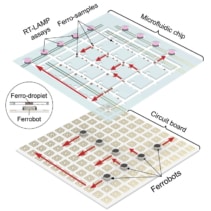
Die UCLA-Forscher demonstrierten auch die Parallelisierung – das gleichzeitige Bewegen vieler Ferrobots unter Verwendung elektromagnetischer Kacheln in der Schaltung – sowie sequentielle Aufgabenoperationen in kollaborativer Weise durch jeden Ferrobot (in Koordination mit den anderen Ferrobots).
„Das kompakte Design und die automatisierte Probenhandhabung dieser Plattform ermöglichen die einfache Implementierung von gepoolten Tests, bei denen Sie Dutzende von Patientenproben gleichzeitig testen können, und das alles mit den gleichen Materialien, die derzeit zum Testen nur eines Patienten erforderlich sind“, sagt Di Carlo. „Zum Beispiel könnten Sie Studenten in einem ganzen Studentenwohnheim mit nur ein paar Dutzend Testkits testen.“

Anpassungsfähiger Biosensor erkennt COVID-19-Viren und -Antikörper schnell
Durch die Implementierung eines gepoolten Testalgorithmus, der bis zu 16 Proben in einem einzigen Assay testen kann, erfordert das System viel geringere Reagenzienkosten als zum individuellen Testen der Proben. Wenn der gepoolte Test ein positives Ergebnis zeigte, findet eine nachfolgende optimierte Reihe von Vorgängen innerhalb der Plattform statt, bis die tatsächlichen positiven Proben identifiziert sind. Letztendlich, stellen die Forscher fest, könnten die Kosten für chemische Reagenzien je nach Virusprävalenz um das 10- bis 300-fache gesenkt werden.
Die Plattform kann nicht nur auf mehrere Krankheiten gleichzeitig testen, sondern auch eine große Anzahl von Eingangsproben parallel und asynchron bei ihrem Eintreffen analysieren, wodurch Wartezeiten im Zusammenhang mit der Stapelverarbeitung vermieden werden. Daher kommt das Team zu dem Schluss, dass diese Technologie eine vielversprechende Lösung darstellt, um die Testkapazität weltweit für die Vorbereitung auf Epidemien und Pandemien zu erhöhen.