Wissenschaftler aus der Weizmann Institute of Science haben zum ersten Mal überhaupt synthetische Embryomodelle von Mäusen außerhalb der Gebärmutter gezüchtet, indem sie in einer Petrischale kultivierte Stammzellen verwendet haben. Dies ist ein bedeutender medizinischer Durchbruch.
Darüber hinaus wird der Zellkulturprozess auch ohne die Verwendung befruchteter Eizellen durchgeführt, wodurch die Notwendigkeit von Spermien umgangen wird.
Dieser Ansatz könnte die technologischen und moralischen Bedenken im Zusammenhang mit der Verwendung natürlicher Embryonen in Forschung und Biotechnologie weitgehend vermeiden, was ihn unglaublich wichtig macht. Selbst mit Mäusen sind einige Tests derzeit nicht praktikabel, da sie Tausende erfordern würden Embryonen; Die Verfügbarkeit von Modellen, die aus embryonalen Mauszellen entwickelt wurden, die sich in Laborinkubatoren millionenfach vermehren, ist jedoch nahezu unbegrenzt.
Prof. Jacob Hanna von Weizmanns Abteilung für Molekulargenetik sagte: „Der Embryo ist die beste Organherstellungsmaschine und der beste 3D-Bioprinter – wir haben versucht, nachzuahmen, was er tut. Wissenschaftler wissen bereits, wie man reife Zellen wieder „stammt“ – Pioniere dieser zellulären Reprogrammierung hatten 2012 einen Nobelpreis erhalten. hat sich als viel problematischer erwiesen.“
„Bisher waren die spezialisierten Zellen in den meisten Studien oft entweder schwer herzustellen oder fehlerhaft, und sie bildeten eher einen Mischmasch als gut strukturiertes Gewebe, das für die Transplantation geeignet war. Wir haben es geschafft, diese Hürden zu überwinden, indem wir das darin codierte Selbstorganisationspotenzial freigesetzt haben Stammzellen"
Im März 2021 entwickelten Wissenschaftler das elektronisch gesteuerte Gerät, das die Züchtung natürlicher Mausembryonen außerhalb der Gebärmutter ermöglicht. Die Wissenschaftler verwendeten das gleiche Gerät in dem neuen Experiment, um über eine Woche lang Mausstammzellen zu züchten – etwa die Hälfte der Tragzeit einer Maus.
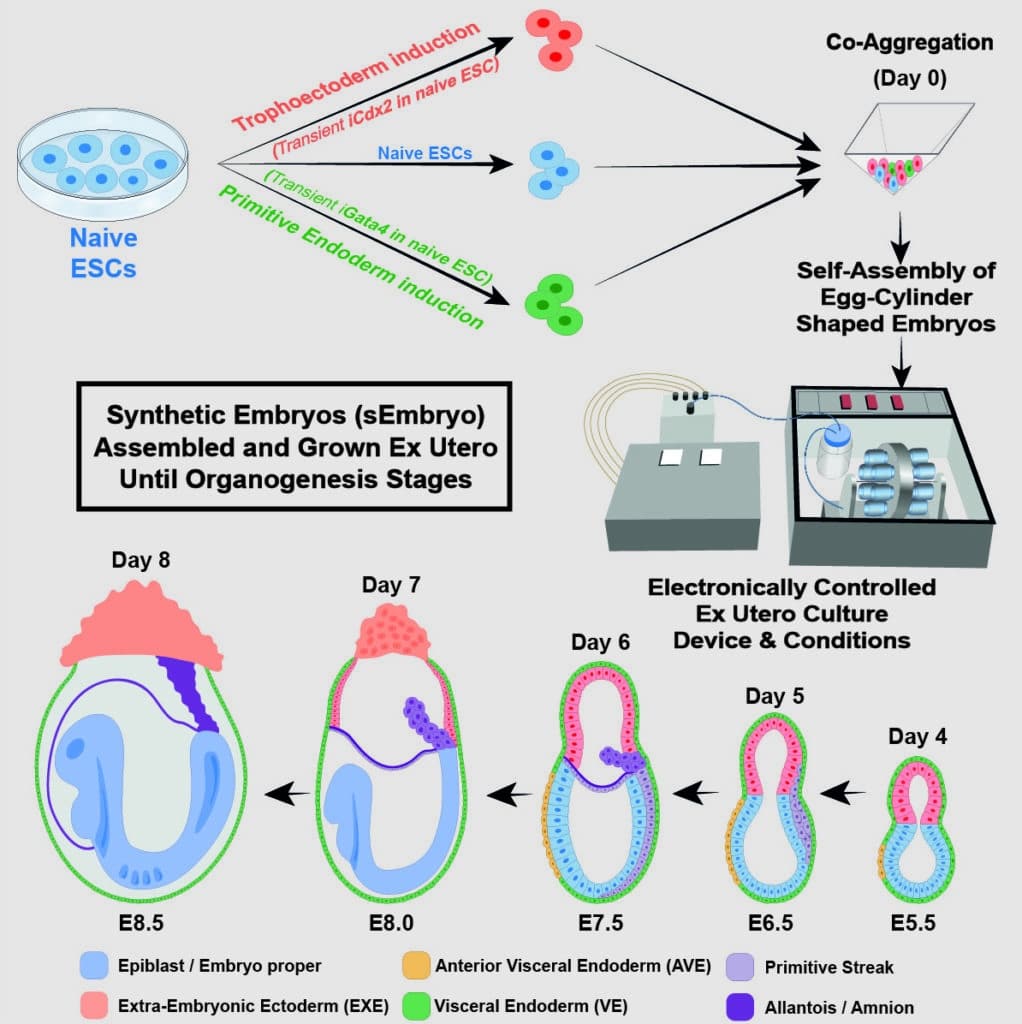
Die Wissenschaftler teilten die Stammzellen in drei Gruppen ein, bevor sie in das Gerät eingebracht wurden. In einem wurden die Zellen, die schließlich selbst zu embryonalen Organen werden würden, in ihrem aktuellen Zustand belassen. Einer von zwei Arten von Genen, Hauptregulatoren entweder der Plazenta oder des Dottersacks, wurde in den Zellen der anderen beiden Gruppen während einer Vorbehandlung, die nur 48 Stunden dauerte, überexprimiert.
Hanna sagte, „Wir haben diesen beiden Zellgruppen einen vorübergehenden Schub gegeben, um extraembryonale Gewebe hervorzubringen, die die Embryo entwickeln"
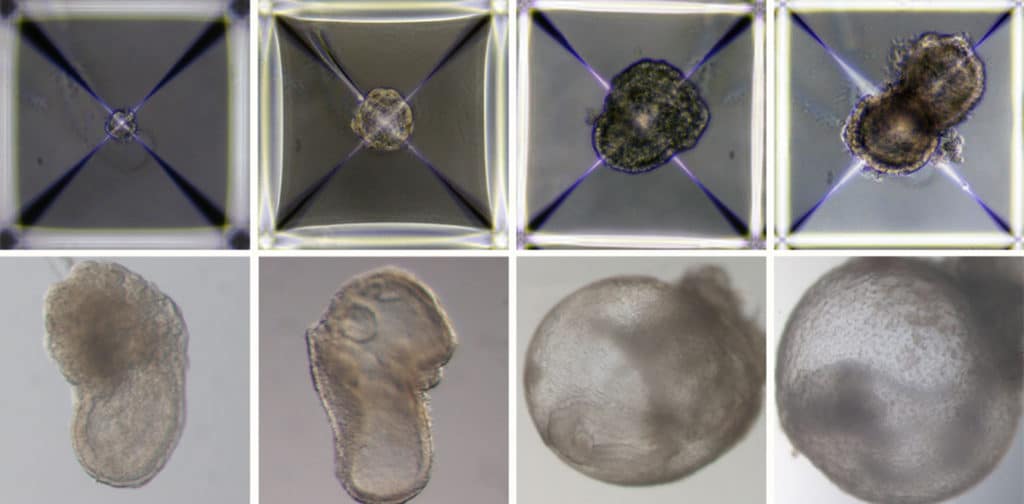
Die drei Zellgruppen wurden innerhalb des Geräts schnell zu Aggregaten kombiniert, von denen die meisten keine vollständige Entwicklung durchliefen. 50 von 10,000 oder ungefähr 0.5 Prozent bildeten jedoch später Kugeln, die sich später zu einer länglichen, embryoähnlichen Struktur entwickelten. Die Plazenta und die Dottersäcke waren außerhalb der Embryonen sichtbar, und die Entwicklung des Modells verlief wie bei einem natürlichen Embryo, da die Wissenschaftler jeden Zellsatz farblich gekennzeichnet hatten.
Diese synthetischen Modelle entwickelten sich normal bis Tag 8.5 – fast die Hälfte der 20-tägigen Trächtigkeit der Maus – in diesem Stadium hatten sich alle frühen Organvorläufer gebildet, einschließlich eines schlagenden Herzens, Blutstammzellenkreislauf und eines Gehirns mit wohlgeformten Falten, a Neuralrohr und Darmtrakt. Im Vergleich zu natürlichen Mausembryos zeigten die synthetischen Modelle eine 95-prozentige Ähnlichkeit sowohl in der Form der inneren Strukturen als auch in den Genexpressionsmustern verschiedener Zelltypen. Die in den Modellen zu sehenden Organe gaben alle Anzeichen dafür, dass sie funktionsfähig waren.
Hanna sagte, „Die Studie eröffnet eine neue Arena: Unsere nächste Herausforderung besteht darin, zu verstehen, wie Stammzellen wissen, was zu tun ist – wie sie sich selbst zu Organen zusammensetzen und ihren Weg zu ihren zugewiesenen Stellen innerhalb eines Embryos finden. Und da unser System im Gegensatz zu einer Gebärmutter transparent ist, könnte es sich als nützlich erweisen, um Geburts- und Implantationsfehler menschlicher Embryonen zu modellieren.“
„Anstatt ein anderes Protokoll für die Züchtung jedes Zelltyps – zum Beispiel der Niere oder der Leber – zu entwickeln, könnten wir eines Tages vielleicht in der Lage sein, ein synthetisches embryoähnliches Modell zu erstellen und dann die Zellen zu isolieren, die wir brauchen. Wir müssen den entstehenden Organen nicht vorschreiben, wie sie sich zu entwickeln haben. Der Embryo selbst macht das am besten.“
Journal Referenz:
- Shadi Tarazi, Alejandro Aguilera Castrejon, et al. ¬Synthetische Embryonen nach der Gastrulation, die ex utero aus naiven ESCs der Maus generiert wurden. Zelle 01. August 2022. DOI: 10.1016 / j.cell.2022.07.028