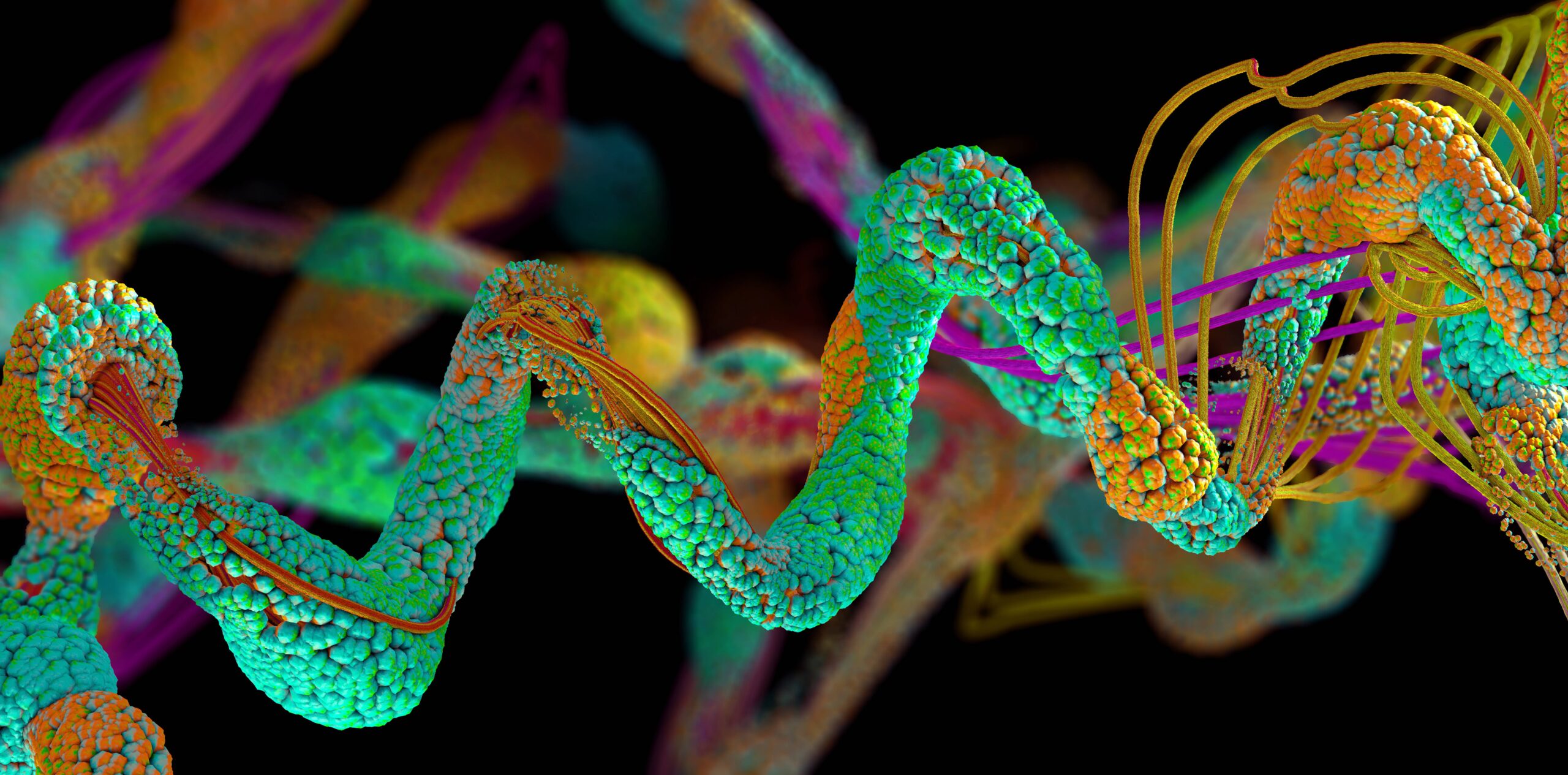
Το μοντέλο αναδίπλωσης πρωτεϊνών με τεχνητή νοημοσύνη AlphaFold έχει προβλέψει περισσότερες από 200 εκατομμύρια πρωτεΐνες, σχεδόν όλες αυτές οι δομές γνωστές στην επιστήμη, δήλωσε την Πέμπτη η DeepMind.
Οι πρωτεΐνες είναι πολύπλοκα βιολογικά μόρια που παράγονται σε ζωντανούς οργανισμούς από οδηγίες που είναι αποθηκευμένες στο DNA. Κατασκευασμένες από έως και 20 τύπους αμινοξέων, αυτές οι αλυσίδες νανοκλίμακας εκτελούν ζωτικές κυτταρικές εργασίες για την εκτέλεση όλων των ειδών των σωματικών λειτουργιών. Η γνώση της τρισδιάστατης μορφής των πρωτεϊνών είναι σημαντική, καθώς η φυσική της δομή παρέχει υποδείξεις για το πώς συμπεριφέρεται και τι σκοπό εξυπηρετεί, κάτι που μας βοηθά να κάνουμε πράγματα όπως να αναπτύξουμε φάρμακα και να δημιουργήσουμε αντιγραφικές πρωτεΐνες για όσους δεν τα έχουν.
Ορισμένες πρωτεΐνες είναι χρήσιμες, όπως αυτές που εμπλέκονται στην πέψη των τροφών, ενώ άλλες μπορεί να είναι επιβλαβείς, όπως αυτές που εμπλέκονται στην ανάπτυξη όγκων. Ωστόσο, είναι δύσκολο να βρεις τα περίπλοκα στριμωγμένα σχήματά τους. Οι μοριακοί βιολόγοι μπορούν να περάσουν χρόνια διεξάγοντας πειράματα για να αποκρυπτογραφήσουν τη δομή μιας πρωτεΐνης και το AlphaFold μπορεί να το κάνει αυτό σε λίγα λεπτά, ανάλογα με το πόσο μεγάλο είναι το μόριο, από τη σύνθεση αμινοξέων.
Το AlphaFold εκπαιδεύτηκε σε εκατοντάδες χιλιάδες γνωστές πρωτεϊνικές δομές και έμαθε τις σχέσεις μεταξύ των συστατικών αμινοξέων και των τελικών συνολικών σχημάτων. Δεδομένης μιας αυθαίρετης εισόδου αλληλουχίας αμινοξέων, το μοντέλο μπορεί να προβλέψει μια τρισδιάστατη δομή πρωτεΐνης. Τώρα, το μοντέλο έχει προβλέψει σχεδόν όλες τις δομές πρωτεΐνης που είναι γνωστές στην επιστήμη.
Σε συνεργασία με το Ευρωπαϊκό Ινστιτούτο Βιοπληροφορικής, η DeepMind έχει επεκτείνει Βάση δεδομένων δομής πρωτεϊνών AlphaFold να περιέχει πάνω από 200 εκατομμύρια τρισδιάστατα σχήματα πρωτεϊνών από τα ζώα στα φυτά, από βακτήρια σε ιούς – μια αύξηση πάνω από 3 φορές από σχεδόν ένα εκατομμύριο μόρια σε τουλάχιστον 200 εκατομμύρια μόρια σε μόλις ένα χρόνο.
«Ελπίζαμε ότι αυτός ο πρωτοποριακός πόρος θα βοηθούσε στην επιτάχυνση της επιστημονικής έρευνας και ανακάλυψης παγκοσμίως και ότι άλλες ομάδες θα μπορούσαν να μάθουν και να βασιστούν στις προόδους που κάναμε με το AlphaFold για να δημιουργήσουμε περαιτέρω ανακαλύψεις», δήλωσε ο Demis Hassibis, συνιδρυτής και Διευθύνων Σύμβουλος της DeepMind. είπε σε δήλωση την Πέμπτη.
«Αυτή η ελπίδα έγινε πραγματικότητα πολύ πιο γρήγορα από ό,τι είχαμε τολμήσει να ονειρευόμαστε. Μόλις δώδεκα μήνες αργότερα, το AlphaFold είχε πρόσβαση σε περισσότερους από μισό εκατομμύριο ερευνητές και χρησιμοποιήθηκε για να επιταχύνει την πρόοδο σε σημαντικά προβλήματα του πραγματικού κόσμου, που κυμαίνονται από την πλαστική ρύπανση έως την αντοχή στα αντιβιοτικά.
Το μητρώο ζήτησε από την DeepMind περαιτέρω σχόλια.
Το AlphaFold έχει επίσης δείξει μεγάλες δυνατότητες για το σχεδιασμό νέων φαρμάκων. Οι δομές βοηθούν τους επιστήμονες να καταλάβουν χημικές ενώσεις που μπορούν να συνδεθούν με πρωτεΐνες-στόχους για να θεραπεύσουν ή να τις αποτρέψουν από το να εκτελούν παθολογικές λειτουργίες. Εταιρείες συμπεριλαμβανομένης της Insilco Medicine έχουν πειραματίστηκε με το μοντέλο να ανακαλύψει νέα φάρμακα? είπε ο διευθύνων σύμβουλος Alex Zhavoronkov Το μητρώο ότι η διαδικασία είναι πολύ πιο περίπλοκη από όσο νομίζετε και περιλαμβάνει πολλά βήματα.
Δεν είναι σαφές πόσο ακριβείς είναι οι προβλέψεις του AlphaFold. Η δομή που μοιάζει με κορδέλα μιας πρωτεΐνης αλλάζει συχνά σχήμα όταν αλληλεπιδρά με ένα φάρμακο, κάτι στο οποίο το AlphaFold δεν μπορεί να βοηθήσει τους επιστήμονες καθώς δεν είναι εκπαιδευμένο σε αυτό. Ο Zhavoronkov είπε ότι το μοντέλο είναι μια «αρκετά αξιοσημείωτη ανακάλυψη», αλλά ήταν επιφυλακτικός με όλη τη διαφημιστική εκστρατεία.
«Μέχρι να δούμε μια δομή για έναν νέο στόχο σε μια μεγάλη ασθένεια που λαμβάνεται μέσω του AlphaFold χωρίς πρόσθετα πειράματα, ένα μόριο που σχεδιάστηκε με χρήση τεχνητής νοημοσύνης – ή άλλων μεθόδων – χρησιμοποιώντας αυτήν την προβλεπόμενη δομή, συντέθηκε και δοκιμάστηκε σε όλη τη διαδρομή και στη συνέχεια δημοσιεύτηκε σε περιοδικό υψηλής ποιότητας – [μπορούμε] τότε να γιορτάσουμε».
Τα μεγάλα φαρμακεία θέλουν να δουν μόρια σχεδιασμένα με τη βοήθεια εργαλείων τεχνητής νοημοσύνης όπως το AlphaFold να δοκιμάζονται πραγματικά σε ποντίκια και ανθρώπους. «Τα καθαρά αλγοριθμικά επιτεύγματα δεν είναι πολύτιμα για τις φαρμακευτικές εταιρείες και ειδικά για τους ασθενείς», πρόσθεσε ο Zhavoronkov.
Ο Fabio Urbina, ανώτερος επιστήμονας στην Collaboration Pharmaceuticals, μια startup που χρησιμοποιεί αλγόριθμους μηχανικής μάθησης για την ανάπτυξη φαρμάκων για σπάνιες γενετικές ασθένειες, είπε ότι το AlphaFold δεν έχει ακόμη αποδειχθεί χρήσιμο στην έρευνά του. Η Urbina χρησιμοποιεί μια διαφορετική τεχνική και εστιάζει περισσότερο στη δομή ενός πιθανού νέου φαρμάκου παρά σε μια πρωτεΐνη-στόχο.
Δεν έχει ακόμη φανεί εάν οι πρωτεϊνικές δομές θα είναι αρκετά χρήσιμες… για να μας βοηθήσουν να ανακαλύψουμε νέα πιθανά φάρμακα για σπάνιες ασθένειες
«Αυτό συμβαίνει για μερικούς λόγους. οι πρωτεϊνικές δομές για πολλούς στόχους φαρμάκων συχνά δεν ήταν εύκολα διαθέσιμες για χρήση από τους ερευνητές και οι πληροφορίες πρωτεΐνης δεν φαινόταν να βοηθούν τα πρώιμα μοντέλα μηχανικής μάθησης να βελτιώσουν την προγνωστική τους ισχύ με σημαντικό περιθώριο», είπε. Το μητρώο.
«Είμαι προσεκτικά αισιόδοξος ότι το AlphaFold έχει ουσιαστικά «λύσει» το πρώτο πρόβλημα, αλλά δεν έχει ακόμη φανεί εάν οι πρωτεϊνικές δομές θα είναι αρκετά χρήσιμες για την κατάντη εφαρμογή μας για τη βελτίωση της προγνωστικής ισχύος μηχανικής μάθησης για να μας βοηθήσει να ανακαλύψουμε νέα πιθανά φάρμακα για σπάνιες ασθένειες. Ωστόσο, βλέπουμε όλο και περισσότερο να λαμβάνονται υπόψη οι δομικές πληροφορίες της πρωτεΐνης ως μέρος νεότερων μεθόδων μηχανικής μάθησης και σκεφτήκαμε να κάνουμε το ίδιο».
Η δημιουργία μιας βάσης δεδομένων με όλες σχεδόν τις γνωστές δομές πρωτεΐνης διαθέσιμη, όπως έχει υποσχεθεί η DeepMind, σημαίνει ότι περισσότεροι επιστήμονες θα έχουν τους πόρους για να πειραματιστούν και να δημιουργήσουν πιο ισχυρά μοντέλα τεχνητής νοημοσύνης, είπε ο Urbina. «Είμαι προσεκτικά αισιόδοξος, αλλά με ολόκληρη τη βιβλιοθήκη δομών πρωτεΐνης διαθέσιμη, θα έλεγα ότι υπάρχει μεγάλη πιθανότητα οι δομές AlphaFold να ενσωματωθούν σε ορισμένα από τα μοντέλα μηχανικής μάθησης μας και μπορεί τελικά να μας βοηθήσουν να ανακαλύψουμε νέες θεραπευτικές μεθόδους. ” ®
- AI
- αι τέχνη
- ι γεννήτρια τέχνης
- ρομπότ ai
- τεχνητή νοημοσύνη
- πιστοποίηση τεχνητής νοημοσύνης
- τεχνητή νοημοσύνη στον τραπεζικό τομέα
- ρομπότ τεχνητής νοημοσύνης
- ρομπότ τεχνητής νοημοσύνης
- λογισμικό τεχνητής νοημοσύνης
- blockchain
- συνέδριο blockchain ai
- Coingenius
- συνομιλητική τεχνητή νοημοσύνη
- κρυπτοσυνεδριο αι
- του νταλ
- βαθιά μάθηση
- έχεις google
- μάθηση μηχανής
- Πλάτων
- πλάτων αι
- Πληροφορία δεδομένων Plato
- Παιχνίδι Πλάτωνας
- Πλάτωνα δεδομένα
- platogaming
- κλίμακα αι
- σύνταξη
- Το μητρώο
- zephyrnet