Imaginemos un ejército de partículas autopropulsadas cubiertas de radioisótopos, entre 2500 y 10,000 veces más pequeñas que una mota de polvo, que, al inyectarse en el cuerpo, buscan tumores cancerosos y se adhieren a ellos, destruyéndolos. ¿Suena a ciencia ficción? No ocurre lo mismo con los ratones con cáncer de vejiga.
Investigadores españoles informan que las nanopartículas que contienen yodo radiactivo y que se impulsan al reaccionar con la urea tienen la capacidad de distinguir los tumores cancerosos de la vejiga del tejido sano. Estos "nanobots" penetran en la matriz extracelular del tumor y se acumulan en su interior, lo que permite que la terapia con radionúclidos alcance su objetivo preciso. En un estudio realizado en el Instituto de Bioingeniería de Cataluña (IBEC) de Barcelona, los ratones que recibieron una dosis única de este tratamiento tuvieron una reducción del 90% en el tamaño de los tumores de vejiga en comparación con los animales no tratados.
Este nuevo enfoque podría algún día revolucionar el tratamiento del cáncer de vejiga. El cáncer de vejiga es el décimo cáncer más común en el mundo, con más de 600,000 nuevos casos diagnosticados en 2022 y más de 220,000 muertes en todo el mundo, según el Observatorio Mundial del Cáncer de la Organización Mundial de la Salud.
El cáncer de vejiga no músculo-invasivo, que representa el 75% de los casos, se trata actualmente mediante resección del tumor seguida de inyección intravesical de quimioterapia o fármacos de inmunoterapia en la vejiga. Sin embargo, la administración de fármacos es particularmente difícil debido a la baja permeabilidad del urotelio (el tejido que recubre el interior del tracto urinario), el llenado de la orina y el posterior lavado de los fármacos. El proceso también resulta incómodo para los pacientes, ya que necesitan girar el cuerpo a intervalos mientras están tumbados boca abajo para permitir que los fármacos lleguen a todos los lados de la pared de la vejiga. Después del tratamiento, existe un riesgo de recurrencia del 30 al 70% en cinco años.
Para mejorar los resultados clínicos, el investigador principal samuel sánchez y sus colegas tienen como objetivo desarrollar tratamientos innovadores y más eficaces para el cáncer de vejiga y, en el proceso, reducir las tasas de recurrencia. Además, una terapia de dosis única reduciría significativamente el costo del tratamiento, que actualmente requiere entre seis y 14 hospitalizaciones.
El equipo creó nanobots a partir de nanopartículas de sílice mesoporosas con varios componentes funcionales en sus superficies. Estos incluyen radioisótopos para visualización PET o terapia con radionúclidos, y la proteína ureasa, que reacciona con la urea en la orina y permite la propulsión del nanobot.
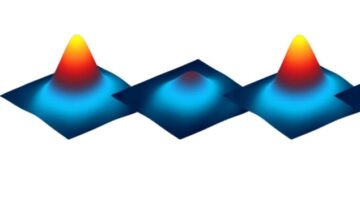
Escribiendo en Naturaleza Nanotecnología, los investigadores informan que cuando agregaron una gota de nanobots a una solución que contenía urea 300 mM, los nanobots exhibieron un movimiento de enjambre, formando frentes activos y vigorosos y vórtices tridimensionales. Sin la urea, los nanobots simplemente se sedimentaron cerca del sitio de adición.
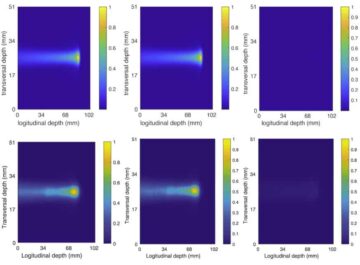
Examinar si los nanobots pueden alcanzar un tumor in vivo, el equipo evaluó su comportamiento en ratones portadores de tumores. Las imágenes de tomografía por emisión de positrones (PET) mostraron que las señales de los nanobots radiomarcados se ubicaban junto con la posición del tumor, determinada mediante resonancia magnética, y la radioactividad se observaba principalmente en el sitio del tumor objetivo. Sólo los ratones inyectados con nanobots más urea mostraron una acumulación sustancial en la masa tumoral: los nanobots administrados en agua y las nanopartículas de control (sin ureasa) administradas en agua o urea exhibieron una absorción tumoral mínima.
Los investigadores sugieren que la movilidad de los nanobots les ayuda a penetrar la masa tumoral. "Los nanorobots carecen de anticuerpos específicos para reconocer el tumor, y el tejido tumoral suele ser más rígido que el tejido sano, pero este no es el caso de los tumores de vejiga", explica el coprimer autor. Meritxell Serra Casablancas del IBEC. “Observamos que estos nanorobots pueden descomponer la matriz extracelular del tumor aumentando localmente el pH mediante una reacción química autopropulsada. Este fenómeno favoreció una mayor penetración del tumor”. Los investigadores creen que los nanobots chocan con el urotelio como si fuera una pared, pero penetran el tumor, que es más esponjoso.
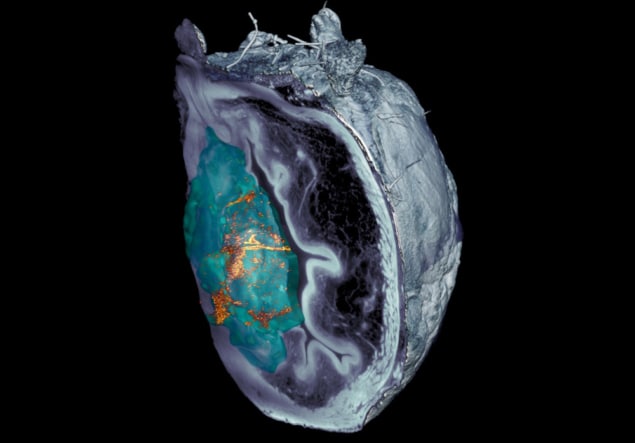
El equipo señala que identificar los nanobots en imágenes de microscopía de tejido disecado fue un desafío. Después del fracaso de las técnicas de microscopía óptica confocal, los investigadores de IRB Barcelona desarrolló un sistema de microscopía basado en láminas de luz, basado en iluminación láser plana, capaz de escanear las diferentes capas de la vejiga y crear una reconstrucción 3D de todo el órgano.
"El sistema de microscopía de lámina de luz elástica dispersa que desarrollamos nos permitió eliminar la luz reflejada por el propio tumor, lo que nos permitió identificar y localizar nanopartículas en todo el órgano sin etiquetado previo, con una resolución sin precedentes", dice Julien Colombelli del IRB Barcelona.

Bacterias modificadas atraen radioisótopos que matan el cáncer hacia los tumores
Para evaluar el efecto terapéutico de la técnica, el equipo etiquetó nanobots con yodo-131 (131I, un radioisótopo comúnmente utilizado para la terapia con radionúclidos), y los administré a los ratones portadores de tumores. Tratamiento con dosis perdidas 131Los I-nanobots en urea detuvieron el crecimiento tumoral, mientras que las dosis altas 131Los I-nanobots administrados en urea condujeron a una reducción de casi el 90% en el volumen del tumor en comparación con los animales no tratados.
Sánchez cuenta Mundo de la física que los próximos pasos del equipo son encapsular pequeños medicamentos que se utilizan actualmente en quimioterapia y continuar probando la eficacia de los nanobots como portadores de medicamentos. Con el tiempo, pretenden ampliar los nanobots y estudiar las vías regulatorias para avanzar hacia los primeros ensayos clínicos en los próximos tres o cuatro años, a través de la spin-off del IBEC. Terapéutica de nanobots.
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- PlatoData.Network Vertical Generativo Ai. Empodérate. Accede Aquí.
- PlatoAiStream. Inteligencia Web3. Conocimiento amplificado. Accede Aquí.
- PlatoESG. Carbón, tecnología limpia, Energía, Ambiente, Solar, Gestión de residuos. Accede Aquí.
- PlatoSalud. Inteligencia en Biotecnología y Ensayos Clínicos. Accede Aquí.
- Fuente: https://physicsworld.com/a/self-propelling-nanobots-shrink-bladder-tumours-in-mice-by-90/
- :es
- :no
- $ UP
- 000
- 10
- 135
- 14
- 2022
- 220
- 300
- 3d
- 600
- a
- capacidad
- Conforme
- Cuentas
- Acumular
- acumulación
- lector activo
- adicional
- adición
- Adicionalmente
- administrado
- Después
- objetivo
- Todos
- Permitir
- también
- an
- y
- animales
- enfoque
- somos
- Ejército
- detenido
- AS
- evaluado
- At
- adjuntar
- atraer
- autor
- Las bacterias
- Barcelona
- basado
- comportamiento
- CREEMOS
- entre
- cuerpos
- cuerpo
- Descanso
- pero
- by
- PUEDEN
- Cáncer
- capaz
- portadores
- case
- cases
- desafiante
- químico
- Clínico
- ensayos clínicos
- personal
- Chocar
- COM
- Algunos
- comúnmente
- en comparación con
- componentes
- llevado a cabo
- contenido
- continue
- control
- Cost
- creado
- Creamos
- En la actualidad
- día
- muertes
- liberado
- entrega
- determina
- desarrollar
- desarrollado
- una experiencia diferente
- distinguir
- dosificar
- DE INSCRIPCIÓN
- droga
- Drogas
- dos
- Dust
- efecto
- Eficaz
- eficiencia
- eliminarlos
- emisión
- habilitar
- facilita
- permite
- permitiendo
- Todo
- EU
- evaluar
- finalmente
- examinar
- exhibido
- Explica
- Fallidos
- Ficción
- relleno
- Nombre
- Digital XNUMXk
- seguido
- siguiendo
- Digital XNUMXk
- Desde
- funcional
- Buscar
- En todo el mundo
- mayor
- Incremento
- tenido
- Tienen
- Salud
- saludable
- ayuda
- Sin embargo
- HTTPS
- Identifique
- identificar
- if
- imágenes
- Inmunoterapia
- mejorar
- in
- incluir
- creciente
- información
- originales
- dentro
- la intención de
- dentro
- IT
- SUS
- sí mismo
- jpg
- etiquetado
- Falta
- láser
- ponedoras
- LED
- luz
- como
- revestimiento
- localmente
- Baja
- Misa
- Matrix
- max-ancho
- Puede..
- Microscopía
- mínimo
- movilidad
- más,
- MEJOR DE TU
- movimiento
- movimiento
- MRI
- Naturaleza
- Cerca
- hace casi
- ¿ Necesita ayuda
- Nuevo
- Next
- nota
- novela
- observatorio
- of
- on
- ONE
- , solamente
- or
- resultados
- Más de
- particularmente
- las vías
- los pacientes
- precios
- un fenómeno mundial
- Física
- Mundo de la física
- Platón
- Inteligencia de datos de Platón
- PlatónDatos
- más
- posición
- necesidad
- las cuales
- Director de la escuela
- Anterior
- Impulsar
- propulsión
- Proteínas
- Tarifas
- en comunicarse
- reacción
- Reacciona
- aprovecha
- reconocer
- reaparición
- reducir
- reducción
- refleja
- regulador
- reporte
- requiere
- investigadores
- Resolución
- revolucionar
- Riesgo
- dice
- Escala
- exploración
- disperso
- Ciencia:
- Ciencia ficción
- Buscar
- visto
- mostró
- Plato Adicional
- señales
- significativamente
- simplemente
- soltero
- página web
- SEIS
- Tamaño
- chica
- menores
- So
- a medida
- suena
- España
- soluciones y
- pasos
- ESTUDIO
- posterior
- sustancial
- sugieren
- te
- Target
- equipo
- técnicas
- decirles
- test
- que
- esa
- La
- el mundo
- su
- Les
- sí mismos
- terapia forestal
- Estas
- ellos
- así
- Tres
- tridimensional
- A través de esta formación, el personal docente y administrativo de escuelas y universidades estará preparado para manejar los recursos disponibles que derivan de la diversidad cultural de sus estudiantes. Además, un mejor y mayor entendimiento sobre estas diferencias y similitudes culturales permitirá alcanzar los objetivos de inclusión previstos.
- a lo largo de
- uña del pulgar
- veces
- a
- hacia
- tratados
- del mismo día
- tratamientos
- ensayos
- verdadero
- GIRO
- típicamente
- sin precedentes
- a
- consumo
- us
- usado
- diversos
- vía
- visualización
- volumen
- Pared
- fue
- Agua
- we
- tuvieron
- cuando
- sean
- que
- mientras
- dentro de
- sin
- mundo
- se
- años
- zephyrnet