Küsige vähiuurijalt, milline on kümnendi läbimurdeline ravi, ja nad ütlevad teile, et CAR T võtab krooni.
Teraapia muudab geneetiliselt inimese enda immuunrakud, muutes need supersõduriteks, kes jahivad vähkkasvajaid vererakke. Hämmastava kiirusega on mitu CAR T-teraapiat heaks kiidetud FDA poolt varem ravimatute verevähkide puhul. Seni on ravi saanud üle 15,000 XNUMX patsiendi.
Pennsylvania ülikooli tehnoloogia teerajajale dr Carl June’ile me vaid kriipime CAR T potentsiaali pinda.
Aastal perspektiiv aastal avaldatud artikkel loodus sel nädalal pani June ja kolleegid paika, kuidas edasi liikuda.
CAR T-teraapia rakendab oma juurtes teatud tüüpi immuunraku, mida nimetatakse T-rakkudeks, loomulikku "tapjainstinkti" ja suunab selle konkreetsele sihtmärgile, näiteks verevähirakkudele. Kuid hoolika ümberkujundamise korral saab CAR T-ravi geneetiliselt muundada, et võidelda paljude inimkonna kõige silmapaistvamate meditsiiniliste vaenlastega: autoimmuunhaigused, astma ja süda, maksa- ja neeruhaigused, mis on põhjustatud järjest kangestuvatest lihastest.
Veelgi intrigeerivam on see, et CAR T võib aidata puhastada vananevaid zombirakke, mis on seotud vanusega seotud haigustega või võidelda HIV-iga ja muud viiruslikud nakkushaigused.
"Me alles hakkame mõistma selle elava ravimi täielikku potentsiaali," ütles autorid.
Mis on jälle CAR T?
CAR T tähistab "kimäärse antigeeni retseptori T-ravi". Mulle meeldib mõelda sellest kui plug-and-play osadega Mr. Potato Headist.
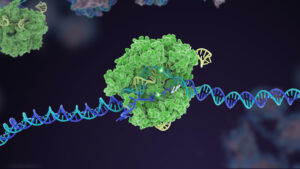
"Kartul" on immuunsüsteemi T-rakk, rakkude perekond, mis tavaliselt uurib meie keha, et otsida ja hävitada sissetungijaid, nagu vähk või infektsioonid. Lisage sellele CAR "osad": geneetiliselt muundatud valgu "konksud", mis võivad haige raku konkreetse valgu külge haarata.
CAR T töötati esmakordselt välja HIV-i vastu võitlemiseks, kuid see saavutas ebaselgete tulemustega, kuid saavutas silmapaistvuse tänu oma tõhususele verevähi ravis. Tavaliselt käib see nii: patsiendi T-rakud eraldatakse verevõtust ja neid täiustatakse laboris geneetiliselt CAR-valgu konstruktsioonidega. Pärast kehasse tagasi infundeerimist väldivad supersõdurid kasvajarakkude kaitsevõimet, kusjuures üks konstrueeritud rakk tapab sadu, kui mitte tuhandeid vähivastaseid.
Autorid ütlesid, et CAR T on tõesti "uus teraapia sammas". Kui T-rakud on seotud teiste haigustega, kas ravi saab rohkem teha?
Tugev võitlus
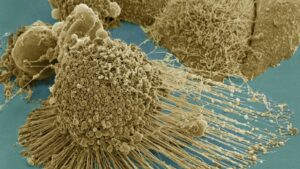
Esimene samm CAR T laiendamiseks verevähist kaugemale on suunatud tahketele vähivormidele – mõelge kõhunäärme-, rinna-, käärsoolevähkidele ja teistele. Kahjuks on autorid öelnud, et tulemused on seni paljudes kliinilistes uuringutes "suuresti pettumust valmistanud".
Kuid nendest ebaõnnestumistest oleme õppinud palju. Erinevalt verevähistest loovad tahked kasvajad kohaliku bioloogilise "kindluse" ja pumpavad välja kemikaale, mis hoiavad T-rakke vaos ja summutavad nende hävitavat toimet. Üks idee, mis aitab neil läbi murda, on CAR T-rakkude otsene süstimine kasvajatesse. Teine on kasutada CRISPR CAR T-rakkude varustamiseks geneetilise profiiliga – teatud geenide lisamine või kustutamine –, mis väldib neid kaitsemehhanisme.
Kahjuks jäävad muud takistused. Tahked kasvajad koosnevad sageli rakkude amalgaamist, millest igaühel on oma pinnavalkude sõrmejälg. See muudab ühe CAR T kujunduse jaoks kõigi vähirakkude jahtimise keeruliseks. Mõned valgu sihtmärgid, mida nimetatakse antigeenideks, laiutavad ka tervete rakkude väliskülge, põhjustades kõrvalkahjustusi.
Siis on võimalus tekitada immuunorkaan. Siin laienevad CAR T-rakud kehas kiiresti, et võidelda oma vähivastase sihtmärgiga, kuid omakorda suunavad keha immuunsüsteemi kriisirežiimi - seisundit, mida nimetatakse "tsütokiinide vabanemise sündroomiks". Lõpptulemus võib olla laastav – palavik, vererõhu kiire langus ja isegi mitme organi puudulikkus.
Nagu kõigi teiste ravimite puhul, on annus võtmetähtsusega. Üks võimalik viis immuunsüsteemi ülekoormuse vältimiseks on anda T-rakkudele ajaliselt piiratud tõuge. Selle asemel, et lisada CAR otse raku geneetilisse koodi, mis muudab need jäädavalt CAR T supersõduriteks, kasutatakse lahenduseks mRNA-d – geenide "tõlkijat". Lõpptulemus on sarnane, kuna rakk sobib tegutsema oma uute CAR-valkudega. Kuid erinevalt geneetilistest insertidest on mRNA ajutine, mis tähendab, et CAR T-rakud võivad loobuda oma supersõduri isiksusest ja naasta oma tavapärase T-raku identiteedi juurde, mis omakorda võimaldab immuunsüsteemil rahuneda.
Laienev universum
Tahkeid vähktõbe on raske lahti saada, kuid hea uudis on see, et nende kaitsemehhanisme teiste haiguste puhul ei eksisteeri. Näiteks autoimmuunhäiretel, diabeedil, südamelihase jäigastumisel või zombirakkudel puudub üldiselt kaitsev kindlus, mis tähendab, et CAR T-l on lihtsam tunnelisse tungida ja oma tapjategevust säilitada. Erinevalt vähkkasvajatest, mis on kurikuulsad oma muteerumisvõime poolest, on neil haigustel sageli püsiv geneetiline profiil, nii et CAR-d võivad säilitada oma tõhususe.
Siiani on CAR T kõige lootustandvam kasutamine väljaspool vähki autoimmuunhaiguste korral.
Tagasi 2022-sse, väikeses kliinilises uuringus süsteemse erütematoosluupusega (SLE) - eluohtliku autoimmuunhaigusega - patsientidel leiti, et CAR T-rakud laienesid nende kehas kiiresti ja leevendasid sümptomeid.
SLE on kõige levinum luupuse tüüp. Siin peab keha immuunsüsteem sõda oma kudede vastu. Peamine süüdlane on teist tüüpi immuunrakud, mida nimetatakse B-rakkudeks, mis tavaliselt toodavad antikehi infektsioonide vastu võitlemiseks. Autoimmuunhaiguste korral peavad B-rakud sõbrad ekslikult vaenlaseks, märgistades eliminatsiooni sihtmärkideks terved kuded – süda, kopsud, neerud.
Pärast CAR T-ravi ei tuginenud ükski uuringus osalenud viiest inimesest enam oma igapäevastele immunosupressiivsetele ravimitele. Üllataval kombel tulid nende B-rakud mõne kuu pärast tagasi, kuid ilma sümptomiteta või organite kahjustusteta.
Teises tõendi mõiste, kasutas meeskond CAR T-d süntetaasivastase sündroomiga patsiendi puhul, mis on autoimmuunhaigus, mis kahjustab kopse ja lihaseid ning põhjustab artriiti. Kolm kuud hiljem paranesid patsiendi lihased ja vähenes kopsupõletik.
Teadlased on nüüd katsetab CAR T raske astma hiiremudelites, mille rakud kaitsevad raskete rünnakute eest, mis kestavad kaua pärast ravi ennast. Teised jõupingutused on seotud autoimmuunhaigustega, nagu reumatoidartriit ja hulgiskleroos, mis mõjutavad närvide ümber olevat kaitsekest.
Kuigi praegused CAR T konfiguratsioonid on paljulubavad, ei tee nad vahet tervete või haigete B-rakkude vahel. Mitmed jõupingutused optimeerivad CAR-i "konkse", et sihtida konkreetselt kahjulikke. Üks uuring hemofiilia - veritsushäire - hiirtel leiti, et uuemad kujundused jätsid terved B-rakud rahule. Kliinilised uuringud kujunduse testimiseks on käimas.
Metsik lääs
Siin muutub CAR T tõeliselt eksperimentaalseks.
Võtke südamefibroosi (südamelihaste jäigastumine), mis võib juhtuda pärast vigastust või kroonilist haigust või vananemise ajal ja viib lõpuks südamepuudulikkuseni. Ravivõimalusi on vähe.
Kontseptsiooni tõestuseks uuringus Eelmisel aastal leiti, et T-rakkude otsene ümberprogrammeerimine hiirte kehas mRNA abil muutis pärast ühekordset süstimist armkoe nende südames. Fibroos ei juhtu ainult südamega. Maks, neerud, kopsud ja lihased kannatavad samuti sarnase jäikuse all, mistõttu on need ideaalsed CAR T-ravi sihtmärgid.
"Kuna otseselt fibroosile suunatud ravimeetodeid napib, võivad CAR T-rakud pakkuda tõhusat ja selektiivset viisi selliste haiguste raviks," ütlesid autorid.
Kuid võib-olla on CAR T-ravi kõige julgem kasutusala vananevate zombirakkude hävitamine. Kuigi need rakud on elus, ei täida need oma tavalisi ülesandeid, vaid pumpavad oma ümbruskonda välja hulga mürgiseid molekule. Tonnide viisi tõend näitab et nende rakkude eemaldamine kemikaalide või geenitehnoloogia abil pikendab tervist, kuid erineva tõhususega.
Siin saab CAR T aidata. Vananevatel rakkudel on spetsiifilised antigeenid, mistõttu on need teraapia jaoks ideaalsed sihtmärgid. Üks uuring kes ravisid kopsuvähki ja maksahaigusi põdevaid hiiri, leidsid, et zombirakkude eemaldamine pikendas eluiga.
Järeldus? CAR T-rakud laienevad kiiresti onkoloogiast kaugemale. Teetõkked jäävad alles: ravi on väga kallis ja potentsiaalselt ohtlik immuuntormide vallandamiseks. Me ei tea veel, kas rakud võivad kehas liikudes terveid kudesid kahjustada või noorendada.
Kuid autorite jaoks oleme sisenemas transformatiivse ravi järgmisse peatükki. "Teoreetilised rakendused on tohutud ja platvorm on võimas ... me alles hakkame mõistma selle elava ravimi täielikku potentsiaali."
Image Credit: labden / Shutterstock.com
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- PlatoData.Network Vertikaalne generatiivne Ai. Jõustage ennast. Juurdepääs siia.
- PlatoAiStream. Web3 luure. Täiustatud teadmised. Juurdepääs siia.
- PlatoESG. Autod/elektrisõidukid, Süsinik, CleanTech, Energia, Keskkond päikeseenergia, Jäätmekäitluse. Juurdepääs siia.
- BlockOffsets. Keskkonnakompensatsiooni omandi ajakohastamine. Juurdepääs siia.
- Allikas: https://singularityhub.com/2023/07/28/the-living-drug-car-t-is-evolving-beyond-just-treating-cancer/
- :on
- :mitte
- : kus
- $ UP
- 000
- 15%
- 23
- a
- võime
- tegevus
- tegevus
- lisama
- lisades
- mõjutada
- pärast
- jälle
- vastu
- Vananemine
- Materjal: BPA ja flataatide vaba plastik
- Lubades
- üksi
- mööda
- Ka
- Kuigi
- an
- ja
- Teine
- mistahes
- rakendused
- OLEME
- ümber
- artikkel
- AS
- At
- Reageerib
- autorid
- vältima
- tagasi
- tõkked
- lahing
- laht
- BE
- olnud
- Algus
- on
- vahel
- Peale
- Verejooks
- veri
- Vererõhk
- asutused
- keha
- suurendada
- Murdma
- läbimurre
- ehitama
- kuid
- by
- kutsutud
- CAN
- vähk
- Vähirakud
- auto
- ettevaatlik
- Carl
- autod
- põhjustatud
- põhjuste
- põhjustades
- Rakke
- kindel
- võimalus
- Peatükk
- kliiniline
- Kliinilistes uuringutes
- kood
- Tagatis
- kolleegidega
- ühine
- koostatud
- mõiste
- seisund
- tuum
- pragu
- krediit
- kriis
- Kroon
- Praegune
- iga päev
- Ohtlik
- kümme aastat
- Disain
- disainilahendused
- hävitama
- laastav
- arenenud
- Diabeet
- raske
- otse
- haigus
- haigused
- häired
- eristatav
- do
- Ei tee
- Ära
- DOT
- alla
- dr
- juhtida
- ajam
- Drop
- uimasti
- Narkootikumide
- ajal
- iga
- lihtsam
- efektiivsus
- jõupingutusi
- lõpp
- vaenlased
- Inseneriteadus
- Inseneride
- tõhustatud
- Sisse
- Isegi
- lõpuks
- näide
- eksisteerima
- Laiendama
- laiendatud
- laiendades
- kallis
- ebaedu
- pere
- kaugele
- FDA
- vähe
- võitlema
- sõrmejälg
- esimene
- eest
- Kindluslinn
- edasi
- avastatud
- sõber
- Alates
- Täida
- täis
- üldiselt
- geenitehnoloogia
- Andma
- Goes
- hea
- rüütama
- juhtuda
- Raske
- kahjulik
- Olema
- juhataja
- tervislik
- süda
- Südamepuudulikkus
- aitama
- siin
- kõrgelt
- hoidma
- Kuidas
- HTTPS
- Inimkond
- sajad
- jaht
- orkaan
- i
- idee
- ideaalne
- if
- Immuunsüsteemi
- paranenud
- in
- Teistes
- Tõstab
- üha rohkem
- nakkused
- Nakkushaigused
- Lisab
- sees
- selle asemel
- sisse
- intrigeeriv
- seotud
- isoleeritud
- IT
- ITS
- ise
- juuni
- Võti
- neer
- Teadma
- labor
- Vähene
- viimane
- Eelmisel aastal
- pärast
- Leads
- õppinud
- lahkus
- vähem
- elu
- nagu
- seotud
- Maks
- elu-
- kohalik
- Pikk
- enam
- põhiline
- TEEB
- Tegemine
- mai..
- tähendus
- meditsiini-
- viga
- mudelid
- kuu
- rohkem
- kõige
- liikuma
- mr
- mRNA
- mitmekordne
- Hulgiskleroos
- Natural
- loodus
- Navigate
- Uus
- uudised
- järgmine
- NIH
- normaalne
- Tavaliselt
- of
- maha
- sageli
- on
- ONE
- ones
- ainult
- peale
- optimeerimine
- Valikud
- or
- Muu
- teised
- meie
- välja
- väljaspool
- üle
- enda
- eriline
- osad
- tee
- patsient
- patsientidel
- Pennsylvania
- Inimesed
- täiuslik
- ehk
- püsivalt
- sammas
- pioneer
- inimesele
- Platon
- Platoni andmete intelligentsus
- PlatoData
- potentsiaal
- potentsiaalselt
- surve
- varem
- toodab
- profiil
- esiletõstmine
- silmapaistev
- paljutõotav
- tõend
- tõendi mõiste
- kaitsta
- Kaitsev
- Valk
- Valgud
- anda
- avaldatud
- pump
- pumpamiseks
- valik
- kiire
- kiiresti
- mõistma
- ümber kujundada
- vabastama
- jääma
- eemaldades
- uurija
- kaasa
- Tulemused
- säilitama
- tagasipöördumine
- teetõkked
- juur
- ROSE
- s
- Ütlesin
- otsima
- selektiivne
- raske
- kuur
- Shutterstock
- sarnane
- ühekordne
- väike
- So
- nii kaugel
- tahke
- mõned
- konkreetse
- eriti
- kiirus
- seisab
- stabiilne
- tormid
- selline
- super
- Pind
- Uuring
- Sümptomid
- süsteem
- süsteemne
- T-rakud
- lahendada
- tegelemine
- võtab
- võtmine
- Kraanid
- sihtmärk
- sihtimine
- eesmärgid
- meeskond
- Tehnoloogia
- öelda
- ajutine
- Testimine
- et
- .
- oma
- Neile
- teoreetiline
- Seal.
- Need
- nad
- mõtlema
- see
- sel nädalal
- tuhandeid
- kolm
- Läbi
- et
- tonni
- muundav
- muudab
- ravimisel
- ravi
- kohtuprotsess
- uuringutes
- käivitamine
- tõeliselt
- tunnel
- Pöörake
- Pööramine
- tüüp
- Käimas
- Ülikool
- erinevalt
- kasutama
- Kasutatud
- kasutamine
- tavaliselt
- suur
- viiruslik
- töötasu
- sõda
- oli
- Tee..
- we
- nädal
- M
- mis
- lai
- Lai valik
- Metsik
- koos
- ilma
- halvim
- aasta
- veel
- sa
- sephyrnet