Teadlased Duke ülikooli meditsiinikeskus on välja töötanud süvaõppepõhise arvutipõhise tuvastamise (CAD) süsteemi, et tuvastada MR-piltidel raskesti tuvastatavaid ajumetastaase. Algoritm näitas suurepärast tundlikkust ja spetsiifilisust, edestades teisi arendamisel olevaid CAD-süsteeme. Tööriist näitab potentsiaali võimaldada tekkivate ajumetastaaside varasemat tuvastamist, võimaldades nende esmasel ilmnemisel stereotaktilise radiokirurgiaga (SRS) suunata ja mõne patsiendi puhul vähendada vajalike raviprotseduuride arvu.
SRS, mis kasutab ühe kiiritusravi seansi jooksul aju sihtmärkidele suure kiirgusdoosi edastamiseks täpselt fokuseeritud footonkiirte abil, on muutumas standardraviks patsientide jaoks, kellel on piiratud arv ajumetastaase. Metastaaside sihtimiseks tuleb see aga esmalt tuvastada MR-pildil. Kahjuks umbes 10% ei ole, 30% alla 3 mm suuruste puhul isegi ekspertide neuroradioloogide läbivaatamisel.
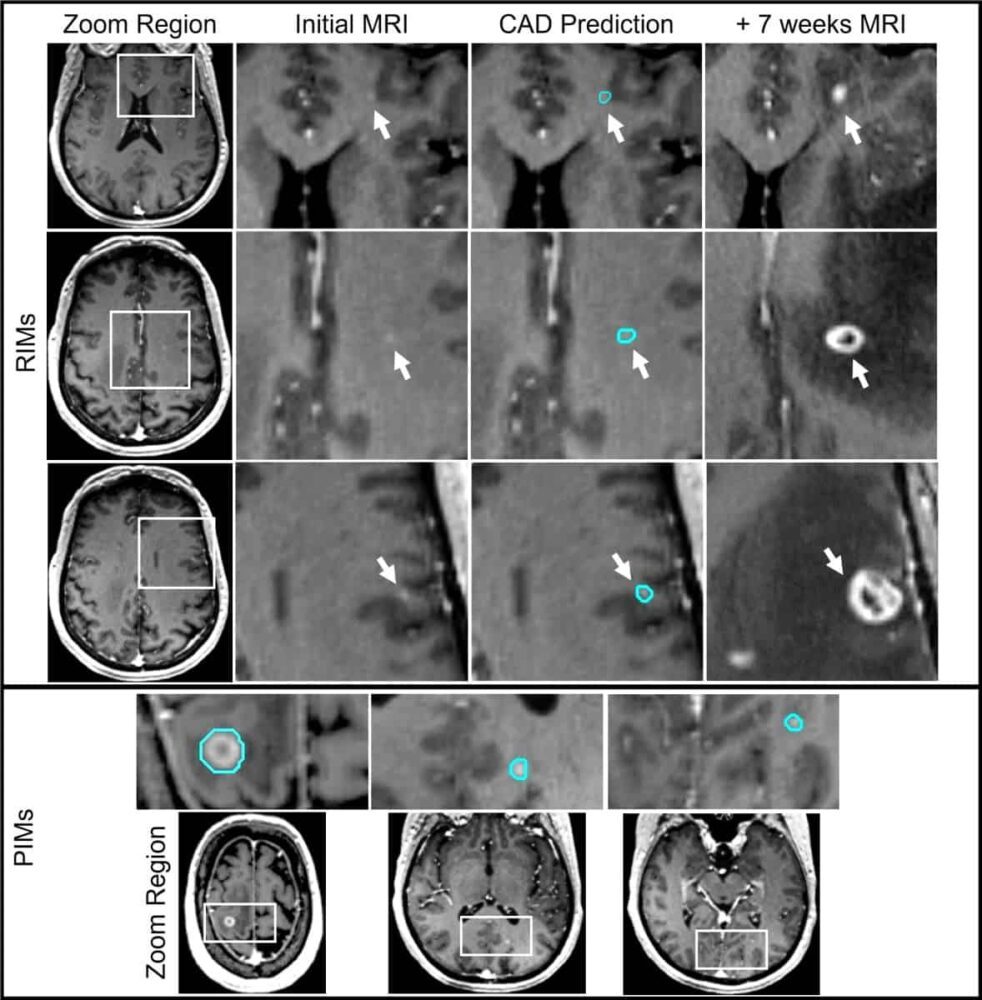
Kui need avastamata ajumetastaasid – mida teadlased nimetavad retrospektiivselt tuvastatud metastaasideks (RIM) – tuvastatakse järgmistel MRI-skaneeringutel, on tavaliselt vaja teist SRS-ravi. Selline ravi on kallis ning võib olla ebamugav ja invasiivne, nõudes mõnikord pea immobiliseerimist tihvtidega kolju külge kinnitatud raamiga.
Hiljutisel ASTRO aastakoosolekul Devon Godfrey selgitasid, et teadlased kujundasid konvolutsioonilise närvivõrgu (CNN) põhise CAD-süsteemi spetsiaalselt selleks, et parandada raskesti tuvastatavate RIM-ide ja väga väikeste prospektiivselt tuvastatud metastaaside (PIM) tuvastamist ja segmenteerimist. Godfrey ja kolleegid kirjeldavad selle süsteemi testimist ja valideerimist dokumendis International Journal of Radiation Oncology Biology Physics.
Meeskond õpetas CAD-tööriista MRI andmetele (kontrastsusega rikutud gradiendi kajajärjestus) 135 patsiendilt, kellel oli 563 aju metastaasi. Pildid saadi 1.5 T ja 3.0 T MRI-skannerite abil erinevatelt müüjatelt mitmes Duke Healthi asukohas. Kokku hõlmas andmekogum 491 PIM-i keskmise läbimõõduga 6.7 mm ja 72 RIM-i 32 patsiendilt keskmise läbimõõduga 2.7 mm.
RIM-ide tuvastamiseks vaatasid teadlased üle iga patsiendi originaalsed MR-pildid, et otsida kontrasti suurenemise märke täpses kohas, kus hiljem metastaasid tuvastati. Pärast ülevaatamist klassifitseerisid nad iga RIM-i nii, et need vastavad pildipõhisele diagnostikakriteeriumile (+DC) või metastaasina tuvastamiseks ebapiisav visuaalne teave (-DC).
Teadlased randomiseerisid RIM-ide ja PIM-ide andmekogumi viide rühma, kasutades neist nelja mudeli ja algoritmi väljatöötamiseks ning ühte testrühmana. "Nii + DC kui ka -DC RIM-ide kaasamine andis suurima tundlikkuse iga aju metastaaside kategooria ja suuruse jaoks, tagastades samal ajal madalaima valepositiivsete määrade ja kõrgeima positiivse ennustusväärtuse," teatavad nad. "See näitab selget kasu, kui lisatakse CAD-treeningu andmetesse väikeste raskete ajumetastaaside ülekaal."
PIM-ide ja +DC RIM-ide puhul, millel on MRI-s selged metastaaside omadused, saavutas mudel üldise tundlikkuse 93%, ulatudes 100% -st kahjustuste puhul, mille läbimõõt on suurem kui 6 mm, kuni 79% -ni nende puhul, mis on väiksemad kui 3 mm. Valepositiivsete tulemuste määr oli samuti muljetavaldavalt madal, keskmiselt 2.7 inimese kohta, võrreldes kaheksa kuni 35-ga teistes CAD-süsteemides, mille tuvastamise tundlikkus on võrreldav väikeste kahjustuste korral.
CAD-süsteem suutis tuvastada ka mõned -DC RIM-id nii arendus- kui ka testikomplektides. Aju metastaaside tuvastamine selles varases staadiumis oleks suur kliiniline eelis, kuna selliseid kahjustusi saaks seejärel põhjalikumalt jälgida pildistamise abil, mis nõuab vajadusel ravi.
Duke'i meeskond töötab nüüd selle nimel, et parandada CAD-tööriista täpsust, kasutades selleks mitut MR-järjestust. Godfrey selgitab, et aju MRI uuringud hõlmavad peaaegu alati mitut MR-järjestust, mis toodavad ainulaadset teavet iga aju voksli kohta. "Usume, et nendest teistest järjestustest saadaoleva lisateabe kaasamine peaks parandama selle täpsust, " ütleb ta.
Godfrey märgib, et teadlased on vaid nädalate kaugusel olemasoleva CAD-süsteemi simuleeritud tulevase kliinilise kasutamise uuringu käivitamisest, et uurida, kuidas tööriist mõjutab nii radioloogide kui ka kiirgusonkoloogide kliinilisi otsuseid.
Sügav õppimine aitab radioloogidel avastada kopsuvähki rindkere röntgenülesvõtetel
"Mitmele SRS-i teostavale neuroradioloogile ja neurokiirguse onkoloogile tehakse aju MR-uuringud. Neil palutakse leida kõik kahjustused, mis võivad olla aju metastaasid, hinnata nende usaldustaset, et see on, ja öelda, kas nad raviksid kahjustust SRS-iga, lähtudes selle esinemisest piltidel," räägib ta. Füüsika maailm. "Seejärel esitame neile CAD-i prognoosid ja hindame CAD-i mõju iga arsti kliinilistele otsustele."
Kui see simulatsiooniuuring annab paljutõotavaid tulemusi, eeldab Godfrey CAD-tööriista kasutuselevõttu, et aidata tuvastada potentsiaalselt raskeid ajumetastaase uutel patsientidel, keda ravitakse Duke'i kiiritusonkoloogia kliinikus uurimisprotokolli alusel, võib-olla niipea kui 2023. aasta keskel.