B-hepatiit on kõige levinum hepatiidi vorm. Tavaliselt edastatakse vere või seksuaalsuhete kaudu, HBV on üks raskemaid ja levinumaid nakkushaigusi.
See viirus nakatab maksarakke, mille tulemuseks on lühiajaline maksapõletik, mis võib areneda krooniliseks infektsiooniks. Sellest võivad tuleneda rasked haigused, nagu tsirroos või maksavähk. Haiguse kroonilise vormi jaoks ei ole tõhusat ravi, seda saab vältida vaid vaktsineerimisega.
Teadlased Genfi ülikool tuvastas olulise valgukompleksi, mis on aktiivne, kui viirus nakatab meie keha. Nad dešifreerisid selle kaitsemehhanismi täpse toimimise.
UNIGE-i meeskond, mida juhtis Michel Strubin, UNIGE arstiteaduskonna mikrobioloogia ja molekulaarmeditsiini osakonna ning Genfi põletikuuuringute keskuse dotsent, avastas 2016. aastal selle haiguse mehhanismi, mis on oluline mõistmiseks: kui meie immuunsüsteemi kaitseb end selle, meie rakkudes esineva kuue valgu kompleksi või vastastikku sõltuva komplekti, SMC5/6 vastu, tuvastab viiruse. DNA ja blokeerib selle.
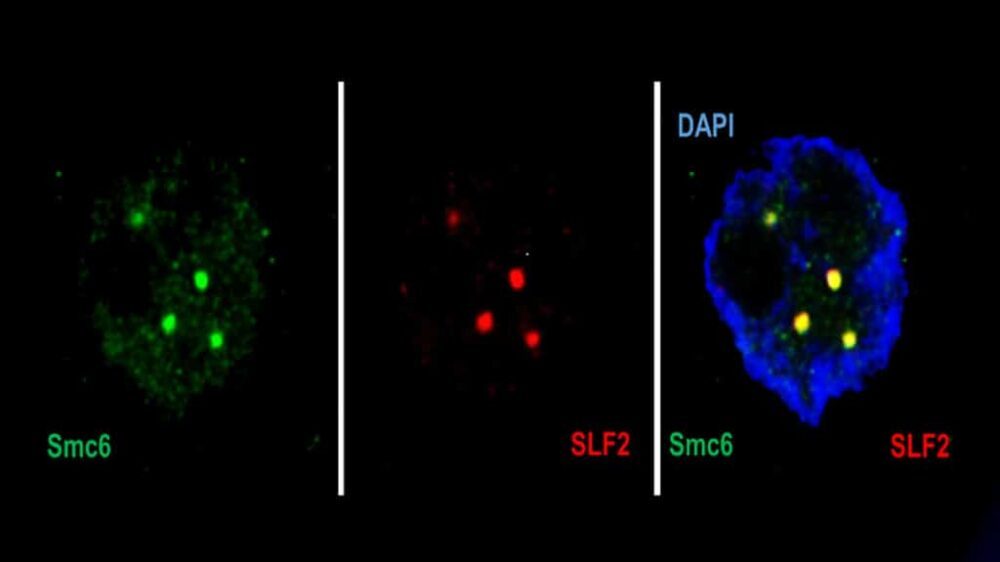
Viirus reageerib seejärel unikaalse valgu, mida nimetatakse X-valguks, vabastamisega. See valk tungib rakku ja lagundab SMC5/6, muutes selle võimetuks täitma oma valvuri rolli.
SMC5 / 6 roll viirusevastases kaitses ei olnud enne seda leidmist teada. Leiti, et see on meie kromosoomide struktuurse terviklikkuse säilitamiseks ülioluline. Michel Strubini meeskond on täna teinud uue arenduse. UNIGE teadlased on koostöös Ameerika ravimifirma Gilead Sciencesiga läbi viinud uuringus kindlaks määranud kolm protsessi ja spetsiifilised valgud, mis on vajalikud SMC5/6 viirusevastase funktsiooni täitmiseks.
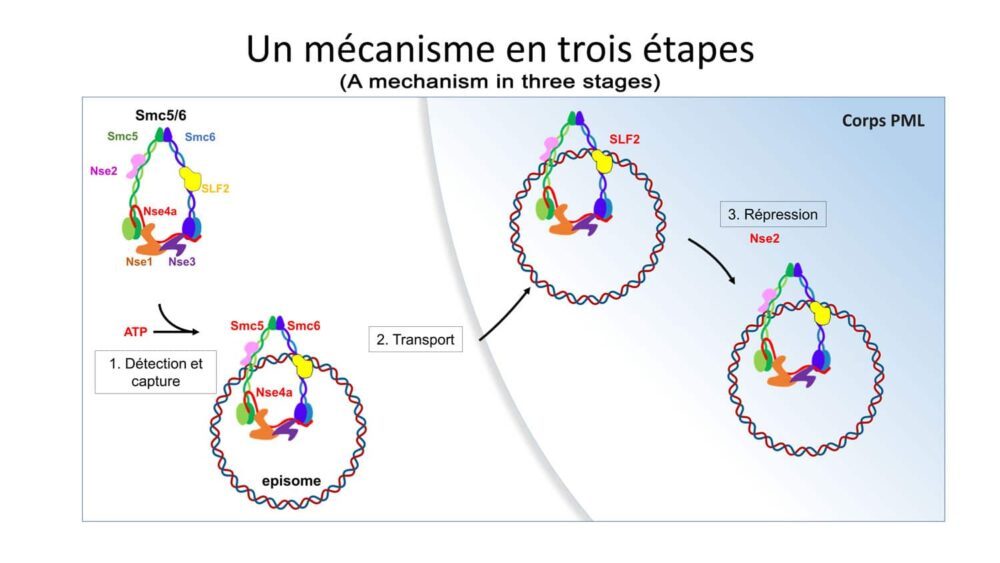
Fabien Abdul, UNIGE arstiteaduskonna mikrobioloogia ja molekulaarmeditsiini osakonna vanemteadur ja õppejõud, ütles: "Esimeses etapis tuvastab SMC5/6 kompleksi valk viiruse DNA ja püüab selle kinni. Seejärel viib kompleksi teine valk – SLF2 – viiruse kinnijäänud DNA rünnatud raku tuuma alamkambrisse, mida nimetatakse PML-i kehaks. Kolmas valk – Nse2 – tuleb siis mängu ja pärsib viirust. kromosoom. "
"Kuna SMC on suur valgukomplekside perekond, tahtsid teadlased ka teada, kas selle perekonna teised "liikmed" on võimelised seonduma B-hepatiidi viiruse DNA-ga. Avastasime, et see pädevus oli SMC5/6 jaoks ainulaadne.
Michel Strubin, uuringu viimane autor, ütles: "Nende tulemuste saavutamiseks töötasime in vitro rakukultuuride kallal. Kasutasime molekulaarbioloogia tehnikaid ja täpsemalt geneetilisi kääre nn CRISPR-case.9. See tööriist võimaldas meil lõigata DNA ahelad rakkudes ja seega kustutada või muuta geeni, mis kodeerib iga SMC5/6 kompleksi moodustavat valku.
"Tänu sellele tehnikale saame panna ühe või teise valgu kaduma ja seeläbi mõista nende vastavaid funktsioone kompleksis. Nende tähelepanekute põhjal saab kindlaks teha viirusevastase mehhanismi kolm etappi.
Aurélie Diman, Michel Strubini labori järeldoktor, ütles, "See avastus annab parema ülevaate sellest, kuidas kompleks oma viirusevastase toime ajal toimib. See võib seega sillutada teed uute terapeutiliste sihtmärkide tuvastamiseks B-hepatiidi viiruse vastu võitlemiseks. Järgmine uurimisetapp seisneb viiruse inhibeerimismehhanismi paremas dešifreerimises raku tuuma alamkambris.
Ajakirja viide:
- Abdul, F., Diman, A., Baechler, B. et al. Smc5/6 vaigistab episomaalse transkriptsiooni kolmeastmelise funktsiooni abil. Nat Struct Mol Biol 29, 922–931 (2022). DOI: 10.1038/s41594-022-00829-0