Naha melanoom on kõigist nahavähkidest kõige surmavam, eriti seetõttu, et sellel on kalduvus tungida ja tekitada metastaase kaugemates kohtades. See on kolmas primaarne pahaloomuline kasvaja pärast kopsu- ja rinnavähki, mis koloniseerib eelistatavalt aju, kusjuures esineb aju metastaaside teke.
Esimest korda uurisid teadlased alates Tel Avivi ülikooli harutas lahti mehhanismi, mis võimaldab nahavähil metastaaseeruda ajju ja suutis olemasolevate ravimeetodite abil haiguse levikut edasi lükata 60–80%. Nad leidsid, et vähirakud "värbavad" astrotsüüte, tähekujulisi rakke, mis asuvad seljaajus ja ajus ja mis vastutavad homöostaasi ehk stabiilsete tingimuste säilitamise eest. aju, ajumetastaasidega melanoomiga patsientidel.
Prof Ronit Satchi-Fainaro ütles: Kaugelearenenud staadiumis tekivad 90% melanoomi (nahavähi) patsientidest ajumetastaasid. See on mõistatuslik statistika. Me eeldame metastaase kopsudes ja maksas, kuid aju peaks olema kaitstud organ. Hematoentsefaalbarjäär hoiab ära kahjulike ainete sisenemise ajju ja siin see väidetavalt ei täida oma ülesannet – naha vähirakud ringlevad veres ja jõuavad ajju. Küsisime endalt, kellega vähirakud ajus räägivad, et sinna imbuda.
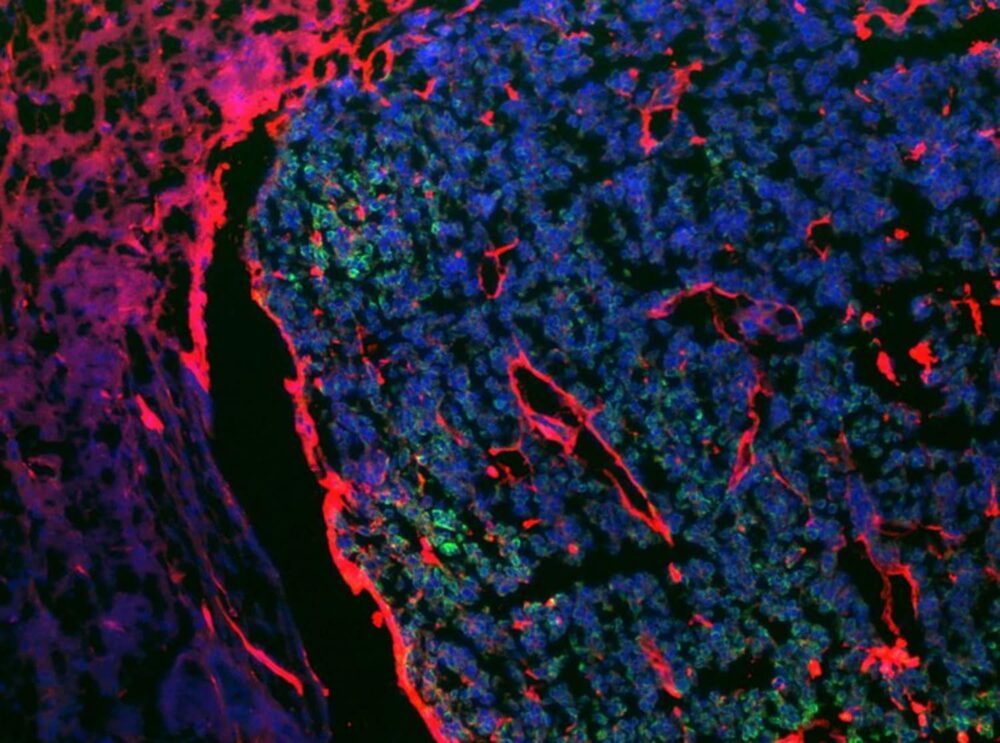
Prof Satchi-Fainaro ütles: "Astrotsüüdid on esimesed, kes näiteks insuldi või trauma korral olukorda parandavad ja just nendega koos vähirakkude omavahel suhelda, molekule vahetades ja neid rikkudes. Veelgi enam, vähirakud värbavad astrotsüüte, nii et need ei pärsi metastaaside levikut. Sellisena tekitavad nad melanoomirakkude ja astrotsüütide interaktsioonipiirkondades lokaalset põletikku, mis suurendab läbilaskvust läbi hematoentsefaalbarjääri ning vähirakkude jagunemist ja migratsiooni.
"Nendevaheline suhtlus peegeldub selles, et astrotsüüdid hakkavad sekreteerima põletikku soodustavat valku nimega MCP-1 (tuntud ka kui CCL2) ja vastusena sellele hakkavad vähirakud ekspresseerima oma retseptoreid CCR2 ja CCR4. mida me kahtlustasime olevat vastutavad hävitava suhtlemise eest astrotsüütidega.
Teadlased kontrollisid oma hüpoteesi, inhibeerides valgu ja selle retseptorite ekspressiooni geneetiliselt muundatud laborimudelites ning primaarse melanoomi ja aju metastaaside 3D-mudelites. Nad kasutasid nii antikeha (bioloogiline molekul) kui ka väikest (sünteetilist) molekuli, mis olid loodud MCP-1 valgu blokeerimiseks.
Nad kasutasid ka CRISPR-tehnoloogiat vähirakkude geneetiliseks redigeerimiseks ja kahe asjakohast retseptorit CCR2 ja CCR4 ekspresseerivate geenide väljalõikamiseks. Iga meetodiga võivad teadlased metastaaside levikut edasi lükata.
Prof Satchi-Fainaro ütles, "Need ravimeetodid aitasid edasi lükata vähirakkude tungimist ajju ja nende edasist levikut kogu ajus. Oluline on märkida, et melanoomi metastaasid ajus on väga agressiivsed ja halva prognoosiga 15 kuud pärast operatsiooni, kiiritust ja keemiaravi. Sõltuvalt sekkumisetapist jõudsime 60–80% hilinemiseni.
“Parimate tulemusteni jõudsime vahetult pärast esmase melanoomi eemaldamise operatsiooni läbiviidud raviga ning suutsime ära hoida metastaaside tungimise ajju; seetõttu usun, et ravi sobib kliinikule ennetava meetmena.“
"Nii antikeha kui ka väikest molekuli, mida me kasutasime – mis on mõeldud peamiselt skleroosi, diabeedi, maksafibroosi ja südame-veresoonkonna haiguste raviks, samuti teiste vähitüüpide biomarkerina – on kliiniliste uuringute osana juba testitud inimestel. . Seetõttu on need ravimeetodid ohutud ja me võime proovida neid melanoomi jaoks uuesti kasutada.
Ajakirja viide:
- Sabina Pozzi, Anna Scomparin jt. MCP-1 / CCR2 telje inhibeerimine sensibiliseerib aju mikrokeskkonda melanoomi aju metastaaside progresseerumise vastu. JCI Insight. DOI: 10.1172/jci.insight.154804